Στο θέμα Γ3 δίνονταν οι παρακάτω 3 δείκτες (τα χρώματα των δύο μορφών δεν δίνονταν αλλά τα έχω προσθέσει εγώ ώστε να μπορέσετε να «παρακολουθήσετε» καλύτερα την πειραματική διαδικασία)
- Κίτρινο της αλιζαρίνης με pKa=11 (κίτρινο – κόκκινο)
- Πορφυρό της βρωμοκρεσόλης με pKa=6,4 (κίτρινο – πορφυρό)
- Ηλιανθίνη με pKa=3,5 (κόκκινο – κίτρινο)
Μπορείτε να διαβάσετε τη συνέχεια:
ΘΕΜΑ Γ3 Πανελλαδικών εξετάσεων Χημείας.
![]()
Καταπληκτική η ανάλυση σου Αντώνη. Μακάρι να την δουν οι θεματοδότες οι οποίοι υποθέτω ότι δεν θεώρησαν την διάσταση που παρουσιάζεις. Τελικά χρειάζεται πολύ μεγάλη προσοχή όταν βάζεις θέματα που αφορούν 80000 με 90000 υποψηφίους. Πρέπει να λαμβάνει υπόψη ο θεματοδότης τι μπορεί να απαντήσει ακόμα κι ένα μικρό ποσοστό «ψαγμένων» μαθητών, οι οποίοι τελικά ίσως χάσουν αρκετά μόρια ως τιμωρία που σκέφτηκαν πιο σωστά από τους πολλούς…
Σε ευχαριστώ πολύ Ανέστη.
Μακάρι η πραγματική πειραματική διδασκαλία των Φυσικών Επιστημών να πραγματοποιηθεί κάποτε στη χώρα μας.
Προς το παρόν η χαρτοχημεία ζει και βασιλεύει!
Έχω προσθέσει στο αρχικό pdf ακόμη μια σελίδα στην οποία μελετάω τα σφάλματα στον υπολογισμό της συγκέντρωσης του ογκομετρούμενου διαλύματος σε κάθε μία από τις 2 περιπτώσεις μετά τη χρήση κάθε δείκτη. Υπενθυμίζω ότι οι καμπύλες έχουν σχεδιαστεί θεωρώντας ότι προσθέτουμε σταγόνα – σταγόνα (0,05 mL) το πρότυπο διάλυμα στο ογκομετρούμενο διάλυμα.
Στην 1η ογκομέτρηση (ΗΑ + NaOH):
· Σε pH=12 έχεις χρησιμοποιήσει V=22,1 mL πρότυπου διαλύματος και η συγκέντρωση του ΗΑ που θα υπολογίζαμε πειραματικά θα ήταν c = 0,2210 M. Μετά από υπολογισμούς βρίσκουμε ότι με τον συγκεκριμένο δείκτη θα είχαμε ένα θετικό σφάλμα στον υπολογισμό της συγκέντρωσης ίσο με 10,5 %.
· Σε pH=7,4 έχεις χρησιμοποιήσει V=19,25 mL πρότυπου διαλύματος και η συγκέντρωση του ΗΑ που θα υπολογίζαμε πειραματικά θα ήταν c = 0,1925 M. Μετά από υπολογισμούς βρίσκουμε ότι με τον συγκεκριμένο δείκτη θα είχαμε ένα αρνητικό σφάλμα στον υπολογισμό της συγκέντρωσης ίσο με 3,75 %.
Στη 2η ογκομέτρηση (B + HCl):
Σε pH=5,4 έχεις χρησιμοποιήσει V=19,95 mL πρότυπου διαλύματος (1 σταγόνα πριν το ΙΣ) και η συγκέντρωση του ΗΑ που θα υπολογίζαμε πειραματικά θα ήταν c = 0,1995 M. Μετά από υπολογισμούς βρίσκουμε ότι με τον συγκεκριμένο δείκτη θα είχαμε ένα αρνητικό σφάλμα στον υπολογισμό της συγκέντρωσης της Β ίσο με 0,25 %.
Σε pH=2,5 έχεις χρησιμοποιήσει V=20,65 mL πρότυπου διαλύματος (13 σταγόνες μετά το ΙΣ) και η συγκέντρωση του ΗΑ που θα υπολογίζαμε πειραματικά θα ήταν c = 0,2065 M. Μετά από υπολογισμούς βρίσκουμε ότι με τον συγκεκριμένο δείκτη θα είχαμε ένα θετικό σφάλμα στον υπολογισμό της συγκέντρωσης της Β ίσο με 3,25 %.
Να ευχαριστήσω τον Γιώργο Βαρελά για ένα υπέροχο αρχείο excel που μου έδωσε ώστε να γίνουν όλοι αυτοί οι υπολογισμοί!
Συνοπτικά έχουμε τα εξής:
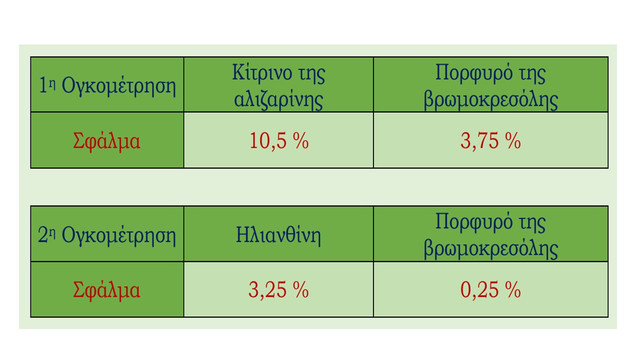
Αντώνη πριν δω την λεπτομερή σου ανάλυση, θεωρούσα ότι το πορφυρό της Βρωμοκρεσόλης ήταν ισοδύναμης καταλληλότητας (πειραματικά και όχι χαρτοχημικά) με την αλιζαρίνη στην Υ1 και με την ηλιανθίνη στην Υ2. Από την ανάλυση σου φαίνεται όμως ότι είναι και ο καταλληλότερος από τους τρεις που έχουν δοθεί!
Αντώνη συγχαρητήρια ότι και να πω είναι λίγο. Δεν περίμενα βέβαια κάτι λιγότερο από σένα. Θα πρέπει να κάνεις ένα σεμινάριο στους θεματοδότες. Πόσο αδικημένος δείκτης είναι τελικά το πορφυρό της βρωμοκρεσόλης! Ας τελειώσουν αύριο τα παιδιά με τις εξετάσεις και νομίζω μπορούμε να πούμε πολύ περισσότερα.
Συγνώμη Ανέστη η απάντηση αφορούσε τον Αντώνη.
Σε ευχαριστώ Αντώνη.
Κατανοώ απολύτως το σκεπτικό της τελευταίας σου πρότασης.
Σχετικά με το Γ3:
Το βιβλίο δίνει ως κριτήριο: α) η περιοχή pH αλλαγής χρώματος να περιέχει το ισοδύναμο σημείο ή β)τουλάχιστον να βρίσκεται στο κατακόρυφο τμήμα της καμπύλης.
Το (α) αποκλείεται, αφού οι προτεινόμενοι δείχτες δεν πληρούν τις προϋποθέσεις.
Για το (β) χρειαζόταν να είναι βαθμονομημένος ο άξονας με τις τιμές του pH.
Σε μια προσπάθεια να βαθμονομήσω τον άξονα και να χρησιμοποιήσω τις γραφικές παραστάσεις για να δω που βρίσκονται οι περιοχές pH αλλαγής χρώματος των δεικτών, διαπίστωσα ότι δεν είναι σχεδιασμένoς υπό κλίμακα ή αφορά άλλες ογκομετρήσεις. Δηλ. το Ι.Σ. στην πρώτη είναι στο 8,5 (κανονικά 9.5) και στη δεύτερη το αρχικό pH είναι 9 (κανονικά περίπου 10,65). Άρα ούτε έτσι μπορεί να απαντηθεί αυτό το ερώτημα.
Η ΚΕΕ και αρκετοί μαθητές χρησιμοποιούν το «διαισθητικό» κριτήριο της επιλογής του δείχτη που «είναι πιο κοντά στο Ι.Σ» χωρίς όμως αυτό να αναφέρεται κάπου στο σχολικό βιβλίο. Εγώ το έχω συναντήσει μόνο σε βοηθήματα. (Βέβαια, απ’ ότι προκύπει από τη συζήτηση εδώ, αυτό δεν επιβεβαιώνεται πειραματικά).
Αρχικά θα ήθελα να χαιρετίσω όλο το ”Υλικό”, συναδέλφους και μαθητές μιας και μόλις πριν λίγο έγινα μέλος και αυτό είναι το πρώτο μου σχόλιο.Αντώνη παρακολουθώ πάντα με ενδιαφέρον τις αναρτήσεις σου και σου δίνω συγχαρητήρια για όσα έχεις προσφέρει σε όλους μας. Θα ήθελα να σχολιάσω την ανάλυση σου στο θέμα Γ3 των Πανελλαδικών Εξετάσεων.
Ας πάρουμε την πρώτη ογκομέτρηση (του Υ1) όπου ογκομετρείται το ασθενές οξύ HA με το NaOH. Αυτό που προτείνεις είναι ότι καταλληλότερος(ή εξίσου κατάλληλος) δείκτης για την ογκομέτρηση είναι το πορφυρό της βρωμοκρεσόλης και όχι το κίτρινο της αλιζαρίνης. Το βασικό σου επιχείρημα είναι ότι ο πειραματιστής θα δει τη χρωματική αλλαγή με σιγουριά στο τέλος της περιοχής pH αλλαγής χρώματος του δείκτη. Το επιχείρημα αυτό πιστεύω πως δεν ισχύει για ένα δείκτη όπως το πορφυρό της βρωμοκρεσόλης όπου η περιοχή pH αλλαγής χρώματος του δεν βρίσκεται στο κατακόρυφο τμήμα της καμπύλης(σύμφωνα και με τη δική σου καμπύλη) αλλά ισχύει για δείκτες που η περιοχή pH αλλαγής χρώματος τους βρίσκεται στο κατακόρυφο τμήμα (ή τουλάχιστον το μεγαλύτερο τμήμα της είναι στο κατακόρυφο τμήμα). Στην τελευταία περίπτωση ακόμα και μικρή προσθήκη πρότυπου διαλύματος κοντά στο ΙΣ μεταβάλει δραματικά το pH και η χρωματική αλλαγή γίνεται πολύ απότομα οπότε ο πειραματιστής θα δει την αλλαγή του χρώματος περίπου στο τέλος της περιοχής pH αλλαγής χρώματος του δείκτη. Στην περίπτωση όμως της βρωμοκρεσόλης η αλλαγή στο χρώμα ξεκινάει από περίπου τα 5mL πρότυπου(όπως πρόχειρα βλέπω από την καμπύλη) που αντιστοιχεί σε pH 5,4 και φτάνει μέχρι τα 19,25 mL πρότυπου που αντιστοιχεί σε pH 7,4. Δηλαδή για να αλλάξει εντελώς το χρώμα του δείκτη πρέπει να προστεθούν περίπου 14 mL πρότυπου διαλύματος! Είναι δυνατόν να μην έχει παρατηρηθεί αλλαγή στο χρώμα πολύ πιο πριν;
Δεν είχα προσέξει Κωνσταντίνε ότι δεν ήταν σχεδιασμένοι υπό κλίμακα οι άξονες που δόθηκαν στα θέματα των εξετάσεων! Δηλαδή ήταν από μια άσχετη αλκαλιμετρία!
Δημήτρη καλησπέρα.
Από την αρχή του μηνύματός σου αντιλαμβάνομαι ότι είμαστε συνάδελφοι οπότε θα προσπαθήσω να απαντήσω στην παρατήρησή σου διαφορετικά από ότι σε ένα μαθητή.
Κάθε δείκτης είναι σχεδόν μια ιδιαίτερη περίπτωση.
Δηλαδή αυτές οι 2 μονάδες pH που λέμε ότι είναι η περιοχή αλλαγής χρώματος είναι κάτι εντελώς θεωρητικό και εξαρτάται από τον δείκτη που χρησιμοποιείς.
Για παράδειγμα το κίτρινο της αλιζαρίνης έχει περιοχή pH αλλαγής χρώματος 10,2 – 12,0 , το πορφυρό της βρωμοκρεσόλης 5,2 -6,8 , η ηλιανθίνη (πορτοκαλί του μεθυλίου) 3,2 – 4,4 και το βάμμα του ηλιοτροπίου 4,5 – 8,3!!! Επίσης υπάρχουν δείκτες που έχουν 2 περιοχές pH αλλαγής χρώματος (πχ. μπλε της θυμόλης).
Στη συνέχεια θα ήθελα να αναφέρω ότι υπάρχουν κάποιοι δείκτες που είναι «εύκολοι» και κάποιοι «δύσκολοι». Εννοώ υπάρχουν δείκτες όπου οι χρωματικές αλλαγές είναι αρκετά εύκολα αντιληπτές (πχ. φαινολοφθαλεΐνη) αλλά υπάρχουν και κάποιοι όπου οι χρωματικές αλλαγές γίνονται δύσκολα αντιληπτές (πχ βάμμα ηλιοτροπίου).
Επίσης υπάρχουν ογκομετρήσεις όπου σταματάς μόλις αντιληφθείς μια πολύ μικρή χρωματική αλλαγή και κάποιες άλλες όπου προσθέτεις πρότυπο διάλυμα μέχρις ότου σταθεροποιηθεί το χρώμα στο διάλυμα.
Βέβαια αντιλαμβάνομαι ότι το σχολικό βιβλίο πρέπει να κάνει γενικεύσεις. Οπότε αναφέρει 2 μονάδες ως ενδιάμεσο χρώμα και πλήρη χρωματική αλλαγή σε pKa-1 ή pKa+1. Αυτό ήταν το σκεπτικό μου και εμένα στην παραπάνω ανάλυση. Πόσο πολύ διαφέρει η πλήρης χρωματική αλλαγή σε κάθε δείκτη από το pH στο ισοδύναμο σημείο. Δηλαδή είχα τα ίδια κριτήρια για κάθε δείκτη.
Οπότε, συνεχίζω να αναφέρω ότι με τα κριτήρια που έχει ένας μαθητής καταλληλότερος είναι ο δείκτης πορφυρό της βρωμοκρεσόλης και για τις δύο ογκομετρήσεις.
Κατά τη γνώμη μου και για τις δύο ογκομετρήσεις καταλληλότεροι δείκτες είναι αυτοί που δίνει η ΚΕΕ δηλ. για την ογκομέτρηση του Υ1 το κίτρινο της αλιζαρίνης και για την ογκομέτρηση του Υ2 η ηλιανθίνη, είτε κοιτάξουμε το θέμα από την οπτική γωνία ενός πειραματιστή χημικού είτε το δούμε από την οπτική ενός μαθητή που διαγωνίστηκε στις Πανελλαδικές εξετάσεις. Θα χωρίσω την ανάλυση μου λοιπόν σε δύο μέρη και για να είμαι πιο σύντομος θα αναφερθώ κυρίως στην ογκομέτρηση του Υ1.
Οπτική γωνία πειραματιστή
Σε ένα χημικό δίνεται α) η καμπύλη ογκομέτρησης του Υ1(και όλα τα απαραίτητα δεδομένα για να προκύψει αυτή), β) το pH στο ΙΣ (9,5) και του ζητείται να διαλέξει έναν από τους δύο δείκτες(κίτρινο της αλιζαρίνης με pKa=11 ή πορφυρό της βρωμοκρεσόλης με pKa=6,4) σαν τον πιο κατάλληλο για την ογκομέτρηση.
Ο χημικός ξεκινάει με το δείκτη πορφυρό της βρωμοκρεσόλης και σκέφτεται: πώς θα κάνω το δείκτη αυτό να ΄΄δουλέψει΄΄ όσο το δυνατόν καλύτερα για αυτή την ογκομέτρηση; Επειδή η περιοχή pH στην οποία αλλάζει χρώμα ο δείκτης βρίσκεται πριν το ΙΣ (και μάλιστα κανένα τμήμα της περιοχής αυτής δεν βρίσκεται στο κατακόρυφο τμήμα της καμπύλης) ο χημικός σκέφτεται ότι για να έχει την μεγαλύτερη δυνατή ακρίβεια θα πρέπει να σταματήσει την ογκομέτρηση όταν αλλάξει εντελώς το χρώμα του δείκτη και καταλήξει να γίνει πορφυρό(γιατί πιο πριν θα έχει πολύ μεγάλο σφάλμα).Το πρόβλημα είναι ότι η αλλαγή χρώματος του δείκτη αυτού γίνεται σε ένα πολύ μεγάλο εύρος τιμών mL πρότυπου διαλύματος(από 5-19,25 mL περίπου λόγω της ύπαρξης ΡΔ όπως ξέρουμε πριν το ΙΣ). Όταν λοιπόν έχουμε μία τόσο αργή αλλαγή χρώματος ο πειραματιστής έχει μεγάλη αμφιβολία στο πότε θα σταματήσει την ογκομέτρηση, ποιο είναι δηλαδή το τελικό σημείο γιατί η αλλαγή στο χρώμα δεν είναι δραστική οπότε έχουμε και μεγαλύτερα σφάλματα. Ας πούμε όμως ότι τελικά αντιπαρέρχεται αυτή τη δυσκολία και ρίχνει τόση ποσότητα προτύπου που το pH καταλήγει στην τιμή 7,4.
Πάει τώρα στον άλλο δείκτη το κίτρινο της αλιζαρίνης και κάνει παρόμοιες σκέψεις. Δηλαδή σκέφτεται πώς θα τον κάνει να ΄΄δουλέψει΄΄ όσο το δυνατόν καλύτερα. Λέει λοιπόν ότι αφού η περιοχή pH στην οποία αλλάζει χρώμα ο δείκτης βρίσκεται μετά το ΙΣ (και μάλιστα ένα τμήμα της περιοχής αυτής βρίσκεται στο κατακόρυφο τμήμα της καμπύλης) αυτό που θα μου δώσει μεγαλύτερη ακρίβεια θα είναι να σταματήσω την ογκομέτρηση ακριβώς όταν παρατηρήσω να αλλάζει έστω και λίγο το χρώμα του δείκτη από κίτρινο σε πορτοκαλί(το ενδιάμεσο χρώμα). Ας συμφωνήσουμε ότι η αλλαγή από κίτρινο σε πορτοκαλί θα παρατηρηθεί σε pH 11 δηλ. σε pH ίσο με την pKa του δείκτη και επίσης μην ξεχνάμε ότι με αυτόν το δείκτη θα είναι απείρως πιο εύκολο να προσδιοριστεί το τελικό σημείο της ογκομέτρησης μιας και το αρχικό τμήμα της περιοχής αλλαγής χρώματος βρίσκεται στο κατακόρυφο τμήμα της καμπύλης οπότε η χρωματική αλλαγή από κίτρινο σε πορτοκαλί θα είναι πολύ δραστική και θα παρατηρηθεί εύκολα.
Τελικό συμπέρασμα για τον φίλο μας τον πειραματιστή είναι ότι με το κίτρινο της αλιζαρίνης πετυχαίνει να βρεθεί πιο κοντά στο pH στο ΙΣ (9,5)!!
Την οπτική του μαθητή θα προσπαθήσω να την ανεβάσω αύριο ή μεθαύριο. Επίσης θα παραθέσω το τι απάντησαν σε γενικές γραμμές τα παιδιά στο θέμα αυτό με βάση τα 90 γραπτά που διόρθωσα(πιστεύω ότι είναι πολύ σημαντικό).
Πριν πάω στην οπτική γωνία του μαθητή θα πρέπει να αναφέρω ότι στην ανάλυση μου για την ογκομέτρηση του διαλύματος Υ1 ΄΄αβάνταρα΄΄ τον δείκτη πορφυρό της βρωμοκρεσόλης θεωρώντας ότι το pH στο τελικό σημείο θα είναι 7,4 δηλαδή όταν θα έχει εγκαθιδρυθεί πλήρως το πορφυρό χρώμα. Στην πραγματικότητα το pH στο τελικό σημείο θα είναι μικρότερο του 7,4 (αν θέλουμε να δώσουμε μια περιοχή θα είναι κάπου μεταξύ του 6,9 και του 7,4 με όλες τις δυσκολίες που ανέφερα στον εντοπισμό του τελικού σημείου). Στον αντίποδα τον δείκτη κίτρινο της αλιζαρίνης τον ΄΄έριξα΄΄ θεωρώντας ότι σε αυτή την περίπτωση το pH στο τελικό σημείο θα είναι 11 δηλαδή όταν θα έχει εγκαθιδρυθεί πλήρως το πορτοκαλί χρώμα(που είναι το ενδιάμεσο χρώμα). Στην πραγματικότητα το pH στο τελικό σημείο σε αυτή την περίπτωση θα είναι μικρότερο του 11 (κάπου κοντά στο 10,5 διότι μην ξεχνάμε ότι σε αυτή την περίπτωση δεν ΄΄κυνηγάμε΄΄ την εγκαθίδρυση του πορτοκαλί χρώματος αλλά του ενδιάμεσου χρώματος μεταξύ κίτρινου και πορτοκαλί).
Η ογκομέτρηση του διαλύματος Υ2(με pHΙΣ= 4,5) είναι μία ακριβώς αντίστοιχη περίπτωση μόνο που αντί για αλκαλιμετρία έχουμε οξυμετρία. Με την ίδια ανάλυση λοιπόν το pH στο τελικό σημείο εάν χρησιμοποιήσουμε το δείκτη πορφυρό της βρωμοκρεσόλης θα είναι μεγαλύτερο του 5,4(αν θέλουμε να δώσουμε μια περιοχή θα είναι κάπου μεταξύ του 5,4 και του 5,9). Εάν τώρα χρησιμοποιήσουμε το δείκτη ηλιανθίνη το pH στο τελικό σημείο θα είναι κάπου κοντά στο 4 διότι εδώ ΄΄κυνηγάμε΄΄ την εγκαθίδρυση του ενδιάμεσου χρώματος μεταξύ κίτρινου και πορτοκαλί και όχι την εγκαθίδρυση του πορτοκαλί χρώματος.
Το τελικό συμπέρασμα είναι ότι η ηλιανθίνη είναι καταλληλότερος δείκτης του πορφυρού της βρωμοκρεσόλης για την ογκομέτρηση του διαλύματος Υ2.