![]() Δημοσιεύτηκε από το χρήστη Αντώνης Χρονάκης στις 15 Δεκέμβριος 2011 στις 15:18 στην ομάδα Χημεία Γ΄Λυκείου
Δημοσιεύτηκε από το χρήστη Αντώνης Χρονάκης στις 15 Δεκέμβριος 2011 στις 15:18 στην ομάδα Χημεία Γ΄Λυκείου
“Σε μια ογκομέτρηση εξουδετέρωσης χρησιμοποιούμε ως πρότυπα διαλύματα μόνο διαλύματα ισχυρών οξέων και ισχυρών βάσεων.”
Η αποψή μου είναι οτι η παραπάνω πρόταση είναι λανθασμένη.
Συμφωνώ οτι δίνει καλύτερα πειραματικά αποτελέσματα αν χρησιμοποιήσουμε ως πρότυπο διάλυμα, κάποιο ισχυρό οξύ ή κάποια ισχυρή βάση, γιατί η μεταβολή pH είναι πολύ πιο απότομη απο τη μεταβολή που θα έχουμε αν χρησιμοποιήσουμε ασθενές οξύ ή βάση. Όμως σε καμία περίπτωση δεν μπορούμε να πούμε ……μόνο……
Τα σχόλια
 Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
-
Κατά την ογκομέτρηση πρέπει χρησιμοποιούμε ισχυρό ηλεκτρολύτη, διότι η ελαχιστότατη περίσσειά του μετά το ισοδύναμο σημείο , δίνει απότομη μεταβολή στο pH, (χρωματική αλλαγή του ογκομετρούμενου διαλύματος ) με το τελικό σημείο πάρα πολύ κοντά στο ισοδύναμοσημείο. Η ογκομέτρηση είναι ακριβέστερη όσο πιο κοντά είναι το ισοδύναμο σημείο με το τελικό σημείο .
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
…. Θεωρητικά στο εργαστήριο μπορείς να κάνεις ότι θέλεις.
Εάν ήμουν σε ένα εργαστήριο που δεν έχει ( έχει τελειώσει ) το HCl , ναι βέβαια θα έκανα ογκομέτρηση με HCOOH ( ή με οποιοδήποτε ασθενές αρκεί να ξέρω την σταθερά του ώστε να προβλέψω το pH στο ισοδύναμο σημείο και να επιλέξω τον κατάλληλο δείκτη )
Θα μπορούσα να ογκομετρήσω ένα ασθενές οξύ με μιά ασθενή βάση … μάλιστα θα επέλεγα ασθενή βάση με ίδια Κ ώστε το pH στο ισοδύναμο να είναι 7 ….!!! ( χωρίς κάν καμπύλες κτλ )
Θα μπορούσα να το «χοντρύνω» ισχυριζόμενος ότι θα μπορούσα να επιλέξω ακόμα και διπρωτικό οξύ ( ογκομετρούνται και αυτά στην τελική ) έχοντας πάντα στο μυαλό μου την επιλογή του «κατάλληλου» δείκτη.
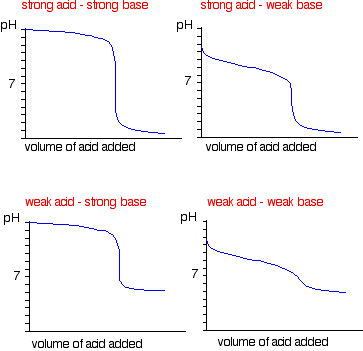
To θεμα είναι να δείς ποσο πιο καθαρά γίνεται αυτό το απότομο της μεταβολής του pH που επιτυγχάνεται όσο πιο ισχυρό είναι το «ζευγος ουσιών» που παίρνουν μέρος στην ογκομέτρηση.
Μέχρι και στην προχοίδα θα μπορούσα να βάλω το ογκομετρούμενο και από κάτω στην κωνική φιάλη το πρότυπο ( σωστά ? ) χωρίς να υπάρχει πρόβλημα αφού το θέμα μας είναι αρχικώς στοιχειομετρικό και μετά pHμετρικό ( άραγε πως θα ονομάζαμε την ογκομετρηση όπου μετράμε τον όγκο του διαλύματος HCOOH άγνωστης συγκεντρωσης που εξουδετερώνει διάλυμα NaOH γνωστής συγκεντρωσης και όγκου …. οξυμετρία ή αλκαλιμετρία ? )
Το θέμα δεν είναι εάν μπορείς αλλά εάν θές.
 Απάντηση από τον/την Αντώνης Χρονάκης στις
Απάντηση από τον/την Αντώνης Χρονάκης στις
-
Συμφωνώ απόλυτα με τα παραπάνω.
Εξ΄άλλου στην αρχική μου τοποθέτηση, εξηγώ οτι καλύτερα πειραματικά αποτελέσματα παίρνουμε με τη χρήση ισχυρού οξέος ή βάσης ως πρότυπο, λόγω απότομης μεταβολής του ρΗ.
Διαφωνώ με τη λέξη ….μόνο…..
Αν η διατύπωση ήταν…..
Στις ογκομετρήσεις εξουδετέρωσης είναι προτυμότερο να χρησιμοποιήσουμε ισχυρό οξύ ή ισχυρή βάση ως πρότυπο διάλυμα.
Θα έλεγα οτι η πρόταση είναι σωστή.
Αφού εχω τη δυνατότητα να κάνω την τιτλοδότηση και με χρήση ασθενούς (έστω και με λιγότερο «εύκολα» πειραματικά αποτελέσματα) δεν μπορώ να δεχθώ τη διατύπωση της πρότασης ως σωστή.
Όσο για το πώς θα ονομαστεί η ογκομέτρηση, δεν νομίζω πως υπάρχει πρόβλημα.
Το πρότυπο είναι αυτό που χαρακτηρίζει την ογκομέτρηση. Δηλαδή αν χρησιμοποιούμε ως πρότυπο οξύ, η ογκομέτρηση ονομάζεται οξυμετρία ή αν χρησιμοποιήσουμε ως πρότυπο βάση αλκαλιμετρία. Ανεξάρτητα αν είναι ισχυρό ή ασθενές.
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
…. πάντως μάλλον όλοι θα συμφωνουσάμε ότι είναι ένα «κακοπροαίρετο» Σ/Λ
 Απάντηση από τον/την Βιβή Γεωργίου στις
Απάντηση από τον/την Βιβή Γεωργίου στις
-
Ένα ενδιαφέρον applet για την ογκομέτρηση βρίσκεται εδώ.
Δοκιμάστε ένα ασθενές οξύ στο πρότυπο διάλυμα (πχ HCOOH με Ka=2,1×10-4) και ογκομετρήστε διάλυμα μιας πολύ ασθενούς βάσης (πχ πυριδίνης με Kb=10-9). Η ογκομέτρηση δεν είναι απλά δύσκολη, είναι αδύνατη.
Υποθέτω ότι όταν επιλέγουμε πρότυπο διάλυμα για ογκομέτρηση, εννοείται ότι αυτό θα πρέπει να μπορεί χρησιμοποιηθεί για κάθε τιτλοδοτούμενο διάλυμα. Οπότε η έκφραση «μόνο ισχυρών» θα έπρεπε να είναι σωστή, γιατί ισχύει στη γενική περίπτωση…
Αν τώρα αυτός που την έγραψε, εννοούσε τι μπορεί να κάνει κανείς για μια φορά μόνο στο εργαστήριο αν θέλει να ογκομετρήσει διάλυμα ΝαΟΗ και διαθέτει οξικό οξύ… τι να πω… τότε η πρόταση είναι λάθος…
Μάλλον θα συμφωνούσα στο ότι είναι πρόχειρα διατυπωμένη…
 Απάντηση από τον/την Σιάπκας Δημήτρης στις
Απάντηση από τον/την Σιάπκας Δημήτρης στις
-
Το σχολικό βιβλίο στην άσκηση 90 σελ 152 ζητάει να βρεθεί ποιος δείκτης είναι κατάλληλος για την ταυτοποίηση του σημείου εξουδετέρωσης CH3COOH με NH3.
 Απάντηση από τον/την Βιβή Γεωργίου στις
Απάντηση από τον/την Βιβή Γεωργίου στις
-
Οπότε θεωρείται ότι χρησιμοποιείται ως πρότυπο το διάλυμα της αμμωνίας;
(αν και η άσκηση δε μιλάει για ογκομέτρηση… θα μπορούσε να είναι μια εξουδετέρωση οξέος από βάση για οποιοδήποτε άλλο λόγο, ίσως; )
![]()
Συμφωνώ Αντώνη ότι η πρόταση είναι λανθασμένη. Και θα πρόσθετα ότι αν πάρουμε την καμπύλη ογκομέτρησης έχουμε πολύ περισσότερες χρήσιμες πληροφορίες, αν το ένα από τα δυο (οξύ ή βάση) είναι ασθενές.
…. εντάξει … θεωρητικά μπορείς να επιλέξεις ότι θέλεις.
Στην πραγματικότητα – ρεαλιστικά – η επιλογή ισχυρού ηλεκτρολύτη ώς πρότυπο είναι μονόδρομος. Θα επιλέγατε ποτέ για την τιτλοδότηση διαλύματος HCl ένα διάλυμα ΝΗ3 ????
Παραθέτω από βιβλίο του Βασιλικιώτη
«Δια την παρασκευήν προτύπου δ/τος οξέος επιλέγεται το κατάλληλον οξύ επι τη βάσει των κατωθι απαιτήσεων:
α. Το οξύ πρέπει να είναι ισχυρό δηλ πλήρως διιστάμενον εις αραιά διαλύματα
β. Το διάλυμα οξέως να είναι σταθερόν επ΄αρκετον χρονικόν διάστημα και το οξύ να μην είναι πτητικόν
γ. Τα πλείστα των αλάτων του οξέος να είναι ευδιάλυτα εις το ύδωρ εφ’οσον χρησιμοποιούμεν υδατικά διαλύματα.
δ. το οξύ να μην παρουσιάζει εντόνους οξειδωτικάς ιδιότητας δια να μην καταστρέφη οξειδώνοντας τας χρησιμοποιούμένας ως δείκτας οργανικάς ενώσεις
Αντώνη να το διατυπώσω κάπως αλλιώς…
Μπορείς να κάνει τιτλοδότηση ενός ασθενούς οξέως χρησιμοποιώντας ως πρότυπο κάποια ισχυρή βάση.
Εχει διαφορά η τιτλοδότηση της ίδιας ισχυρής βάσης χρησιμοποιώντας ως πρότυπο το ίδιο ασθενές οξύ?
π.χ
Ογκομετρούμε CH3COOH με πρότυπο ΝαΟΗ.
Γιατί δεν μπορούμε να ογκομετρήσουμε ΝαΟΗ με πρότυπο CH3COOH?
Οι δυο παραπάνω διαδικασίες οδηγούν στα ίδια πειραματικά αποτελέσματα.