 Δημοσιεύτηκε από το χρήστη Αντώνης Μπαλτζόπουλος στις 3 Ιούνιος 2013 στις 15:08 στην ομάδα Χημεία Γ΄Λυκείου
Δημοσιεύτηκε από το χρήστη Αντώνης Μπαλτζόπουλος στις 3 Ιούνιος 2013 στις 15:08 στην ομάδα Χημεία Γ΄Λυκείου
Τα ρυθμιστικά διαλυματα ογκομετρούνται ακριβώς όπως και τα διαλύματα οξέων και βάσεων αλλά επειδή σε αυτά συνυπάρχουν ΚΑΙ οξύ ΚΑΙ βάση μπορούμε να εφαρμόσουμε ΚΑΙ οξυμετρία ΚΑΙ αλκαλιμετρία
Παράδειγμα …. ογκομέτρηση 10 mL διαλύματος CH3COOH 0.1 M – CH3COONa 0.1 M με πρότυπο διάλυμα ΝαΟΗ 0,1 Μ ( αλκαλιμετρία )
Στο ισοδύναμο σημείο 0.1*0.01=0.1*Vισ και μένει CH3COONa με συγκέντρωση (0,1*0,01+0,1*0,01) / (0,01+Vισ)
Το πείραμα στο Iridium
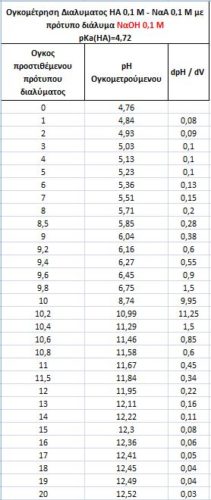
και οι καμπύλες τιτλοδότησης ( με την πολύ εντυπωσιακή dpH/dV )
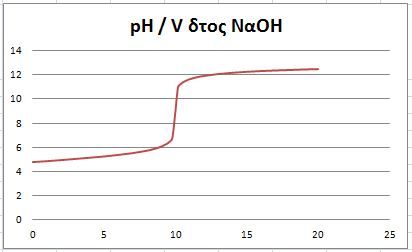
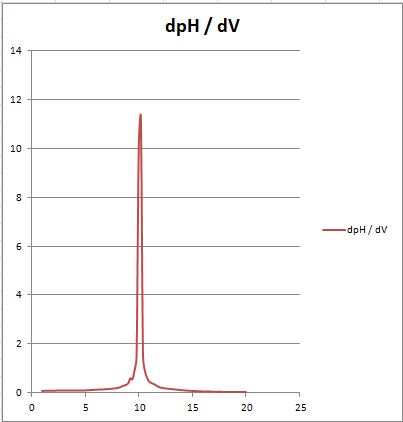
Η ίδια ογκομέτρηση μπορούσε να γίνει με την χρήση όξινου πρότυπου διαλύματος ( πχ δ/μα HCL 0.1 M ) όπου θα γράφαμε CH3COONa + HCL –> CH3COOH + NaCL όπου στο ισοδύναμο σημείο η συγκέντρωση του CH3COOH θα πρόεκυπτε από την άθροιση των αρχικών mol του CH3COOH και των mol που θα παραχθούν από την αντίδραση ( πρός τον νέο όγκο )
To Yridium για την οξυμετρική τιτλοδότηση του αρχικού ρυθμιστικού διαλύματος δίνει τα παρακάτω αποτελέσματα
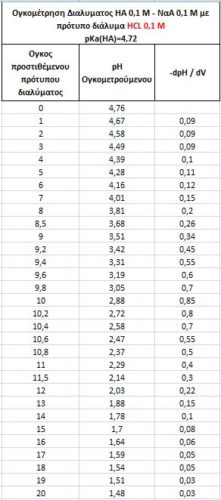
Που δίνει τις παρακάτω καμπύλες τιτλοδότησης
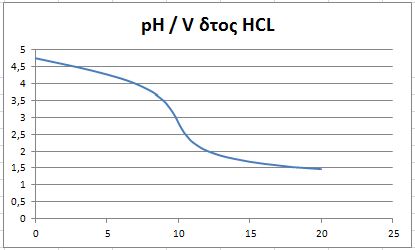
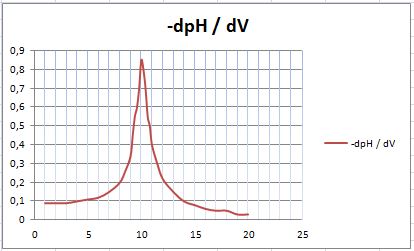
Σε αυτήν την περίπτωση αξίζει να σημειωθεί
1) μια καμπύλη τιτλοδότησης ( pH/V ) που δεν “περνά” από το 7 ( κινείται εξ’ολοκλήρου στην όξινη περιοχή )
2) την χρησιμότητα της 1ης παραγώγου
Με την χρησιμοποίηση κατάλληλων δεδομένων ( pHαρχ – Vισ – pHισ ) μπορούμε να δημιουργήσουμε ένα σύστημα εξισώσεων 2×2 και να βρούμε τις συγκεντρώσεις των ουσιών του ρυθμιστικού διαλύματος
![]()