 Δημοσιεύτηκε από το χρήστη Κατερίνα Μπόνια στις 19 Οκτώβριος 2016 στις 11:31 στην ομάδα Χημεία Γ΄Λυκείου
Δημοσιεύτηκε από το χρήστη Κατερίνα Μπόνια στις 19 Οκτώβριος 2016 στις 11:31 στην ομάδα Χημεία Γ΄Λυκείου
Καλημέρα.’Ηθελα να ρωτήσω στην προσθήκη αδρανούς αερίου σε σύστημα που βρίσκεται σε ισορροπία είναι εντός ύλης μόνο η προσθήκη υπό σταθερό όγκο και θερμοκρασία.την προσθήκη υπο σταθερή πίεση όπου έχουμε μετατόπιση της θέσης Χ.Ι την αναφέρουμε στο φροντιστήριο;;;
![]()
Εγώ Κατερίνα στο σχολείο την αναφέρω…
Η ερώτηση είναι καλή. Στην περίπτωση κατά την οποία σε μια ΧΙ ζητείται η μελέτη της επίδρασης δύο παραγόντων, το πρώτο είναι να μην ξεχάσουμε τον έναν από αυτούς. Στην περίπτωση που θέτεις Κατερίνα, ο ένας από τους δύο (το ευγενές αέριο) δεν έχει καμιά επίδραση αλλά ο άλλος (η μεταβολή του όγκου) μπορεί να έχει, ανάλογα με τη στοιχειομετρία των αερίων της αντίδρασης.
Παρόμοια περίπτωση είναι να προσθέσουμε σε διάλυμα οξέος ή βάσης, διάλυμα NaCl ή άλλου άλατος που τα ιόντα του δεν αντιδρούν πρακτικά με το νερό. Είναι πολύ συνηθισμένο όταν ένας μαθητής αντιμετωπίζει μια σχετική ερώτηση, να πει ότι το pH του διαλύματος δεν επηρεάζεται, παραβλέποντας τη μεταβολή του όγκου του διαλύματος!
Προσοχή λοιπόν όταν απαντάμε σε μια ερώτηση, να την έχουμε προηγουμένως μελετήσει καλά.
Εγώ θεωρώ ότι είναι εκτός ύλης η συγκεκριμένη ερώτηση γιατί ερμηνεύεται με βάση τις μερικές πιέσεις ή με βάση το Qc. Τους αναφέρω ότι στην περίπτωση αυτή μετατοπίζεται η Χ.Ι. αλλά δεν μπορούμε να το εξηγήσουμε. Εκτός αν σε μια άσκηση δίνεται κάποια πληροφορία για τη Ν.Χ.Ι. και μπορούμε να καταλάβουμε προς τα που μετατοπίστηκε η Χ.Ι.
Δεν συμφωνώ Άγγελε ότι χρειάζεται η αναφορά σε μερικές πιέσεις ή στην Qc, για την ερμηνεία της μη επίδρασης στη ΧΙ των ευγενών αερίων ή γενικά αερίων που δεν παίρνουν μέρος στην αντίδραση. Προσωπικά λέω στα παιδιά να γράψουν απλώς ότι η ΧΙ δεν επηρεάζεται αφού με την προσθήκη λχ Ne, οι συγκεντρώσεις των σωμάτων της ΧΙ δεν μεταβάλλονται, ούτε φυσικά ο όγκος του δοχείου ή η θερμοκρασία. Προφανώς αναφέρεσαι στην πιο «πονηρή» διατύπωση της ερώτησης, σύμφωνα με την οποία η πίεση στο δοχείο αυξάνεται με την προσθήκη του ευγενούς αερίου. Ούτε εκεί όμως νομίζω ότι υπάρχει πρόβλημα, αφού στο σχολικό βιβλίο συσχετίζεται από την αρχή η μεταβολή της πίεσης του μίγματος αποκλειστικά με μεταβολή του όγκου του δοχείου, ενώ ξεκαθαρίζεται (παράθεμα) ότι δεν παίζει ρόλο η μεταβολή της πίεσης όταν οφείλεται στην προσθήκη ευγενούς αερίου. Αυτό αφορά πχ πάρα πολλές αντιδράσεις οργανικής χημείας.
Γενικεύοντας πάντως θα έλεγα ότι το πρόβλημα της μη ικανοποιητικής ερμηνείας, αφορά ερωτήσεις του τύπου Σωστό/Λάθος με αιτιολόγηση. Αν κάποιο θέμα δεν είναι επαρκώς αιτιολογημένο στο σχολικό βιβλίο, η επιτροπή που βάζει τα θέματα μπορεί να το θέσει σε κλειστή ερώτηση, όπως τύπου Σωστό/Λάθος χωρίς αιτιολόγηση ή σε ερώτηση πολλαπλής επιλογής.
Ευχαριστώ για άλλη μια φορά.Κι εγώ την αναφέρω την περίπτωση προσθήκης ευγενούς αερίου υπό σταθερή πίεση απλά ερμηνεύω την μετατόπιση της θ.Χ.Ι προς τα περισσότερα mol αερίων με βάση τη μεταβολή των συγκεντρώσεων λόγω μεταβολής όγκου.
Είσαι λίγο ασαφής Κατερίνα. Τι ακριβώς ερμηνεύεις με βάση τη μεταβολή των συγκεντρώσεων;
Κατερίνα Μπόνια είπε:
Νίκος Παπαβασιλείου είπε:
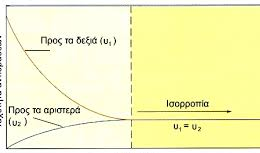
Εξηγώ πως οδηγείται ή θέση της Χ.Ι προς τα δεξιά όταν πρόσθετω ευγενες αέριο υπό σταθερή πίεση άρα μεταβλητο ογκο.Δηλαδη αναφέρω ότι αυξάνεται ο όγκος του δοχείου άρα μειώνονται οι συγκεντρώσεις των σωμάτων και ή θεση της Χ.Ι μετατοπίζεται προς τα περισσότερα molαεριων …αφού έχω αναφέρει ότι κανονικά πρέπει να δοθεί ή εξήγηση με τις μερικές πιέσεις αλλά είναι εκτος…..
Νίκο δεν αναφέρομε στην περίπτωση που προσθέτουμε αδρανές αέριο με σταθερό όγκο. Αυτό είναι εντός ύλης. Η περίπτωση που προσθέτουμε αδρανές αέριο με σταθερή πίεση είναι εκτός ύλης. Στην περίπτωση αυτή δεν μπορεί ο μαθητής να εξηγήσει τη μετατόπιση με τα εργαλέια που διαθέτει καθώς είναι εκτός ύλης οι μερικές πιέσεις και το Qc. Εκτός αν έχουμε κάποια πληροφορία για κάποια μεταβολή μεγέθους στην νέα χημική ισορροπία. Η καλύτερη εξήγηση πάντως είναι με το Qc που κακώς είναι εκτός ύλης.
Καλησπέρα συνάδελφοι. Πάντως ξαναλέω ότι μάλλον θα ήταν καλύτερα τα πράγματα αν λέγαμε ότι οι συντελεστές ισορροπίας είναι ουσιαστικά δύο: η θερμοκρασία και οι συγκεντρώσεις…
Σωστό Θοδωρή. Η πίεση ουσιαστικά μας «βολεύει» στην εξήγηση όταν αλλάζει ο όγκος. Ότι η Χ.Ι. μετατοπίζεται προς τα περισσότερα ή λογότερα mol αερίων. Ουσιαστικά παράγοντας είναι ο όγκος.
Ο όγκος είναι φυσικά ο άμεσος παράγοντας, δεν μπορούμε όμως να τον ταιριάξουμε με την αρχή του Le Chatelier, γι αυτό και αναφερόμαστε στην πίεση. Για να εξηγήσουμε εξ’ άλλου την επίδραση της μεταβολής της πίεσης, χρησιμοποιούμε εύκολα την καταστατική εξίσωση.
Νομίζω Νίκο ότι αν πούμε ότι συντελεστής ισορροπίας είναι η συγκέντρωση μπορούμε ωραιότατα να τον ταιριάξουμε με την αρχή Le Chatelier… Μιλάω γενικά, όχι μόνο για τη συγκεκριμένη εξεταστέα ύλη της Γ λυκείου. Κι έτσι θα μορούμε να εξηγήσουμε αβίαστα και το ότι όταν γίνεται αραίωση διαλύματος ασθενούς ηλεκτρολύτη η ιοντική ισορροπία μετατοπίζεται δεξιά.
Πως θα το ταιριάξουμε Θοδωρή;Με αύξηση του όγκου μειώνονται όλες οι συγκεντρώσεις. Ποιά είναι η αναίρεση που πρέπει να γίνει; Να αυξηθεί το άθροισμα των συγκεντρώσεων άρα προς τα περισσότερα mol αερίων; Έχει νόημα να το μούμε αυτό; Μπορούμε βέβαια να χρησιμοποιήσουμε το Qc. Η αναγωγή πάντως της μεταβολής του όγκου σε μεταβολή της πίεσης είναι αρκετά «βολική» οπότε ας την κρατήσουμε. Όσον αφορά την αραίωση του διαλύματος ασθενούς ηλεκτρολύτη χρησιμοποιώ Qc. Γενικά το Qc λύνει πολλά προβλήματα και θε έπρεπε να είναι εντός ύλης.
Για την αραίωση ασθενούς ηλεκτρολύτη και μετατόπιση της θέσης Ι.Ι προς τα δεξιά εγώ χρησιμοποιώ τον βαθμό ιοντισμού και τον τύπο που προκύπτει με απόδειξη από το νόμο αραίωσης του Οstwald.Ka=a2c.Δε’ιχνει οτι το α αυξάνεται άρα η θ .Ι.Ι μετατοπίστηκε προς τα δεξιά με την αραίωση.
Άγγελε και βέβαια έχει νόημα να το πούμε αυτό. Όταν χρησιμοποιείς το Qc ουσιαστικά το ίδιο κάνεις. Δείχνεις δηλαδή ότι με την αραίωση ελαττώνεται περισσότερο ο αριθμητής από τον παρανομαστή της Qc, δηλαδή οι δρώσες μάζες των προιόντων έναντι αυτών των αντιδρώντων. Αυτό που καθορίζει το τι θα γίνει είναι τα γινόμενα των δρωσών μαζών αντιδρώντων-προϊόντων. Δε μπορούμε να το διδάξουμε αυτό; Τόσο δύσκολο είναι; Κι έτσι θα απαλαχθούμε από το συντελεστή ισορροπίας «Πίεση» που κατά τη γνώμη μου το μόνο που «εξυπηρετεί» είναι να δημιουργεί παρανοήσεις… Παρ’όλο που τον αναφέρουν όλα τα βιβλία και δε μπορώ να καταλάβω γιατί…
Κατερίνα διαφωνώ με αυτήν την προσέγγιση. Η μεταβολή του βαθμού ιοντισμού δεν είναι κριτήριο για το που μετατοπίζεται η ισορροπία. Όταν κάνουμε συμπύκνωση δηλ. αυξάνουμε τη C του ασθενούς ηλεκτρολύτη ο βαθμός ιοντισμού ελαττώνεται αλλά η ισορροπία μετατοπίζεται δεξιά…
Δηλαδή την αραίωση και τη συμπύκνωση διαλύματος ασθενούς ηλεκτρολύτη οι μαθητές σε Πανελλήνιο επίπεδο μπορούν να χρησιμοποιούν το Qc για τους ίδιους φαντάζομαι…όμως αιτιολόγηση πώς θα γίνεται στο επίσημο γραπτό;;;;με τη συγκέντρωση……
Επίσης να ρώτήσω και κάτι άλλο αγαπητοί συνάδελφοι πότε τελειώνετε αυτή την ύλη περίπου;;;;;
Θοδωρή το Qc το συγκρίνεις με την Κc ώστε να καταλάβεις την κατεύθυνση αντίδρασης. Δεν διαφωνώ στην ουσία μαζί σου απλά σου λέω τι εξυπηρετεί η πίεση. Εξυπηρετεί την διατύπωση της Le chatelier. Ενώ με τον παράγοντα όγκο αλλάζουν όλες οι συγκετρώσεις οπότε με την Le chatelier νομίζω δεν μπορούμε να δώσουμε καλή εξήγηση χωρίς τη χρήση της πίεσης.Γενικά πάντως έχεις απόλυτο δίκιο ότι πρέπει να αναθεωρηθούν αρκετά πράγματα (όχι μονο στη Χ.Ι.) γιατί όπως λες πιο πολύ μπερδεύουν παρά λύνουν προβλήματα. Συμφωνώ επίσης ότι είναι λάθος η ταύτιση που υπάρχει για τον βαθμό ιοντισμού και τη μετατόπιση ισορροπίας. Κατερίνα εγώ την ύλη τη βγάζω περίπου τέλη φλεβάρη (φροντιστήριο).
Αν πούμε δηλαδή άγγελε ότι με την αύξηση του όγκου ελαττώνονται περισσότερο οι συγκεντρώσεις συνολικά των προϊόντων σε σχέση με αυτές των αντιδρώντων, υπάρχει κάποιο πρόβλημα με την αρχή Le Chatelier; Η ισορροπία θα τείνει να αναιρέσει τη μεταβολή, δηλαδή τη μεγαλύτερη συνολικά ελάττωση των συγκεντρώσεων των προϊόντων, άρα θα μετατοπιστεί δεξιά. Δεν εξηγείται πολύ ωραία με την αρχή Le Chatelier; Το ότι έχουμε ελάττωση συγκέντρωσης και στα αντιδρώντα θεωρώ ότι δεν είναι πρόβλημα. Απλά τείνει να αναιρεθεί η μεγαλύτερη ελάττωση…
Κατερίνα, ελπίζω σε πανελλαδικές να μη βάλλουν το ερώτημα «Που μετατοπίζεται η ισορροπία με την αραίωση». Θεωρώ ότι με βάση τη διάρθρωση της ύλης, ένα τέτοιο ερώτημα ΔΕΝ ΕΙΝΑΙ ΔΙΚΑΙΟ για τους μαθητές…
Τέλη Φλεβάρη…πολύ νωρίς μπράβο…νομίζω οτι πρέπει να βιαστώ!!Ευχαριστώ πολύ!!!
Προσωπικά συμφωνώ με την Κατερίνα ότι μπορούμε να χρησιμοποιούμε την τιμή ή τη μεταβολή του βαθμού ιοντισμού, για να εκφράσουμε πόσο προς τα δεξιά ή προς τα αριστερά μετατοπίζεται ή είναι μετατοπισμένη η ΧΙ. Έχει δίκιο βέβαια ο Θοδωρής όταν λέει ότι αυτή δεν είναι μια πολύ καλή ερώτηση, πάντως ένα ισχυρό οξύ έχει ισορροπία ιοντισμού μετατοπισμένη πολύ προς τα δεξιά, οπότε το α τείνει στο 1, ενώ σε ένα πολύ ασθενές οξύ η ισορροπία είναι μετατοπισμένη πολύ προς τα αριστερά και το α τείνει στο 0. Διαφωνώ τέλος Θοδωρή με το «όταν κάνουμε συμπύκνωση δηλ. αυξάνουμε τη C του ασθενούς ηλεκτρολύτη ο βαθμός ιοντισμού ελαττώνεται αλλά η ισορροπία μετατοπίζεται δεξιά». Αφού μειώνεται ο βαθμός ιοντισμού και τείνει ασυμπτωτικά στην τιμή 0, δεν μπορούμε να πούμε ότι η ισορροπία μετατοπίζεται προς τα δεξιά!
Νίκο, έχεις διάλυμα ασθενούς ΗΑ και προσθέτεις και άλλο ΗΑ, δηλαδή αυξάνεις τη C του ΗΑ. Με βάση την αρχή Le Chatelier, προς τα που μετατοπίζεται η ισορροπία; Νομίζω προς τα δεξιά…
Ναι, υπάρχει ένα πρόβλημα εδώ, γι αυτό συμφώνησα μαζί σου ότι δεν είναι καλό θέμα. Η συνεχής προσθήκη ΗΑ ελαττώνει συνέχεια το βαθμό ιοντισμού του οξέος, ο οποίος τείνει θεωρητικά στο 0, το οξύ δηλαδή τείνει να πάψει να ιοντίζεται. Ένα τέτοιο φαινόμενο δεν μπορούμε να το μελετήσουμε με όρους μετατόπισης της ιοντικής ισορροπίας, αφού αν χρησιμοποιήσουμε την αρχή του Le Chatelier, η ισορροπία φαίνεται μεν να μετατοπίζεται προς τα δεξιά αλλά βαθμιαία καταλήγουμε να μην έχουμε σχεδόν καθόλου αντίδραση του ηλεκτρολύτη με το νερό!
Ελπίζω κι εγώ να μη θέσουν την ερώτηση…