 (με αφορμή την 35 ερώτηση του ΠΜΔΧ 2018 για την Α Λυκείου
(με αφορμή την 35 ερώτηση του ΠΜΔΧ 2018 για την Α Λυκείου
- Oι προτάσεις που ακολουθούν αναφέρονται σε χημικές αντιδράσεις
ιι) Σε κάθε αντίδραση εξουδετέρωσης παράγεται H2O. )
Αν διατρέξει κανείς την παράγραφό 3.5 Χημικές αντιδράσεις του σχολικού εγχειριδίου της Χημείας Α Λυκείου θα βρει 7 τουλάχιστον αναφορές στην κατηγορία αντιδράσεων που ονομάζονται εξουδετερώσεις …
Στις τρεις από αυτές τις αναφορές φαίνεται ότι αντίδραση εξουδετέρωσης είναι ο σχηματισμός νερού από κατιόντα Υδρογόνου και ανιόντα Υδροξειδίου.
Στις υπόλοιπες φαίνεται ότι αντίδραση εξουδετέρωσης είναι κάθε αντίδραση μεταξύ βάσεως και οξέος ( μάλλον κατά Arrhenius αφού δεν γίνεται αναφορά σε άλλες θεωρίες).
Στην παράγραφο που αφιερώνεται ειδικά για την εξουδετέρωση γράφει και τα δυο και μάλιστα στο γαλάζιο περιθώριο τονίζει ότι στις αντιδράσεις εξουδετέρωσης ανήκουν και οι αντιδράσεις μεταξύ βασικού και όξινου οξειδίου προς σχηματισμό άλατος.
Στην συνέχεια αναφέρει εξαιρέσεις
Α) δεν παράγεται νερό όταν αντιδρά η Αμμωνία με το Θεϊκό οξύ προς Θειϊκό Αμμώνιο
Και
Β) δεν παράγεται νερό όταν αντιδρά τριοξείδιο του Θείου με οξείδιο του Σιδήρου (III) [στις εξισώσεις βέβαια που ακολουθούν φαίνεται πεντακάθαρα η παρενθεσούλα (aq) ]
>>>>>>>>>>
Τα ερωτήματα
- Είναι τελικά εξουδετέρωση μια αντίδραση μεταξύ οξέος και βάσης που δεν συνοδεύεται από εξουδετέρωση κατιόντων Υδρογόνου από ανιόντα Υδροξειδίου ; Και τι εννοούμε όταν λέμε ενθαλπία εξουδετέρωσης ;
- Η παραγωγή άλατος είναι το χαρακτηριστικό γνώριμα που καθορίζει αν μια αντίδραση είναι εξουδετέρωση ή μήπως η αντίδραση μεταξύ κατιόντων Υδρογόνου και ανιόντων Υδροξειδίου ;
- Όταν τα ιόντα που προκύπτουν από το ανιόν του οξέος και το κατιόν της βάσης είναι ευδιάλυτα και δεν σχηματίζουν κρύσταλλο άλατος τότε είναι αυτή αντίδραση εξουδετέρωσης ;
- Αντιδρά ένα οξείδιο με ένα άλλο οξείδιο σε στερεά μορφή ( π.χ. κρύσταλλος ή μήπως -όπως φαίνεται στο και βιβλίο- αποτελεί προϋπόθεση η ευκινησία των ιόντων που παράγονται μετά από την διάλυσή τους ;
- Οι εξαιρέσεις μη παραγωγής νερού σε αντιδράσεις οξέος βάσης διαπιστώνεται στη φύση ( κατά την πραγματοποίηση της αντίδρασης σε εργαστήριο ) ή την διαπιστώνουμε κατά την αναγραφή της εξίσωσης που περιγράφει τα φαινόμενα ; Τελικά αυτές οι εξαιρέσεις εντάσσονται στις εξουδετερώσεις ή όχι ;
- Ο όρος εξουδετέρωση συμπεριλαμβάνει και όλες τις αντιδράσεις μεταξύ βάσεων και οξέων κατά Bronsted-Lowry ή μήπως και κατά Lewis ;
![]()
Δημήτρη καλησπέρα. Έγραψα κάτι και θέλω να το ανεβάσω αλλά δε μπορώ γιατί είναι σε pdf. Πως να στο στείλω;
mltsosgk(at)gmail(dot)com
Καλησπέρα Μήτσο, καλησπέρα Θοδωρή.
Εν αναμονή της απάντησης του Θοδωρή, να δώσω μια αντίδραση:
CaO(s) +CO2(g)→CaCO3(s)
Δεν είναι “εξουδετέρωση” Μήτσο;
Η απάντηση του Θοθωρή εδώ
Καλησπέρα Θοδωρή , Καλησπέρα Διονύση
Θοδωρή δεν είναι προσωπικές απόψεις σου αυτό που έστειλες είναι ένα σχεδόν πλήρες σχεδίασμα των θεωριών που διαπραγματεύονται την μελέτη κάποιων χημικών αντιδράσεων.
Διονύση απαντώ πριν εκθέσω την άποψη μου για την διδακτική του θέματος γιατί θα μπορούσα έτσι να θέσω κι εγώ το ερώτημα.
Η αμφίδρομη αντίδραση Οξείδιο του ασβεστίου και διοξειδίου του άνθρακα προς ανθρακικό ασβέστιο δεν είναι αντίδραση εξουδετέρωσης ; Αν ναι σύμφωνα με ποιον ορισμό και με ποια θεωρία;
Διαβάζω για παράδειγμα στο σχολικό εγχειρίδιο . "Στις ποσοτικές αντιδράσεις διπλής αντικατάστασης εντάσσονται ως ειδική περίπτωση και οι αντιδράσεις εξουδετέρωσης αφού από κατιόντα υδρογόνου και ανιόντα υδροξειδίου παράγεται νερό που είναι ελάχιστα ιονιζόμενη ένωση" … Είναι η αντίδρασή σύνθεσης Ανθρακικού ασβεστίου ποσοτική ; παράγεται νερό ;
Η Γνώμη μου :
1. Ένας ορισμός πρέπει να είναι μονοσήμαντος . Αν ένας όρος ( όπως "εξουδετέρωση ) λαμβάνει διαφορετικές σημασίες στα πλαίσια διαφορετικών θεωριών τότε πρέπει να είμαστε σαφείς και προσεκτικοί δυο και τρεις φορές περισσότερο.
2. Δεν νομίζω πως είναι καλή ιδέα να διδάσκουμε στην Α Λυκείου και θεωρίες για οξέα και βάσεις εκτός υδατικών διαλυμάτων αλλά αν διδάσκουμε διαφορετικές θεωρίες οφείλουμε να διευκρινίζουμε την διαφορετική σημασία των όρων .
3. Στα πλάισια του βιβλίου της Α Λυκείου γίνεται σαφής αναφορά μόνο στη θεωρία Arrhenius και πρέπει να μείνουμε σε αυτήν.
4. Οι αντιδράσεις ανυδριτών ( και όταν αυτές επιτυγχάνονται ) δεν είναι ποσοτικές ούτε εξώθερμες σίγουρα . Δεν έχουν τα χαρακτηριστικά γνωρίσματα της εξουδετέρωσης κατά Arrhenius και δεν υπόκεινται στον κανόνα του Le Bartolle ( δεν ξέρω πως γράφεται ) για τις αντιδράσεις διπλής αντικατάστασης
Τέλος σημειώνω πως δεν θεωρώ λάθος το ερώτημα που ετέθη στον ΠΜΔΧ … Αλλά εξίσου σωστό θα ήταν και το ερώτημα : " Γιατί η πρότυπη γραμμομοριακή ενθαλπία εξουδετέρωσης έχει πάντα την ίδια τιμή" ; ( με στόχο να αξιολογηθεί η συσχέτιση με την αντίδραση κατιόντων Υδρογόνου +ανιόντων Υδροξειδίου )
Και προβληματίζομαι ως προς τον καλό σχεδιασμό της διδακτικής μας ως προς το σημείο αυτό…
Καλησπέρα Μήτσο, καλησπέρα Θοδωρή.
Θεωρώ ότι το κείμενο του Θοδωρή είναι άκρως διαφωτιστικό.
Όμως, από διδακτικής άποψης με βρίσκουν σύμφωνες και οι δικές σου αντιρρήσεις Μήτσο.
Ίσως στην Α΄Λυκείου θα έπρεπε να περιοριστούμε αυστηρά σε αντιδράσεις σύμφωνα με τη θεωρία Arrhenius….
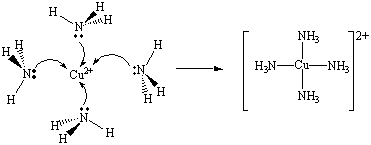
Στην πολύ όμορφη απάντηση σου Θοδωρή να προσθέσουμε και μια άλλη αντίδραση εξουδετέρωσης, οξέος (Cu+2) και βάσης (NH3) για τη δημιουργία συμπλόκου χαλκού ( σύνδεση Γ Λυκείου).