![]() Δημοσιεύτηκε από το χρήστη Αντώνης Μπαλτζόπουλος στις 20 Απρίλιος 2016 στις 17:11 στην ομάδα Χημεία Γ΄Λυκείου
Δημοσιεύτηκε από το χρήστη Αντώνης Μπαλτζόπουλος στις 20 Απρίλιος 2016 στις 17:11 στην ομάδα Χημεία Γ΄Λυκείου
Πολυ συχνά βλεπουμε σε βοηθήματα να παρουσιάζονται τα 3 στάδια ( όπως παρουσιάζονται στο σχολικό βιβλίο ) της αλογονοφορμικής ως ανεξάρτητες εφικτές αντιδράσεις .
Το σχολικό βιβλίο παρουσιάζει την αντίδραση ώς αντίδραση 3 βημάτων/σταδίων :
![]()
Στην πραγματτικότητα η αντίδραση είναι μια αντίδραση πολύ περισσότερων σταδίων και είναι καθαρά θέμα της πηγής το βάθος της αναλυση με την οποία θα παρουσιαστεί .
Στην wikipedia ( https://en.wikipedia.org/wiki/Haloform_reaction ) παρουσιάζεται πολύ πιο αναλυτικά .
“… In the first step, the halogen disproportionates in the presence of hydroxide to give the halide and hypohalite (example with bromine, but reaction is the same in case of chlorine and iodine; one should only substitute Br for Cl or I):

![]()
If a methyl ketone is present, it reacts with the hypohalite in a three-step process:
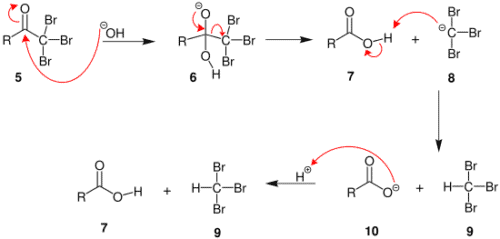
- (1) Under basic conditions, the ketone undergoes keto-enol tautomerization. The enolate undergoes electrophilic attack by the hypohalite (containing a halogen with a formal +1 charge).
- (2) When the α position has been exhaustively halogenated, the molecule undergoes a nucleophilic acyl substitution by hydroxide, with −CX3 being the leaving group stabilized by three electron-withdrawing groups. In the third step the −CX3 anion abstracts a proton from either the solvent or the carboxylic acid formed in the previous step, and forms the haloform. At least in some cases (chloral hydrate) the reaction may stop and the intermediate product isolated if conditions are acidic and hypohalite is used.
-
Στην ίδια σελίδα παρουσιάζεται και ένα animation ( Σχεδιοκίνηση ) του μηχανισμού :Διαβάζοντας και άλλα site ( ιστοσελίδες ) φαίνεται μια ομοφωνία ώς πρός τον μηχανισμό :Το πιο σημαντικό όμως ( ή τουλάχιστον αυτό που εκτιμώ ότι θα μπορούσε να ενδιαφέρει εμάς ) είναι ότι τα στάδια της οξείδωσης δεν πραγματοποιούνται από το αλογόνο Χ2 αλλά από το υποαλογονώδες ιόν ΧΟ- όπως αυτό προκύπτει από την αντίδραση του Χ2 + ΝaOHΣτην σελίδα του wikipedia αυτό φαίνεται στην έναρξη της περιγραφής του μηχανισμού ,
“…. In the first step, the halogen disproportionates in the presence of hydroxide to give the halide and hypohalite (example with bromine, but reaction is the same in case of chlorine and iodine; one should only substitute Br for Cl or I):
 …”Ενώ στο http://www.chemgapedia.de/ γίνεται παρουσίαση των 3 σταδίων ( κατά συμπτωση τα ίδια με αυτά του σχολικού βιβλίου ) με την χρησιμοποίηαη του Χ2 + NaOH ως αντιδρώντων ( και όχι σκέτου του Χ2 )Στην εργασία των Reynold C. Fuson, and Benton A. Bull με τίτλο “The Haloform Reaction” ( η αλογονοφορμική αντίδραση ) σημειώνεται
…”Ενώ στο http://www.chemgapedia.de/ γίνεται παρουσίαση των 3 σταδίων ( κατά συμπτωση τα ίδια με αυτά του σχολικού βιβλίου ) με την χρησιμοποίηαη του Χ2 + NaOH ως αντιδρώντων ( και όχι σκέτου του Χ2 )Στην εργασία των Reynold C. Fuson, and Benton A. Bull με τίτλο “The Haloform Reaction” ( η αλογονοφορμική αντίδραση ) σημειώνεται Απομονώνοντας την έκφραση “…ΜΟΧ represents a hypohalite…” δηλ το ΜΟΧ αντιπροσωπεύει έναν υποαλογονίδιο ( δική μου η μετάφραση του τελευταίου όρου ) καταλαβάινουμε ότι το Χ2 ουδέποτε δρά ως ανεξάρτητο αντιδρών .
Απομονώνοντας την έκφραση “…ΜΟΧ represents a hypohalite…” δηλ το ΜΟΧ αντιπροσωπεύει έναν υποαλογονίδιο ( δική μου η μετάφραση του τελευταίου όρου ) καταλαβάινουμε ότι το Χ2 ουδέποτε δρά ως ανεξάρτητο αντιδρών .
Ολόκληρη η εργασία των Reynold C. Fuson, and Benton A. Bull για την αλογονοφορμική αντίδραση είναι στο επισυναπτόμενο #1Αλλά και οι Morrison & Boyd ( ακόμα και ) στην ελληνική 4η έκδοση της Οργανικής Χημείας τους γράφουν Δηλαδή ορίζουν ως αντιδρών σύστημα αυτό του Ιωδίου και του καυστικού νατίου δηλάδη του προιόντος τους ΝaOJ δηλαδή του ιόντος OJ-
Δηλαδή ορίζουν ως αντιδρών σύστημα αυτό του Ιωδίου και του καυστικού νατίου δηλάδη του προιόντος τους ΝaOJ δηλαδή του ιόντος OJ-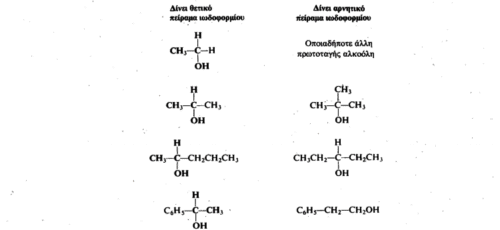 Και βέβαια η παρουσίαση των 3 σταδίων ( όπως του σχολικού βιβλίου και εδώ ) γίνεται με το NaOI. Αξία επίσης έχει και το “διδακτικο” σπάσιμο της περιγραφης της αντίδραση από τους Morrison & Boyd σε 1ο και 2ο στάδιο να δείξουν ότι το ίδιο αντιδραστήριο (NaOI ) κάνει και υποκατάσταση .
Και βέβαια η παρουσίαση των 3 σταδίων ( όπως του σχολικού βιβλίου και εδώ ) γίνεται με το NaOI. Αξία επίσης έχει και το “διδακτικο” σπάσιμο της περιγραφης της αντίδραση από τους Morrison & Boyd σε 1ο και 2ο στάδιο να δείξουν ότι το ίδιο αντιδραστήριο (NaOI ) κάνει και υποκατάσταση . Για τις μέθυλο κετόνες οι ίδιοι γραφούν :
Για τις μέθυλο κετόνες οι ίδιοι γραφούν :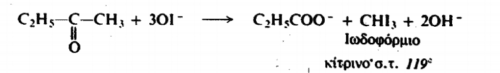 Το απόσπασμα από βιβλίο των Morrison & Boyd ειναι διαθέσιμο εδώ ή στο επισυναπτόμενο #2ΥΓ … στον Πολυνίκη , στον Χρήστο , στον Βασίλη , στον Κώστα , στον Θοδωρή , στον Τάσο , στον Αντώνη , στο Θρασύβουλο , στην Βιβή , στον Ερρίκο , στον Ηλία στον Δημήτρη στον Δημητρη στον Γιαννη και στον Παύλο .ΥΓ … σε όλους εμάς που διδάσκαμε τόσα χρόνια ότι το HCOOH δεν οξειδώνεται από FehlingΥΓ … Ακόμα με στοιχειώνει η κουβέντα της μαθητριας του Νίκου που του είπε πως ο καλύτερος Χημικός είναι εκείνος που διδάσκει καλύτερα ενα συγκεκριμένο βοήθημα . Είναι φανερό ότι δεν θα γίνω ποτέ ο καλύτερος Χημικός
Το απόσπασμα από βιβλίο των Morrison & Boyd ειναι διαθέσιμο εδώ ή στο επισυναπτόμενο #2ΥΓ … στον Πολυνίκη , στον Χρήστο , στον Βασίλη , στον Κώστα , στον Θοδωρή , στον Τάσο , στον Αντώνη , στο Θρασύβουλο , στην Βιβή , στον Ερρίκο , στον Ηλία στον Δημήτρη στον Δημητρη στον Γιαννη και στον Παύλο .ΥΓ … σε όλους εμάς που διδάσκαμε τόσα χρόνια ότι το HCOOH δεν οξειδώνεται από FehlingΥΓ … Ακόμα με στοιχειώνει η κουβέντα της μαθητριας του Νίκου που του είπε πως ο καλύτερος Χημικός είναι εκείνος που διδάσκει καλύτερα ενα συγκεκριμένο βοήθημα . Είναι φανερό ότι δεν θα γίνω ποτέ ο καλύτερος Χημικός
- Συνημμένα:
![]()
Aντωνη, καλησπερα. Στο παλιο σχολικο βιβλιο (2000) των Μανουσακη-Κεφαλλωνιτη – Χρηστιδη , που απεσυρθη μετα απο ενα χρονο η αντιδραση δινεται ως εξης: