-
H/o Πέτρος Μάλλιος έγραψε ένα νέο άρθρο πριν από 8 έτη, 5 μήνες
Το παρακάτω διάγραμμα αναφέρεται στην αυτοκατάλυση και βρίσκεται στη σελίδα 80 του σχολικού βιβλίου. Η ερώτησή μου είναι η εξής:
Δε θα έπρεπε η πράσινη καμπύλη να ελαχιστοποιείται σε διαφορετική χρονική στιγμ […]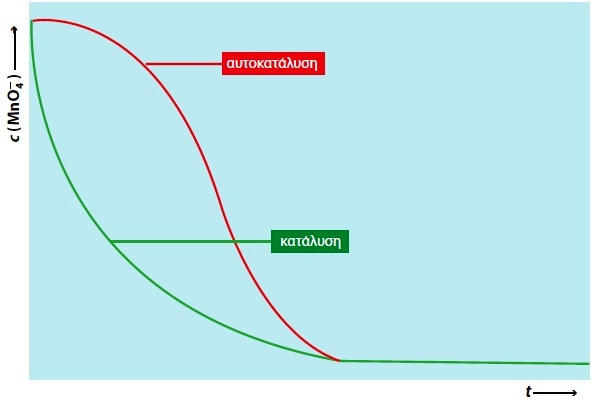
-
Ο/η Πέτρος Μάλλιος σχολίασε το άρθρο Μεγάλες αλλαγές στις πανελλαδικές εξετάσεις… πριν από 8 έτη, 7 μήνες
Στα παραδείγματα που ανέφερα (Χημικός, Μηχανικός Υπολογιστών) εννοείται ότι και οι δύο πρέπει να δώσουν και Φυσική και Μαθηματικά.
Στις τελευταίες σου ερωτήσεις απάντησα ήδη. Το κάθε τμήμα είναι αρμοδιότερο όλων να γνωρίζει για το ποιες γνώσεις πρέπει να είναι εφοδιασμένοι οι φοιτητές τους.
Γιατί εγώ θα λέω Χημεί&alph…[Περισσότερα]
-
Ο/η Πέτρος Μάλλιος σχολίασε το άρθρο Μεγάλες αλλαγές στις πανελλαδικές εξετάσεις… πριν από 8 έτη, 7 μήνες
Πιστεύω ότι το 6ωρο «μάθημα» Χημεία/Βιολογία θα είναι 3 ώρες Χημεία και 3 ώρες Βιολογία και θα το κάνουν 2 εκπαιδευτικοί.
Ποια μαθήματα πρέπει να δώσει ένας μαθητής πρέπει να το αποφασίζει το εκάστοτε τμήμα ΑΕΙ ή ΑΤΕΙ.
Θέλεις Χημικό; Θα εξεταστείς στη Χημεία.
Θέλεις Μηχανικός Υπολογιστών; Θα εξεταστείς στην Πληρ&omicro…[Περισσότερα]
-
H/o Πέτρος Μάλλιος έγραψε ένα νέο άρθρο πριν από 8 έτη, 7 μήνες
didaktea_yli_g_taxis_gel
Με μια πρώτη ματιά στην ύλη της Χημείας εντοπίζω τρεις αλλαγές.
Εντός η παράγραφος 3.2 «Παράγοντες που επηρεάζουν την ταχύτητα αντίδρασης. Καταλύτες»
Εκτός η εισαγωγή στο κεφ […] -
Ο/η Πέτρος Μάλλιος σχολίασε το άρθρο Σχόλια για τα θέματα Χημείας 2017. πριν από 8 έτη, 10 μήνες
Πόσο εύκολα κάνουμε κριτική για θέματα που έβαλαν συνάδελφοι Χημικοί…
Ξέρετε κάποια χρονιά που δεν έχουν σχολιαστεί αρνητικά τα θέματα; Εγώ όχι.
Ξέρετε πόσες ημέρες έχουν στη διάθεσή τους αυτοί οι άνθρωποι; Μόνο λίγες ημέρες…
Έχετε αναρωτηθεί αν μπορείτε να βάλετε εσείς αψεγά&de…[Περισσότερα] -
Ο/Η Πέτρος Μάλλιος άλλαξε φωτογραφία προφίλ πριν από 8 έτη, 10 μήνες
-
Πέτρος Μάλλιος συμμετέχει στην ομάδα Το στέκι μας πριν από 9 έτη
-
Ο/η Πέτρος Μάλλιος σχολίασε το άρθρο Διδακτική απορία στην ύλη της Ά Λυκείου. πριν από 9 έτη
Απορία ενός Χημικού που διδάσκει Φυσική στην Α' Λυκείου:
Πρέπει να κάνω κι εγώ ασκήσεις στο σχολείο με τροχαλία όταν αυτή είναι εκτός ύλη&… -
Ο/η Διονύσης Μάργαρης και ο/η
 Πέτρος Μάλλιος είναι πλέον φίλοι πριν από 9 έτη, 5 μήνες
Πέτρος Μάλλιος είναι πλέον φίλοι πριν από 9 έτη, 5 μήνες -
Πέτρος Μάλλιος εγγράφηκε πριν από 9 έτη, 5 μήνες
Καλησπέρα Πέτρο.
Μιας και δεν βλέπω κάποια απάντηση από φίλο Χημικό, ας καταθέσω εγώ κάποιες σκέψεις (ως φυσικός…).
Έστω η συγκέντρωση του αντιδρώντος παίρνει την τιμή C1, όπως στο σχήμα.
Παρουσία καταλύτη αυτό συμβαίνει τη χρονική στιγμή t1, ενώ στην περίπτωση της αυτοκατάλυσης, πολύ αργότερα τη στιγμή t2. Αν πάρουμε τις δυο κλίσης -dC/dt βρίσκουμε τις εφαπτόμενες των γωνιών α και φ, όπου με βάση το σχήμα εφφ>εφα, πράγμα που σημαίνει ότι η 2η καμπύλη έχει μεγαλύτερη κλίση και κατά συνέπεια η αντίδραση με αυτοκατάλυση έχει μεγαλύτερη ταχύτητα αντίδρασης και σε πολύ λιγότερο χρονικό διάστημα Δt=t3-t2 το αντιδρόν θα αποκτήσει την κοινή συγκέντρωση C2, σε σύγκριση με το χρονικό διάστημα Δt΄= t3-t1 που θα χρειαστεί η αντίδραση με τον καταλύτη.
Το θέμα είναι ποια είναι η «κοινή» συγκέντρωση C2; Είναι η τελική συγκέντρωση, όταν σταματά η αντίδραση ή είναι μια πριν μηδενιστούν οι δυο ταχύτητες;
Αν με τη συγκέντρωση C2 οι αντιδράσεις συνεχίζονται (πράγμα που θεωρώ πιθανότερο, αφού τη στιγμή t3 και οι δυο καμπύλες έχουν μη μηδενικές κλίσεις), θα έπρεπε να συνεχιζόταν και η κόκκινη (την έχω προσθέσει) και η πράσινη να μην είναι οριζόντια, από εκεί και πέρα, έστω για ελάχιστο χρόνο.
Αν θεωρεί το βιβλίο ότι τη στιγμή t3 όπου οι δυο συγκεντρώσεις εξισώνονται, είναι και η στιγμή που τελειώνει η αντίδραση είτε επειδή C2=0 είτε για άλλο λόγο (τέλειωσε το άλλο αντιδρόν, αν έχουμε για παράδειγμα την αντίδραση Α +Β → Γ, όπου το Α είναι σε περίσσεια), τότε μάλλον είναι …σχεδιαστική αδεία αυτή η σύμπτωση.
Και όταν λέω …σχεδιαστική αδεία εννοώ, ότι θεωρητικά η αντίδραση τελειώνει σε άπειρο χρόνο, οπότε αυτή η στιγμή t3 μπορούμε να θεωρήσουμε ότι, με μαθηματική λογική, τείνει στο άπειρο, οπότε λίγο νωρίτερα, λίγο αργότερα, δεν έχει νόημα…
Κ. Μάργαρη, ευχαριστώ για την απάντηση.
Αναφέρετε ότι το πιθανότερο είναι τη χρονική στιγμή t3 και οι δύο καμπύλες έχουν μη μηδενικές κλίσεις.
Για την κόκκινη καμπύλη να το δεχτώ.
Για την πράσινη, όμως, φαίνεται ξεκάθαρα ότι η συγκέντρωση σταθεροποιείται στην ελάχιστη τιμή (ίσως και να μηδενίζεται) οπότε η αντίδραση ολοκληρώνεται.
Τη σχεδιαστική αδεία δεν μπορώ να την δεχτώ γιατί δημιουργεί παρερμηνείες.
Περιμένω τα σχόλια κυρίως των παλαιότερων συναδέλφων που έχουν διδάξει επί σειρά ετών το μάθημα στη Β' Λυκείου Θετικής Κατεύθυνσης.
Καλησπέρα. Πέτρο θα συμφωνήσω με την άποψή σου. Αφού στην κατάλυση ο καταλύτης (Mn2+) υπάρχει από την αρχή ενώ στην αυτοκατάλυση σχηματίζεται μετέπειτα, μου φαίνεται λογικό να ολοκληρώνεται πιο γρήγορα η αντίδραση στην κατάλυση…
Καλημέρα Πέτρο, καλημέρα Θοδωρή.
Βλέποντας το διάγραμμα χθες το βραδάκι και τις διαφορετικές κλίσεις, το μυαλό μου “κόλλησε” σε διαφορετικές ταχύτητες, ωσάν να είχαμε άλλο (εξωτερικό) καταλύτη και άλλο “αυτοκαταλύτη”, οπότε πήγα στις διαφορετικές ταχύτητες για την συγκέντρωση C1 . Μόλις τώρα είδα ότι αναφερόμαστε στα ιόντα του δισθενούς Μαγγανίου, οπότε όλα αυτά είναι άκυρα…
Άλλωστε ότι βγαίνουν διαφορετικές οι κλίσεις επιβεβαιώνει από άλλη πλευρά ότι το διάγραμμα είναι λάθος.
Οπότε πείτε ότι δεν υπάρχει το πρώτο μου σχόλιο…
Συμφωνώ λοιπόν ότι η αντίδραση τη δεύτερη φορά θα ολοκληρωθεί αργότερα…