 Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
-
Aυτό που λες ισχύει στην περίπτωση που δεν λάβεις καθόλου τα ιοντα από τον ιοντισμό του οξικού οξέος. Δηλαδή θεωρείς ότι το ασθενές δεν παίζει κανένα ρόλο.Μπορείς να κάνεις την προσέγγιση;Φιλικά.
Αντωνης Μπαλτζοπουλος είπε:
Όμως , Η συγκέντρωση των ιόντων Η3Ο που προέρχονται από το CH3COOH μετά από την προσθήκη του δ/τος HCl δεν προκύπτει από τυπους αραίιωσης.Η απάντηση που υιοθετώ ειναι αυτή του κ. Παπαδάκη μιας που τελικα [Η3Ο]= χ’ + C2′ όπου C2 είναι η νέα συγκετρωση που θα αποκτήσει το δ/μα HCL .
Όσο η αραίωση ειναι σε επίπεδα που μας επιτρέπει να πούμε [Η3Ο]= χ’ + C2′ = C2′ τότε η μελέτη του C2′ = 10^-3*V2 / V1 + V2 μας οδηγεί σε μείωση της συγκέντρωσης των οξωνίων άρα αύξηση του pH.
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
…. η συνεισφορά του CH3COOH στα Η3Ο ειναι μικρότερη παρουσία του HCl από όταν ήταν μόνο του. Τόσο μικρότερη δε που δεν μπορεί να αναπληρώθεί από την προσφορά σε Η3Ο από το ισχυρο HCl. Αυτό γίνεται γιατί η συγκέντρωση του HCl ειναι 0,001 .Εάν η συγκέντρωση του HCl ηταν 0,01 τότε η άσκηση θα ηταν άλυτη ( η απάντηση θα ηταν ότι όσο η αραίωση δεν ρίχνει την συγκέντρωση του HCl κάτω από το 0,001 θα έχουμε μείωση pH ενώ εάν η η αραίωση δώσει τιμή κάτω από 0,001 θα αυξηθεί το pH )
υγ … την προσέγγιση την κάνω ( γίνονταν ήδη στο αρχικό διάλυμα ενώ τώρα επιπροσθέτως έχουμε και ΕΚΙ ). Θεωρώ την συγκέντρωση που θα πάρει το HCl , κυρίαρχη ( με 1/10 φτάνει στο 0,0001 ).
Σε αυτά που γραφω βασίζομαι κυριώς βασίζομαι στό ότι το CH3COOH δεν μπορεί να αναπληρώσει τα H3O που του περιορίζει το HCl (… τείνει να αναιρέσει την επιφερόμενη αλλαγή ..)
 Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
-
Υπάρχει όμως και η αραίωση που οδηγεί την ισορροπία δεξιά.Αντωνης Μπαλτζοπουλος είπε:
…. η συνεισφορά του CH3COOH στα Η3Ο ειναι μικρότερη παρουσία του HCl από όταν ήταν μόνο του. Τόσο μικρότερη δε που δεν μπορεί να αναπληρώθεί από την προσφορά σε Η3Ο από το ισχυρο HCl. Αυτό γίνεται γιατί η συγκέντρωση του HCl ειναι 0,001 .Εάν η συγκέντρωση του HCl ηταν 0,01 τότε η άσκηση θα ηταν άλυτη ( η απάντηση θα ηταν ότι όσο η αραίωση δεν ρίχνει την συγκέντρωση του HCl κάτω από το 0,001 θα έχουμε μείωση pH ενώ εάν η η αραίωση δώσει τιμή κάτω από 0,001 θα αυξηθεί το pH )
υγ … την προσέγγιση την κάνω ( γίνονταν ήδη στο αρχικό διάλυμα ενώ τώρα επιπροσθέτως έχουμε και ΕΚΙ ). Θεωρώ την συγκέντρωση που θα πάρει το HCl , κυρίαρχη ( με 1/10 φτάνει στο 0,0001 ).
Σε αυτά που γραφω βασίζομαι κυριώς βασίζομαι στό ότι το CH3COOH δεν μπορεί να αναπληρώσει τα H3O που του περιορίζει το HCl (… τείνει να αναιρέσει την επιφερόμενη αλλαγή ..)
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
… υπάρχει η αραίωση που μετατοπίζει την ιοντική ισορροπία προς τα δεξιά και η ΕΚΙ στα Η3Ο που μετατοπίζει την ιοντική προς τα αριστερά. ( αντικρουόμενοι παράγοντες )Και εδώ έρχεται το πολύ έξυπνο παράδειγμα του κ. Χριστάκου και του κ. Παπαδακη. Εάν υπερίσχυε ο παράγοντας της αραίωσης θα είχαμε αυξηση ph … ενώ στην καλύτερη περίπτωση για το HCl θα μπορούσε να΄δώσει ph=3
 Απάντηση από τον/την Διονύσης Μάργαρης στις
Απάντηση από τον/την Διονύσης Μάργαρης στις
-
Αχ βρε Νίκο τι μας κάνεις να ψάχνουμε μεσ’ τα μεσάνυχτα. Και βλέπει τα καμώματα η μέρα και γελά!!!
Λοιπόν έχουμε και λέμε:
[Η3Ο+]= χ+C2
όπου C2 η συγκέντρωση του υδροχλωρικού οξέος στο αραιωμένο διάλυμα και από την ισορροπία του οξικού οξέος, αν χ η συγκέντρωση των παραγομένων οξονίων, λόγω επίδρασης κοινού ιόντος παίρνουμε:
Κα= χ.(χ+C2)/(c1-x) = χ.(χ+C2)/c1
όπου C1 η αραιωμένη συγκέντρωση του οξικού.
Και τι προκύπτει;
ότι ανεξάρτητα των όγκων το pH μένει πάντα σταθερό και ίσο με 3.
Για να βεβαιωθείτε δείτε το αρχείο Excell που επισυνάπτω, και βάλτε τιμές ΜΟΝΟ στα κίτρινα κελιά για τους όγκους των δύο διαλυμάτων
το pH είναι πάντα 3. - Συνημμένα:
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
…. μπορείς σε παρακαλώ να κανεις ενα excel χωρίς να κάνεις την προσσεγγιση του c1-x = c1( εχω θέσει το πρόβλημα ανάποδα …. με ποια αναλογία όγκων πρέπει να αναμιξω τα διαλύματα CH3COOH 0.1M και HCL 0.1 M …ώστε να προκύψει διάλυμα με ph = 3 )
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
…. to excell χωρις την προσέγγιση ( με καποιες επιφυλάξεις αλλά τα αποτελέσματα συμφωνουν με αυτά που βρηκα με το χερι )( την ανάλυση του pH στο 5 δεκαδικο την κάνω για να καταρίψω το «για κάθε όγκο» … )
- Συνημμένα:
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
Πηγή προβληματισμού μου είναι η παρακάτω σκέψη του συναδέλφου κ. Ελευθερίου….Αν ανακατέψω νερό 10C με άλλη ποσότητα νερού 10C η τελική θερμοκρασία δεν θα είναι πάλι 10C;Aν ανακατέψω διαλύμα με ΡΗ=3 με άλλο διάλυμα με ΡΗ=3 δεν θα βγει πάλι ΡΗ=3; ….
… εκτιμώ τελικά ότι η απάντηση βρίσκεται στην μελέτη αυτής της πρότασης του κ. Ελευθερίου.
Στην άσκηση που έχει θέσει ο κ. Καρχιμάνης εάν λυθεί με τον τρόπο που προτείνει ο κ. Μαργαρης ( που μεταξύ μας μόνο έτσι μπορεί να λυθεί ) το pH παραμένει σταθερό.
Μπορεί αυτό να ερμηνευτεί χημικά ?
Θα πρέπει να δεχθούμε (?) ότι …
…ή ότι η αραίωση ( που οδηγεί την ιοντική ισορροπία δεξιά ) αναιρείται πλήρως ( και ακριβώς ) από την ΕΚΙ στα Η3Ο που οδηγεί την ιοντική ισορροπία αριστερά
… ή ότι το διάλυμα CH3COOH αναιρεί πλήρως τις ( πολλες ) επιφερόμενες αλλαγές και επιστρέφει στην αρχική τιμή του πε-χα.
Μόνο εάν λυθεί η άσκηση «στεγνά υπολογιστικά χωρίς προσεγγίσεις» φαίνεται η διαφοροποίηση ( σχολιάζω μόνος μου «… στο 4ο δεκαδικό του πε-χα … ? »)
Λοιπον ?
Ξαναγυρνώ στην πρόταση του κ. Ελευθερίου. ,«Aν ανακατέψω διαλύμα με ΡΗ=3 με άλλο διάλυμα με ΡΗ=3 δεν θα βγει πάλι ΡΗ=3; ….»
Τι λέτε για αυτό συνάδελφοι ?
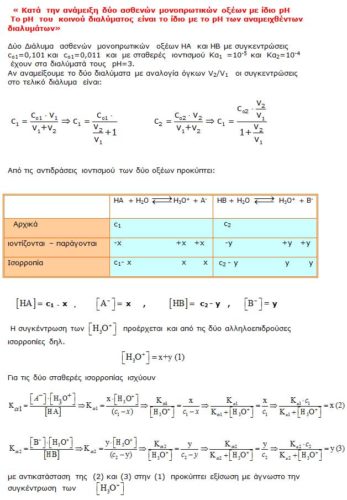
Δ1: Δ/μα ασθενούς ΗΑ με 0,1 Μ και Κα=10^-5 ( πεχα = 3 )
Δ2: δ/μα ασθενούς ΗΒ με 0,01 Μ και Κα’=10^-4 ( πεχα = 3 )Ποιο θα είναι το πε-χα του διαλύματος που θα προκύψει από την ανάμιξή τους ?
( εγω δοκίμασα με συγκεκριμένες αναλογίες 1-1 … 1-9 … και 9-1 γιατί ήθελα να μελετήσω και τον βαθμό ιοντισμού των οξέων στο τελικό διάλυμα )
Εάν κάνουμε την προσέγγιση στους παρονομαστές των επιμέρους Κ ( δηλ στο C1’-x = C1’ και C2’-y = C2’ ) η απάντηση είναι πάλι …3.
( εδώ μερικά (α) βγαίνουν της τάξης του 10% που είναι ένα θέμα που χτυπά καμπανάκι για την προσέγγιση – αλλά οφείλω να πω πως χωρίς την προσέγγιση δεν έχω την υπομονή να λύσω την άσκηση – )Πως ερμηνεύεται αυτό από την θεωρία της ιοντικής ισορροπίας ?
Ερχόμαστε σε αντιθεση με βασική αρχή των χημικών ισορροπιών ( αποκλείεται ) ?
Είμαστε στην περίπτωση που οι αντικρουόμενοι παράγοντες αναιρούν πλήρως ο ένας τον άλλον ( όπως σε κάτι περιπτώσεις χημικής ισορροπίας όπου χρησιμοποιούσαμε το Qc για να δούμε ποιος παράγοντας υπερισχύει και όταν βρίσκαμε Qc-=Kc λέγαμε ότι ΔΕΝ μετατοπίζεται η χημική ισορροπία ) …. ?
Είναι η μεταβολή στο πε-χα επιπέδου 4ου ή 5ου δεκαδικού ψηφίου και στην προσπάθεια μας να λύσουμε την άσκηση την ακυρώνουμε μέσω των προσεγγίσεων μας ?
Ή μήπως δεν είναι δυνατόν με πρώτες ύλες που έχουν το ίδιο χαρακτηριστικό ( pH=3) να καταλήξουμε σε ένα τελικό προιόν με διαφορετική τιμή ως προς αυτό το χαρακτηριστικό ( δηλ pH διαφορετικό του 3 ) ?
Σας ευχαριστώ προκαταβολικά .
 Απάντηση από τον/την Διονύσης Μάργαρης στις
Απάντηση από τον/την Διονύσης Μάργαρης στις
-

Συμφωνείτε συνάδελφοι;
Έκανα τις γνωστές προσεγγίσεις. Ισχύουν; Νομίζω ναι. Οι συγκεντρώσεις των ιόντων Α και Β είναι πολύ μικρότερες από τις συγκεντρώσεις των οξέων στο διάλυμα που προκύπτει από την ανάμειξη.
Δείτε το επισυναπτόμενο αρχείο Excell και βάλτε τιμές για τους όγκους των δύο διαλυμάτων, μόνο στα κελιά με το κίτρινο χρώμα. Το pH είναι πάντα 3!!!
Το παράδειγμα όμως που χρησιμοποίησε ο Χρήστος δεν με ικανοποιεί. Εκεί πίσω από την απάντηση κρύβεται ο πρώτος Θερμοδυναμικός νόμος. Εδώ τι συμβαίνει;
Οι εξισώσεις και οι προσεγγίσεις μας κάνουν παιχνίδι; Εντάξει αν το ένα έχει μεγάλο όγκο, επιβάλει την «παρουσία του», αλλά τόσο πολύ;
Θα ήθελα, πέρα από τις εξισώσεις μια ερμηνεία… - Συνημμένα:
Απάντηση από τον/την Παπαδάκης Γιάννης στις
-
Το αρχικό ερώτημα αφορούσε ανάμιξη ενός ισχυρού και ενός ασθενούς οξέος με Ph=3 και τα δύο.
Επιμένω, ότι το αποτέλεσμα της ανάμιξης, όταν ο όγκος του ασθενούς είναι πολύ μεγαλύτερος από τον όγκο του ισχυρού, το Ph που θα προκύψει θα είναι μεγαλύτερο από 3.
Δείτε το επισυναπτόμενο αρχείο. - Συνημμένα:
 Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
-
Γιατί ένα διάλυμα 99 λίτρων με ΡΗ=3 να επηρεαστεί από ένα διάλυμα 1 λιτρου με PH=3 και να γίνει ΡΗ=3,32 μήπως οι προσεγγίσεις που κάνεις είναι πολύ χονδρές…..(0,09999999999).Τόσο εύκολα μπορούμε να αλλάζουμε το ΡΗ ενός μεγάλου σε όγκου διαλύματος;Παπαδάκης Γιάννης είπε:
Το αρχικό ερώτημα αφορούσε ανάμιξη ενός ισχυρού και ενός ασθενούς οξέος με Ph=3 και τα δύο.
.
Απάντηση από τον/την Παπαδάκης Γιάννης στις
-
Χρήστο,οπως θα είδες δεν έκανα καμμία απολύτως προσέγγιση.
Επίσης, η αναλογία έxει σημασία. Το ίδιο συμβαίνει αν αντι για 1L – 99L, χρησιμοποιείσης 1 mL – 99mL.
ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ είπε:
Γιατί ένα διάλυμα 99 λίτρων με ΡΗ=3 να επηρεαστεί από ένα διάλυμα 1 λιτρου με PH=3 και να γίνει ΡΗ=3,32 μήπως οι προσεγγίσεις που κάνεις είναι πολύ χονδρές…..(0,09999999999).Τόσο εύκολα μπορούμε να αλλάζουμε το ΡΗ ενός μεγάλου σε όγκου διαλύματος;Παπαδάκης Γιάννης είπε:
Το αρχικό ερώτημα αφορούσε ανάμιξη ενός ισχυρού και ενός ασθενούς οξέος με Ph=3 και τα δύο.
Επιμένω, ότι το αποτέλεσμα της ανάμιξης, όταν ο όγκος του ασθενούς είναι πολύ μεγαλύτερος από τον όγκο του ισχυρού, το Ph που θα προκύψει θα είναι μεγαλύτερο από 3.
Δείτε το επισυναπτόμενο αρχείο.
 Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
Απάντηση από τον/την Παπαδάκης Γιάννης στις
-
Φυσικά αυτό θα συμβεί.Γιατι προσθέτοντας μια μικρή ποσότητα ισχυρού οξέως θα μειωθεί ο βαθμός ιοντισμού του ασθενούς.
Η επίδραση κοινού ιόντος, δεν λειτουργεί -οπως λάθος, νομίζω αναφέρθηκε σε προηγούμενο σχόλιο- με τρόπο ώστε να διατηρεί τη συγκέντρωση οξωνίων σταθερή. Δεν υπάρχει τέτοιος νόμος ούτε τέτοια επίδραση.
Η επίδραση κοινού ιόντος λειτουργεί με τρόπο τέτοιο, ώστε στον νόμο της ιοντικής ισορροπίας να μετέχει η συνολική συγκέντρωση οξωνίων.
Εξάλλου οι μαθηματικοί υπολογισμοί που παρέθεσα αυτό ακριβώς δεν αποδεικνύουν;
Έχεις ένσταση στην αντιμετώπιση του προβλήματος;
Για την ανάμιξη 1:9 παρουσίασα εκτός την λύση χωρίς προσεγγίσεις και λύση με προσεγγίσεις, μονο και μόνο για να δείξω ότι μπορούν να εφαρμοστούν και οι προσεγγίσεις χωρις ιδιαίτερη απόκλιση από το ακριβές αποτέλεσμα. Για μεγαλύτερες αραιώσεις οι απλοποιήσεις θα διευκόληναν τους μαθηματικούς υπολογισμούς.
Βέβαια στην λύση έχω κάνει ένα σημαντικό λάθος στο τέλος. Στην συγκέντρωση οξωνίων για τον υπολογισμό του ph, έβαλα το χ, ενώ έπρεπε να βάλω το 10^-4+χ στην 1η περίπτωση και το 10^-5+χ στην 2η. Όμως αυτό δεν αλλάζει την ουσία της μελέτης.
Απάντηση από τον/την Παπαδάκης Γιάννης στις
-
Της νύχτας τα καμώματα ….
Έγινε μια μικρή διόρθωση στον υπολογισμό του ph… - Συνημμένα:
 Απάντηση από τον/την Διονύσης Μάργαρης στις
Απάντηση από τον/την Διονύσης Μάργαρης στις
-
Φίλε Γιάννη καλημέρα.
(ελπίζω να ξύπνησες, γιατί τέτοιες … ώρες που γράφεις, μπορεί και να κοιμάσαι ακόμη. Αλλά αυτά τα γράφει ένας μεγαλύτερος και καταλαβαίνεις ότι μπαίνει και η ζήλια για τους .. .νεώτερους. Τάχω πάρει και λίγο με τον γιο μου που ακόμη δεν ξύπνησε…)
Δεν υπάρχει καμιά διαφορά στον τρόπο που αντιμετωπίζουμε το πρόβλημα. Το θέμα είναι τι βγάζουν αυτές οι σπαστικές εξισώσεις. Στην χθεσινή σου απάντηση υπάρχει ένα αριθμητικό λάθος στην διακρίνουσα.
Δεν έχεις πάρει το -4αγ αλλά -αγ με αποτέλεσμα να βγαίνει λάθος το αποτέλεσμα, οπότε και το συμπέρασμά σου.
Το αρχείο Excell που ανέβασε ο φίλος Αντωνης Μπαλτζοπουλος, σαν τροποποίηση του δικού μου, ώστε να μην έχει προσεγγίσεις εδώ δεν βγάζει διαφορά στο pH παρά μόνο στο 3ο δεκαδικό ψηφίο. (και από ότι μπόρεσα να το ελέγξω δεν βρήκα λάθος.).
Να σου εκμυστηρευτώ κάτι;
Θα μου πήγαινε και μένα η λογική να αυξάνεται το pH, αλλά δεν βγαίνει…
 Απάντηση από τον/την Νικόλαος Καχριμάνης στις
Απάντηση από τον/την Νικόλαος Καχριμάνης στις
-
Μια πιό απλή εξήγηση νομίζω ότι είναι η εξής η συγκέντρωση των [Η30+] είναι ίδια αρχικά όμως το νερό του διαλύματος του HCl προκαλεί αραίωση και μετατοπιζει την ισορροπία δεξιά άρα έστω και λίγο άρα …
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
Νικόλαος Καχριμάνης είπε:
Μια πιό απλή εξήγηση νομίζω ότι είναι η εξής η συγκέντρωση των [Η30+] είναι ίδια αρχικά όμως το νερό του διαλύματος του HCl προκαλεί αραίωση και μετατοπιζει την ισορροπία δεξιά άρα έστω και λίγο άρα ……
Εγω σημερα μιλησα με τον κ.Σαλτερή και μου ειπε πανω κάτω ότι ο προς τα αριστερά παράγοντας ( ΕΚΙ ) αναιρείται από τον προς τα δεξια παράγοντα ( αραίωση ) και έτσι το πεχα μένει σταθερό. ( Περίπτωση αναλογη με το Qc=Kc της Χημικής ισορροπίας )
Μου είπε να τσεκάρω τους βαθμούς ιοντισμού για να δώ ότι δεν αλλάζουν ( κατι που ισχύει για την μελέτη χωρίς προσεγγιση αλλά δεν ισχύει για την μελέτη με προσέγγιση … ενώ δεν ισχύει για την περίπτωση των 2 ασθενών ηλεκτρολυτών … που εξακολουθώ να μην μπορώ να βρω την υπομονή να την λύσω χωρίς προσέγγιση )
Δεν κρύβω ότι δεν πείστηκα πολύ … αλλά και εμένα τα νουμερα με οδηγούν στο 3. ( και τρέφω και απειρο σεβασμό στο κ. Σαλτερή )
Δεν πείστηκα γιατί και ο ίδιος ο κ.Σαλτερής λύνει (τελικά) άσκηση με παρόμοιες τιμες ( όχι περίπτωση 3+3 = 3 ) χωρίς να κάνει την προσεγγιση στο C1-X … «Ανόργανη Χημεια Γ Λυκείου» Εκδόσεις Σαββάλα – 1994 / σελ 256-257 ασκηση 5.53
Επίσης οι Κορέσης-Ντάσης στο γνωστο βοήθημα λύνουν ανάλογη ασκηση ( σελ 130-132 ) χωρίς να κάνουν την προσέγγιση στο C1-X στην άσκηση με παρόμοιες τιμές και περίπτωση ασθενούς/ισχυρού ….
….
Απάντηση από τον/την Παναγιώτης Χριστάκος στις
-
Φίλε Αντώνη, παραθέτω την παρακάτω σκέψη μου υποστηρίζοντας την αρχική θέση μου όσο και τη θέση του κου Παπαδάκη, (οτι δηλ. το pH αυξάνεται):Εστω 1L του δ/τος CH3COOH : περιέχει 10^{-3} mol Η3Ο+.
Τα βάφουμε κόκκινα. Επομένως κόκκινα = 10^{-3}Προσθέτω 1L H2O. Τα κόκκινα αυξήθηκαν -αραίωση- (τα βάφουμε όλα πράσινα).
Αρα πράσινα > κόκκινα.
Ομως κόκκινα/2 > πράσινα >2 αφού η αραίωση καθιστά το διάλυμα λιγότερο όξινο (αύξηση pH)Προσθέτω 10^{-3} mol Η3Ο+ , τα πράσινα μειώθηκαν(ΕΚΙ), έγιναν κίτρινα
Αρα κίτρινα/2 < πράσινα/2 < κόκκινα/2 = 10^{-3}/2Τελικά ποια είναι η [Η3Ο+];
Δεν είναι [10^{-3} + κίτρινα ]/2 δηλαδή μικρότερη από από 10^{-3}Μ και το pH μεγαλύτερο από 3;
Τώρα αν αυτή η διαφορά είναι τέτοια που δεν υπολογίζεται πρακτικά ή δεν αξίζει τον κόπο να την υπολογίσεις αυτό είναι άλλο θέμα.Να ρωτήσω κάτι άλλο. Στην πολλαπλής επιλογής :
Σε διάλυμα HCl έστω 0,1Μ ισχύει:
α. [Η3Ο+]=[Cl-]
β. [Η3Ο+]>[Cl-]
γ. [Η3Ο+]<[Cl-]
Δε δίνουμε ως σωστή απάντηση τη β λόγω του αυτοϊοντισμού; Το λαμβάνουμε αυτό ποτέ υπόψη στους υπολογισμούς;
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
Παναγιώτης Χριστάκος είπε:
Να ρωτήσω κάτι άλλο. Στην πολλαπλής επιλογής :
Σε διάλυμα HCl έστω 0,1Μ ισχύει:
α. [Η3Ο+]=[Cl-]
β. [Η3Ο+]>[Cl-]
γ. [Η3Ο+]<[Cl-]
Δε δίνουμε ως σωστή απάντηση τη β λόγω του αυτοϊοντισμού; Το λαμβάνουμε αυτό ποτέ υπόψη στους υπολογισμούς;Παρενθετικά στο συγκεκριμένο θέμα απαντώ Α ( κυρίως εκ του πονηρού … γιατι εαν ηταν το Β , τοτε δεν θα είχε νοημα η αναγραφή της συγκέντρωσης 0,1 στην εκφώνηση )
… εαν είχαμε C=10^-7 θα απαντούσα το ΒΤεσπα … θα επανέλθω με το κυριο συλλογισμό σου
 Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
Απάντηση από τον/την ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ στις
-
Αν δουλεύαμε με mole στο αρχικό διάλυμα θα είχαμε 0,1.V1 -10-3.V1 mol οξικού οξέος 10-3.V1 mole οξικών ανιόντων και 10-3V1 mol οξωνιων.Αν προσθέσουμε και το διάλυμα ΗCl θα έχουμε και 10-3V2 mole οξωνίων που θα προέρχονται από τον ιοντισμό του HCl.Aν πάρουμε τώρα την QC με την υπόθεση ότι η ισορροπία δεν θα μετατοπισθεί θα βλέπαμε ότι το QC=10-5 άρα η ισορροπία δεν θα μετατοπιζόταν μόνο με την υποθεση ότι το 0,1V1-10-3V1=0,1V1 .To ΡΗ θα ήταν φυσικά 3.Αρα μάλλον θα πρέπει να συγλίνουμε στην άποψη του Αντώνη.
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
Ετοίμασα ένα excel-όφυλο που λύνει την άσκηση ανάμιξης διαλύματος ασθενούς οξέος με διάλυμα ισχυρού οξέος ΧΩΡΙΣ να κάνει αριθμητικές προσεγγίσεις. …Ξεκίνησα την νέα μου τοποθέτηση πάνω στο θέμα, από την σκέψη / παραδοχή ότι οι μαθηματικές προσεγγίσεις στην επίλυση της άσκησης είναι μέρος της «δικής μου» αδυναμίας και όχι μέρος του φαινόμενου που συζητάμε.
Επίσης είναι φανερό ότι η προσεγγίσεις που κάνουμε για να λύσουμε την άσκηση «καπελώνουν» την εκδήλωση το όποιου φαινόμενου.
ΞΕΚΑΘΑΡΙΖΩ ότι στην αίθουσα θα έλυνα την άσκηση με προσεγγίσεις που όπως θα δείξω καταλήγουν στο ίδιο αποτέλεσμα.
Πρώτα-πρώτα
Το διάλυμα CH3COOH 0.1 M έχει pH = 3,00021715 και βαθμό ιοντισμού α= 0,009950
Το διάλυμα HCl 0,1 Μ έχει pH = 3
Μια λογική σκέψη είναι το pH του διαλύματος που προκύπτει να είναι ανάμεσα σε αυτές τις δύο τιμές. ( αυτό θα οδηγούσε σε μείωση του pH σε σύγκριση με το αρχικό ) ή ακόμα εάν θέλετε το πεχα θα μειωθεί αφού προσθέτουμε πιο όξινο διάλυμα. ( όπως και να το δείς περιμένουμε μείωση του νεου πεχα )
Προς τα πού όμως μετατοπίζεται η ιοντική ισορροπία του CH3COOH μιας που έχουμε ταυτόχρονη ΕΚΙ ( που οδηγεί προς τα αριστερά ) και αραίωση ( που οδηγεί προς τα δεξιά )
Εύρεση Qc = [CH3COO][H3O]/CH3COOH] με τις ποσότητες που υπάρχουν στα δυο διαλύματα ( εύρεση επιμέρους mol και διαίρεση στον τελικό όγκο για συγκεντρώσεις στο διάλυμα από την αναμίξη )
Qc = 1.002506*10^-6 δηλ μεγαλύτερο από την Κα. Αρα η ιοντική ισορροπία θα μετατοπιστεί προς τα αριστερά
Και πραγματικά εάν λύσουμε την ιοντική ισορροπία του διαλύματος που προκύπτει από την ( οποιαδήποτε ) ανάμιξη θα βρούμε μικρότερο βαθμό ιοντισμου ( αρα είχαμε όντως μετατόπιση προς τα αριστερά όπως μας έδειξε/προέβλεψε η Qc ) ενώ το pH πήρε μια τιμή που ήταν ανάμεσα στις δύο αρχικές. ( δηλ πραγματικά μειώθηκε )
Δοκιμάστε και με άλλες τιμές Κ , C1 , C2 , V1 , V2 ( προσοχή στο σημαντικό ψηφίο στο κελί ) και θα δείτε ανάλογα αποτελέσματα. Οι τιμές του πεχα που προκύπτουν είναι πάντα ανάμεσα στις 2 αρχικές τιμές και η μεταβολή του βαθμού ιοντισμού είναι πάντα σε συμφωνία με την φορά της μετατόπισης που δείχνει και η Qc.
Ας πάμε όμως στην φιλοσοφία του αρχικού ερωτήματος . Τι θα προκύψει εάν αναμίξουμε διαλύματα με ίδιο πεχα ( όπως προφανώς υπονοούσε η άσκηση και όπως είχε σαν βασικό άξονα η σκέψη του Χρήστου )
Ας πούμε λοιπόν ότι αρχικά είχαμε
Διάλυμα CH3COOH 0.1 M ( K=10^-5) ( που έχει αρχικό πεχα = 3,00021715 )
Και
Διάλυμα HCl 0.0009950125 M που έχει και αυτό πεχα = 3,00021715Τότε βάση των παραπάνω η τιμή του πεχα στο διάλυμα που θα προκύψει από οποιαδήποτε ανάμιξη των δύο αυτών διαλύματων θα είναι ανάμεσα στο 3,00021715 και στο 3,00021715 …. Δηλ … 3,00021715 ( σταθερό)
Η μελέτη της Qc δίνει τιμή 1,00000*10^-5 ( είμαστε στο 10ο δεκαδικό !!! ) αρα η ιοντική ισορροπία δεν θα μετατοπιστεί.
Και πραγματικά, η μελέτη της ιοντικής ισορροπίας στο διάλυμα που προκύπτει από την ανάμιξη δίνει την ίδια τιμή πεχα και – κυρίως – τον ίδιο βαθμό ιοντισμού ( που αποδεικνύει την μη μετατόπιση )
Οποιον όγκο και να χρησιμοποιήσουμε από τα διαλύματα η απάντηση είναι ίδια !
- Συνημμένα:
-
Αντωνης Μπαλτζοπουλος είπε:
Πρώτα-πρώταΤο διάλυμα CH3COOH 0.1 M έχει pH = 3,00021715 και βαθμό ιοντισμού α= 0,009950
Το διάλυμα HCl 0,1 Μ έχει pH = 3
- το διάλυμα HCl 0.001 M έχει pH = 3
 Απάντηση από τον/την Νικόλαος Καχριμάνης στις
Απάντηση από τον/την Νικόλαος Καχριμάνης στις
-
Το έχω σκεφτεί και αυτό και πράγματι έθεσα την ερώτηση γιατί ήμουν ανάμεσα στο αυξάνεται και στο μένει σταθερό. Τώρα πια πιστεύω ότι μένει σταθερό με την εξής λογική:
Η συγκέντρωση των οξωνίων δεν αλλάζει. Η αραίωση είναι η ίδια και στο CH3COOH και στα CH3COO- αν τα βάλω λοιπόν στην έκφραση της Κα ο λόγος τους είναι ο ίδιος άρα η ισορροπία δεν μετατοπίζεται. Απάντηση από τον/την Νικόλαος Καχριμάνης στις
Απάντηση από τον/την Νικόλαος Καχριμάνης στις -
HCl + H20 -> Cl- + H30+
0,1 0,1 0,1
[H30+].[OH-] =10-14 άρα [ΟΗ-] =10-13
επομένως στον αυτοιοντισμό ισχύει [H30+]=[ΟΗ-] =10-13 και η ολική[H30+]είναι 0,1 + 10-13 Δηλαδή 0,1Μ
 Απάντηση από τον/την Νικόλαος Καχριμάνης στις
Απάντηση από τον/την Νικόλαος Καχριμάνης στις -
Αρχικά έθεσα την ερώτηση γιατί ήμουν ανάμεσα στο αυξάνεται (περισσότερο στο αυξάνεται) και στο μένει σταθερό. Τώρα πια πιστεύω ότι μένει σταθερό με την εξής λογική:
Η συγκέντρωση των οξωνίων δεν αλλάζει. Η αραίωση είναι η ίδια και στο CH3COOH και στα CH3COO- αν τα βάλω λοιπόν στην έκφραση της Κα ο λόγος τους είναι ο ίδιος άρα η ισορροπία δεν μετατοπίζεται.
Φανταστείτε λοιπόν να βρεθεί κάποιος και να θέσει ένα τέτοιο θέμα στις πανελλήνιες….. Έχει να γίνει το έλα να δείς.
Επίσης δεν πίστευα ότι ένα τέτοιο ερώτημα θα φέρει τόση συζήτηση.
Είναι ένα δείγμα τελικά ότι εμείς οι εκπαιδευτικοί δεν είμαστε και τόσο αδιάφοροι.
 Απάντηση από τον/την Σπύρος Καρέκος στις
Απάντηση από τον/την Σπύρος Καρέκος στις -
Συνάδελφοι, για την ανάμιξη διαλυμάτων με ίδια τιμή pH, ανεξάρτητα διαλυμένων ουσιών, ισχύει ο νόμος: «Με οποιαδήποτε σχέση όγκων ανάμιξης, το μίγμα έχει την ίδια τιμή pH με τα αρχικά διαλύματα.» Σαν παράδειγμα μπορούμε να πάρουμε τα διαλύματα Δ1 (CH3COOH με C1=0,1 M Ka = 10-5 {με pH=3}) και Δ2 (HCl με pH=3). Στην ισορροπία ιοντισμού στο Δ1 έχουμε [CH3COOH] = 0,1-10-3, [CH3COO-]=[H3O+] =10-3.
Αν χρησιμοποιήσουμε V1L του Δ1 και V2L του Δ2 την στιγμή ανάμιξης έχουμε:
[CH3COOH]’ = (0,1-10-3) V1/(V1+V2)
[CH3COO-]’ = 10-3 V1/(V1+V2)
και [H3O+]’ = 10-3 V1/(V1+V2)+10-3 V2/(V1+V2) = 10-3
Τότε το κλάσμα Q = [CH3COO-]’ . [H3O+]’ / [CH3COOH]’ είναι ίσο με την τιμή Κa του CH3COOH, άρα η ισορροπία του οξέος δεν μετατοπίζεται και η τελική τιμή pH παραμένει 3.
Με αντίστοιχους τρόπους (εύρεσης Qc=Kc) κατά τη στιγμή ανάμιξης διαλυμάτων ίδιας τιμής pH σποδεικνύουμε ότι το μίγμα διατηρεί ίδιο pH με τα αρχικά διαλύματα.
 Απάντηση από τον/την ΠΑΥΛΟΣ ΜΠΑΣΔΑΡΑΣ στις
Απάντηση από τον/την ΠΑΥΛΟΣ ΜΠΑΣΔΑΡΑΣ στις -
Αγαπητε συναδελφε Σπυρο ,αυτο που αναφερεις σαν νομο θα ειχε ισχυ στη συγγεκριμενη περιπτωση μονο για ισχυρους ηλεκτρολυτες π.χ αν στη θεση του οξικου υπηρχε ΗΒr. Αν κανεις επαληθευση στη συγκεκριμενη ασκηση για ΡΗ=3 καταληγεις σε ατοπο. Η θεωρητικη προσεγγιση απλη και κατανοητη ειναι αυτη του συναδελφου Χρηστακου διοτι αν εχω ΗΒr και HCl προκυπτει PH=3 αν ομως τη θεση του HBr παρει το οξικο τοτε εκτος απο την αραιωση , μειωση της συγκεντρωσης των οξονιων προκαλει και η επιδραση κοινου ιοντος απο το ΗCL .Μαθηματικα επιλυοντας την ασκηση χωρις προσεγγισεις βρισκουμε παντα ΡΗ>3.
 Απάντηση από τον/την Σπύρος Καρέκος στις
Απάντηση από τον/την Σπύρος Καρέκος στις -
Αγαπητε Παυλο,στελνω την αποδειξη του Νομου η αν θες του Θεωρηματος αναμιξης δ/των ιδιου pH»Aνεξαρτητα του ειδους των διαλυμενων ουσιων και των ογκων αναμιξης, το μιγμα εχει pH ιδιο με τα αρχικα δ/τα. Περιπτωση ισχυρων οξεων η βασεων.» Τα δ/τα Δ-1, Δ-2 εχουν pH=α, οποτε για την ισορροπια του ΗΟΗ θα ισχυουν και στα δυο δ/τα [Η3Ο+]=10-ακαι [OH-]=10-14-α
Αν αναμιχθούν όγκοι V1,V2 των Δ-1,Δ-2 τη στιγμή ανάμιξης θα έχουμε [Η3Ο+]=V1*10-α/(V1+V2) ++ V2*10-α/(V1+V2)=10-α και βέβαια αντίστοιχα [OH-]=10-14-αΆρα κατά την ανάμιξη η ισορροπία του νερού δεν μετατοπίζεται και η τιμή pH μένει σταθερή.Περιπτωση όπου υπαρχει τουλαχιστον ενας ασθενης ηλεκτρολυτης:Τα δ/τα Δ-1, Δ-2 εχουν pH=α, και περιεχουν π.χ. το Δ-1 το οξυ ΗΑ(C1, Kα) και το Δ-2 HCl. Στο Δ-1 θα εχουμε [ΗΑ]=C1-10-α, [Α–]=[Η3Ο+]=
=10-α και βεβαια Kα =10-2α/C1-10-α. Στο Δ-2 θα ισχυει [Η3Ο+]=10-α και [ΟΗ–]=10-14-α.
Την στιγμη αναμιξης V1 L του Δ-1 με V2 L του Δ-2 θα ειναι: [ΗΑ]’=C1-10-α*V1/(V1+V2)
[Α–]’=10-α*V1/(V1+V2) και [Η3Ο+]’=10-α*V1/(V1+V2) + 10-α*V2/(V1+V2)=10-α.
Τοτε Q=[Α–]’*[Η3Ο+]’/[HA]’ =10-2α/C1-10-α=Kα. Αρα μετα την αναμιξη δεν γινεται μετατοπιση ισορροπιας καμιας αμφιδρομης αντιδρασης (ουτε του ΗΑ ουτε του Η2Ο) οποτε τελικα pH = α.
Πιστευω οτι ο συμβατικος τροπος επιλυσης προβληματος αναμιξης διαλυματων ηλεκτρολυτων με ιδια τιμη pH δινει ακριβη αποτελεσματα μονο στην περιπτωση που οι ηλεκτρολυτες ειναι ισχυροι (οξυ-οξυ, βαση-βαση). Για την περιπτωση ισχυρου-ασθενους (π.χ. οξικο οξυ, υδροχλωριο) ο συμβατικος τροπος – δεν παιρνει υπ’οψη τον ιοντισμο του νερου – και γι’αυτο δινει ανακριβη αποτελεσματα. Για το λογο αυτο απαιτειται συγκεκριμενη σχεση ογκων αναμιξης τετοιων διαλυματων ωστε να προκυψει το pH του μιγματος ιδιο με αυτο των αρχικων διαλυματων.
-
 Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
-
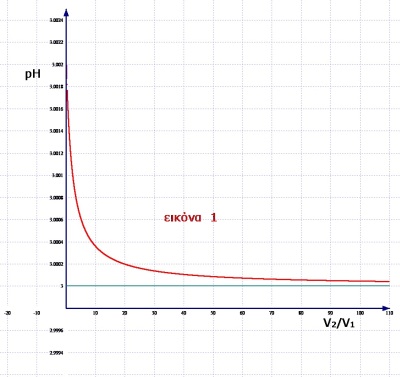
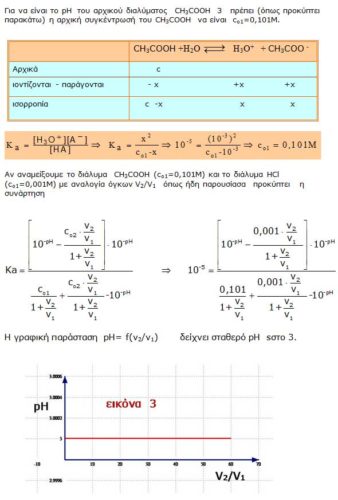
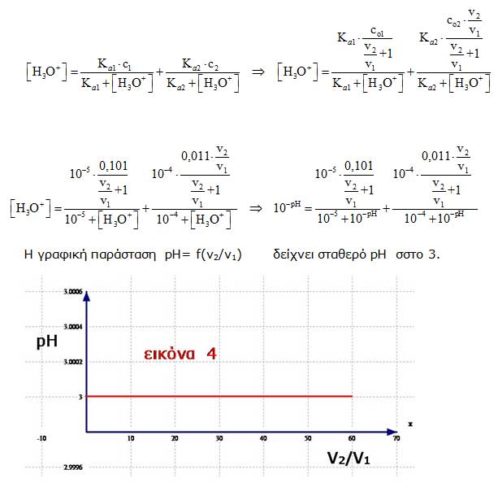
Χωρίς καμία προσέγγιση και λαμβάνοντας υπ’ όψιν την Ε.Κ.Ι. προκύπτει συνάρτηση του pH=f(V2/V1) με γραφική παράσταση όπως φαίνεται στην εικόνα 1.
Με την ανάμειξη το pH του διαλύματος που προκύπτει κυμαίνεται μεταξύ του pH του καθαρού διαλύματος CH3COOH που είναι 3,002 και του pH του καθαρού διαλύματος HCl που είναι 3. Συνεπώς μπορούμε να θεωρήσουμε ότι το pH διαλύματος που προκύπτει από την ανάμειξη είναι «σταθερό» στο «3».
Παράδειγμα με ασθενές οξύ HA C1=1M Kα=10 -4 και διάλυμα HCl με C2=10-2, οδηγεί στα ίδια συμπεράσματα. Με το pH του διαλύματος να κυμαίνεται μεταξύ του pH του καθαρού διαλύματος HΑ που είναι 2,002 και του pH του καθαρού διαλύματος HCl που είναι 2 ( εικόνα 2). Δηλαδή το pH διαλύματος που προκύπτει από την ανάμειξη είναι «σταθερό» στο «2».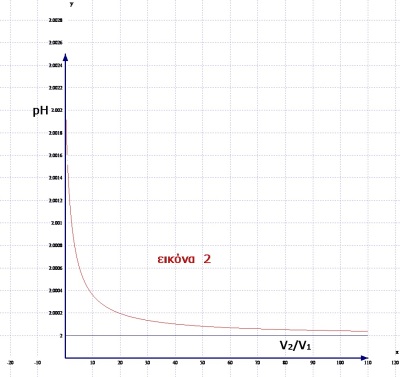
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
…. Δάσκαλε , μπορείς να γράψεις κατι παραπάνω για αυτό ?
Παπαδοπουλος Γεώργιος είπε:
Χωρίς καμία προσέγγιση και λαμβάνοντας υπ’ όψιν την Ε.Κ.Ι. προκύπτει συνάρτηση του pH=f(V2/V1)…..
 Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
-
Αν αναμείξουμε τα δύο διαλύματα με αναλογία όγκων V2/V1 οι συγκεντρώσεις των CH3COOH και HCl στο τελικό διάλυμα είναι:
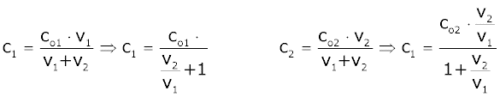
HCl + H2O Cl– + H3O+ C2 -C2 +C2 0 C2 CH3COOH + H2O CH3COO– + H3O+ C1 C2 -x +x +x C1-x +x C2+x 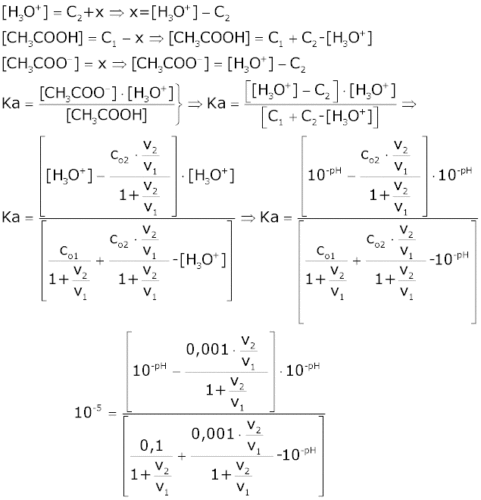
Για τις γραφικές παραστάσεις χρησιμοποιήθηκε το πρόγραμμα Graph.
 Απάντηση από τον/την ΠΑΥΛΟΣ ΜΠΑΣΔΑΡΑΣ στις
Απάντηση από τον/την ΠΑΥΛΟΣ ΜΠΑΣΔΑΡΑΣ στις
-
Αγαπητοί συνάδελφοι, όταν σε διαλύματα ασθενών ηλεκτρολυτών, έχουμε προσθήκη άλλων ηλεκτρολυτών και μάλιστα ισχυρών, όπως στην προκειμένη περίπτωση, τότε λόγω αυξημένης ιονικής ισχύος, αν επιδιώκουμε ακριβή και όχι προσεγγιστικά αποτελέσματα,πιστευω οτι σωστο ειναι να χρησιμοποιούμε την πραγματική συγκέντρωση α και όχι την συμβατική cόπως και την πραγματική Καντι της συμβατικής Κα
Απο τη γνωστη σχέση που τις συνδέει α = γ c , όπου γ ο συντελεστής ενεργότητας του σωματιδίου ,εχουμε για τα οξωνια α Η3Ο+ = γ Η3Ο+ c Η3Ο+ και επειδή γ Η3Ο+ < 1 προκύπτει α Η3Ο+ < c Η3Ο+ αν λοιπον στην περίπτωση μας στη συμβατική c αντιστοχει PΗ=3,στην πραγματική συγκέντρωση ααντιστοιχεί PΗ<3.
 Απάντηση από τον/την ΠΑΥΛΟΣ ΜΠΑΣΔΑΡΑΣ στις
Απάντηση από τον/την ΠΑΥΛΟΣ ΜΠΑΣΔΑΡΑΣ στις
-
PAYLOS MPASDARAS είπε:
Αγαπητοί συνάδελφοι, όταν σε διαλύματα ασθενών ηλεκτρολυτών, έχουμε προσθήκη άλλων ηλεκτρολυτών και μάλιστα ισχυρών, όπως στην προκειμένη περίπτωση, τότε λόγω αυξημένης ιονικής ισχύος, αν επιδιώκουμε ακριβή και όχι προσεγγιστικά αποτελέσματα,πιστευω οτι σωστο ειναι να χρησιμοποιούμε την πραγματική συγκέντρωση α (ενεργοτητα) και όχι την συμβατική c όπως και την πραγματική Κ(Θερμοδυναμικη σταθερα) αντι της συμβατικής Κα
Απο τη γνωστη σχέση που τις συνδέει α = γ c , όπου γ ο συντελεστής ενεργότητας του σωματιδίου ,εχουμε για τα οξωνια α Η3Ο+ = γ Η3Ο+ c Η3Ο+ και επειδή γ Η3Ο+ < 1 προκύπτει α Η3Ο+ < c Η3Ο+ αν λοιπον στην περίπτωση μας στη συμβατική c αντιστοχει PΗ=3,στην πραγματική συγκέντρωση α αντιστοιχεί PH>3.
 Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
Απάντηση από τον/την Παπαδοπουλος Γεώργιος στις
 Απάντηση από τον/την Σπύρος Καρέκος στις
Απάντηση από τον/την Σπύρος Καρέκος στις
-
Σας παραθέτω δύο λύσεις που μου έστειλε ο συνάδελφος Γιάννης Κεφαλλωνίτης στο παρακάτω έγγραφο.
https://docs.google.com/viewer?a=v&pid=explorer&chrome=true…
 Απάντηση από τον/την χρηστος παπαδοπουλος στις
Απάντηση από τον/την χρηστος παπαδοπουλος στις
-
Αγαπητοι συναδελφοι,ενα καθαρα χημικο προβλημα το μετατρεψαμε σε μαθηματικο.Αν θελουμε ακριβη αποτελεσματα πρεπει να χρισημοποιηθει η θερμοδυναμικη σταθερα Κ που δινει την πραγματικη συγκενρωση (ενεργοτητα) των h3o.Στο ιδιο θεμα αναφερεται ο αειμνηστος Δ.Γιανακουδακης σελ 153 εκδοση 1977 ασκησεις φυσικοχημειας και ο καθηγητης μου της αναλυτικης χημειας στο ΑΠΘ Ντινος Παπαδοπουλος στη σελιδα 27 εκδοση του 1984 οτι.οταν εχουμε διαλυμα ασθενους ηλεκτρολυτη και ισχυρου ηλεκτρολυτη συγχρονως τοτε αντι των συμβατικων συγκεντρωσεων χρισημοποιουμε τισ ενεργοτητες.προσεγγιση καθαρα χημικη ειναι του συναδελφου Κ μπασδαρα που με βρισκει συμφωνο
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
-
… η απόδειξή σας πάντως λειτουργεί ΚΑΙ για την περίπτωση ανάμιξης διαλυμάτων ασθενών οξέων με ίδια αρχική τιμή pH ( όπου βέβαια απαιτείται έλεγχος Q και στις δύο Κ )
 Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις
Απάντηση από τον/την Αντώνης Μπαλτζόπουλος στις -
το πρόσεξε ένας συνάδελφος στο DFE.
Πανελλήνιες 2011 – ΘΕΜΑ Δ4
Διαθέτουμε υδατικά διαλύματα CH3COONa 0,1M (διάλυμα A) και NaF 1M (διάλυμα B).
.
.
.
.
.
Δ4
10 mL του διαλύματος Α ( που έχει pH = 9 ) αναμειγνύονται με 40 mL του διαλύματος Β ( ( που έχει pH = 9 ) και προκύπτουν 50 mL διαλύματος Γ. ( που θα έχει pH = 9 )
Να υπολογιστεί το pH του διαλύματος Γ.
Δίνεται ότι:
• Όλα τα διαλύματα βρίσκονται σε θερμοκρασία θ=25°C,Ka(CH3COOH)=10−5, Ka(ΗF) =10−4 , Kw=10−14
 Απάντηση από τον/την Διονύσης Μάργαρης στις
Απάντηση από τον/την Διονύσης Μάργαρης στις -
Σωστά Αντώνη.
Αν κάποιος υπολόγιζε το pH του β’ διαλύματος, θα μπορούσε να υποστηρίξει ότι το pH του τελικού διαλύματος είναι 9!! χωρίς καμιά άλλη λύση. (δύο διαλύματα με την ίδια τιμή pH που αναμιγνύονται με οποιαδήποτε αναλογία όγκων διατηρούν σταθερό το pH τους.
Αλλά είναι το μόνο λεπτό σημείο των θεμάτων; Το φελλίγγειο υγρό τι οξειδώνει;;;
Σε ποια τροχιακά βρίσκονται τα ηλεκτρόνια των ατόμων/ιόντων;
Ποιο το pH διαλύματος ΝαΟΗ;
Αλλά δεν βλέπω ιδιαίτερο πάθος από τους φίλους Χημικούς, οπότε …
-
![]()
… ετσι απλά ? ( η άσκηση ειναι θεωρητική ή πρέπει να λυθεί αριθμητικά ?…. μια γρήγορη σκεψη ……εαν ειναι θεωρητική… θα έλεγα ότι το pH αυξάνει εφόσον η προσθήκη του ισχυρου ηλεκτρολύτη δεν αυξάνει την οξυτητα λογω του 0,001 ενω ταυτόχρονα έχουμε και αραίωση )( εάν είχαμε συγκέντρωση του δ/τος HCl να ειναι μεγαλύτερη του 0,001 η άσκηση δεν θα λυνονταν – εκτιμώ – αφού θα είχαμε αντικρουόμενους παράγοντες και χωρίς να ξέρουμε την έκταση της αραίωσης δεν θα ξέραμε ποιος παράγοντας θα υπερισχύσει )
… όλα αυτα στα γρήγορα ( με εν θερμω σκέψεις )
Το pH μπορεί να αυξάνεται να μειώνεται ή να παραμένει σταθερό και αυτό θα εξαρτηθεί από την αναλογία όγκων με τους οποίους θα αναμείξεις τα δύο διαλύματα.
π.χ. Αν είναι ίσοι οι όγκοι το pH θα μείνει σταθερό (αν δεν έχω κάνει λάθος στις πράξεις… βράδυ είναι), αν είναι μεγαλύτερος ο όγκος του HCl το pH θα αυξηθεί, ενώ στην αντίθετη περίπτωση θα μειωθεί.
Διονύσης Μάργαρης είπε:
επιβεβαιώνω ( και για μενα βράδυ είναι …επλπίζω να μην έκανα κατι στραβό )
από την επίλυση της ΕΚΙ μετά από τις νεες συγκεντρώσεις προκύπτει ότι …
[Η3Ο] = 10^-3 * V1 / V2
Ean V1>V2 => [Η3Ο] > 10^-3 => pH < 3
Ean V1=V2 => [Η3Ο] = 10^-3 => pH = 3
Ean V1 [Η3Ο] < 10^-3 => pH > 3
… kalo quiz ( έστω και βραδιάτικα )
..το CH3COOH ειναι ασθενες. Δεν ιοντίζεται πλήρως
. Μ ε την προσθηκη του διαλύματος HCl η συνεισφορα του CH3COOH σε ιόντα H3O αλλάζει αφού έχουμε και ΕΚΙ αλλά και αραίωσηΗ άσκηση λυμενη ….
To ξέρω ότι το οξικό είναι ασθενές.Ας το πάρουμε λίγο από την αρχή.Αν πάρω νέες συγκεντρώσεις για το HCl θα έχω [Η3Ο]=10-3V2/V1+V2 αυτά προέρχονται από τον ιοντισμό του HCl στο νέο διάλυμα.Αν τώρα κάνω διάσταση του οξικού οξεος από τη Κα και χωρίς να κάνω απλοποίηση του για τα [Η3Ο] θα βγάλω ότι [CH3COO]=10-6.V1/{V1+V2}[H3O]. Ετσι τα συνολικά ιόντα [Η3Ο]=10-6.V1/{V1+V2}[H3O] + 10-3V2/V1+V2 .Η παραπάνω εξίσωση έχει λύση την [Η3Ο]=10-3. Η λογική με οδηγεί.Αν ανακατέψω νερό 10C με άλλη ποσότητα νερού 10C η τελική θερμοκρασία δεν θα είναι πάλι 10C;Aν ανακατέψω διαλύμα με ΡΗ=3 με άλλο διάλυμα με ΡΗ=3 δεν θα βγει πάλι ΡΗ=3;Αντωνης Μπαλτζοπουλος είπε:
Δεν νομίζω ότι χρειάζονται υπολογισμοί. Αν είχαμε όλα τα δεδομένα ναι. Με την άσκηση όμως όπως δίνεται νομίζω ισχύουν τα εξής :Γενικά η παρουσία του ισχυρού οξέως HCl περιορίζει (ουσιαστικά μηδενίζει) τον ιοντισμό του ασθενούς οξέως εξαιτίας του κοινού ιόντος (οξωνίου). Οπότε το ph καθορίζεται αποκλειστικά από την συγκέντρωση ιόντων οξωνίου που θα προκύψουν από το ισχυρό οξύ, και θα είναι ίση με την συγκέντρωση του HCl που θα έχει στο νέο διάλυμα αφού θα έχει αραιωθεί με τον όγκο του νερού του ασθενούς οξέως θα είναι μικρότερη. Το τελικό ph θα είναι μεγαλύτερο από 3.
Στην περίπτωση όμως που οι όγκοι των δύο διαλυμάτων έχουν πολύ μεγάλη διαφορά τότε:
Α. Η προσθήκη ελάχιστης ποσότητας διαλύματος HCl σε πάρα πολύ μεγάλη ποσότητα διαλύματος του ασθενούς οξέως θα μειώσει τον βαθμό ιοντισμού του ασθενούς οξέως (επίδραση του κοινού ιόντος οξωνίου) όμως η συγκέντρωση ιόντων οξωνίου δεν με μεταβληθεί στο σύνολο σημαντικά (στην πραγματικότητα θα υπάρξει μια μικρή αύξηση) και το ph τελικά θα μείνει πρακτικά αμετάβλητο δηλαδή 3.
Β. Η προσθήκη ελάχιστης ποσότητας διαλύματος ασθενούς οξέως σε πάρα πολύ μεγάλη ποσότητα διαλύματος HCl δεν θα μεταβάλει ουσιαστικά την τελική συγκέντρωση του HCl, ούτε και την συγκέντρωση ιόντων οξωνίου μιας και το ασθενές οξύ δεν θα πάθει καθόλου διάσταση λόγω της παρουσίας του ισχυρού HCl (επίδραση του κοινού ιόντος οξωνίου), και το ph θα είναι πάλι 3.
Γιατί στην Κα αντί για την συγκέντρωση [CH3COO] βάζεις C2 δηλαδή την συγκέντρωση του ΗCl;Δεν πρέπει να βάλεις το χ και να το συνδέσεις με τη συγκέντρωση του ΗCl΄;Αντωνης Μπαλτζοπουλος είπε:
ΧΡΗΣΤΟΣ ΕΛΕΥΘΕΡΙΟΥ είπε:
… έχεις δίκιο ως προς αυτό. Λιγο η δυναμη της συνήθειας και περισσότερο το βραδυνό της υπόθεσης με έκαναν να πάρω – τυφλοσούρτη – την ΕΚΙ και στα οξικά ιόντα . ( μάλλον το ίδιο έχει κάνει και ο Διονύσης )
Πραγματικά η [CH3COO]=χ …
Όμως , Η συγκέντρωση των ιόντων Η3Ο που προέρχονται από το CH3COOH μετά από την προσθήκη του δ/τος HCl δεν προκύπτει από τυπους αραίιωσης.
Η απάντηση που υιοθετώ ειναι αυτή του κ. Παπαδάκη μιας που τελικα [Η3Ο]= χ’ + C2′ όπου C2 είναι η νέα συγκετρωση που θα αποκτήσει το δ/μα HCL .
Όσο η αραίωση ειναι σε επίπεδα που μας επιτρέπει να πούμε [Η3Ο]= χ’ + C2′ = C2′ τότε η μελέτη του C2′ = 10^-3*V2 / V1 + V2 μας οδηγεί σε μείωση της συγκέντρωσης των οξωνίων άρα αύξηση του pH.
Επειδή το CH3COOH είναι ασθενές η συνεισφορά του σε οξώνια (συγκέντρωση) στο τελικό διάλυμα είναι μικρότερη λόγω επίδρασης κοινού ιόντος. Συνεπώς το pH του τελικού διαλύματος θα αυξηθεί