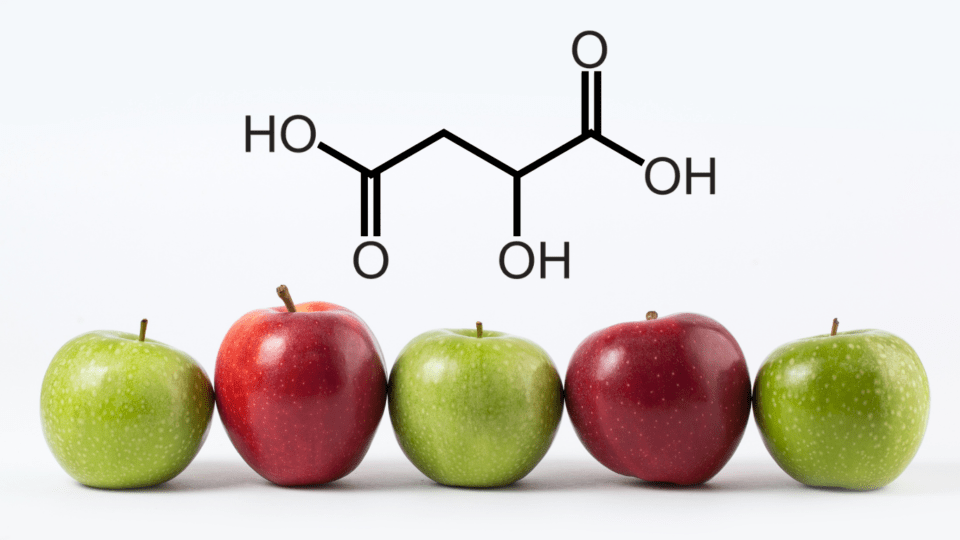
Το μηλικό οξύ C4H6O5 αποτελεί ένα φυσικό οργανικό οξύ που συναντάται στα πράσινα μήλα (και άλλα φυσικά προϊόντα ).
Διαθέτουμε ένα μείγμα το οποίο περιέχει 0,2 mol μηλικού οξέος και a mol ενός ακόρεστου υδρογονάνθρακα CxΗψ με x<4 . Η ποσότητα αυτή του υδρογονάνθρακα απαιτεί 0,2 mol ΗCl για πλήρη αντίδραση . Όταν όλη η ποσότητα του μείγματος καεί με την απαιτούμενη ποσότητα Ο2 ,πραγματοποιώντας τέλεια καύση, παράγονται 1,2 mol CO2 . Nα προσδιοριστεί ο Σ.Τ του υδρογονάνθρακα.
![]()
Γεια σου Τόνια! Το μόνο που με προβληματίζει λίγο είναι ότι το μηλικό οξύ είναι στερεό ενώ το αιθένιο αέριο. Εννοώ το μείγμα στερεού με αέριο… Αν είναι ρεαλιστικό …
Καλημέρα κυρίε Θοδωρή, ευχαριστώ πολύ για το σχόλιο! Πιστεύω πως σε ασκησιακο επίπεδο, μπορούμε να το θεωρήσουμε ένα ετερογενές μείγμα και να γίνουν κανονικά οι υπολογισμοί!
Τόνια καλησπέρα και Καλή Χρονιά. Θα ήθελα να δεις και μια άλλη προσέγγιση λύσης για την άσκησή σου. Ελπίζω να φανεί κάπου χρήσιμη.
Καλησπέρα σας κύριε Τσιλογιαννη! Καλή χρονιά να έχετε με υγεία! Σας ευχαριστώ πολύ για την παράθεση της δεύτερης λύσης.. πραγματικά πολύ ενδιαφέρουσα και διευρύνει την άσκηση!
Τόνια καλημέρα και καλή χρονιά με υγεία. Παραθέτω μια ενδεικτική λύση, έχοντας μια ένσταση στη διατύπωση: << η ποσότητα αυτή του υδρογονάνθρακα απαιτεί 0,2 mol HCl για πλήρη αντίδραση>>
Η μάζα του άνθρακα στο οξύ και στον υδρογονάνθρακα είναι ίση με τη μάζα του άνθρακα στο διοξείδιο του άνθρακα. Έτσι έχουμε:
mC(C4H6O5) + mC(CxHψ)= mC(CΟ2) => 4∙0,2∙12g + x∙a∙12g=1,2∙12g => x∙a=0,4
Επειδή το x είναι ακέραιος και ισχύει 1<x<4 θα είναι x=3 ή x=2.
1η περίπτωση: x=3 , οπότε a=(0,4/3).
Στο προπένιο προστίθενται μέχρι και (0,4/3)mol HCl.
C3H6 +HCl → C3H7Cl
Στο προπίνιο ή στο προπαδιένιο προστίθενται μέχρι και 2∙(0,4/3)mol HCl.
C3H4 +2HCl → C3H6Cl2
Απορρίπτονται γιατί δεν προστίθενται μέχρι 0,2 mol που δίνεται στην εκφώνηση.
2η περίπτωση: x=2 , οπότε a=0,2.
Στο αιθένιο προστίθενται μέχρι και 0,2mol HCl.
C2H4 +HCl → C2H5Cl
Στο αιθίνιο προστίθενται μέχρι και 0,4 mol HCl.
C2H2 +2HCl → C2H4Cl2 (δύο ισομερή λόγω Markovnikov)
Δεκτά και τα δύο!!! (Όταν σε 0,2mol αιθινίου προσθέσουμε 0,2mol HCl , το αιθίνιο αντιδρά πλήρως και παράγονται 0,2mol χλωρο-αιθένιου, έχουμε δηλαδή πλήρη αντίδραση.)
*** θα μπορούσε να ήταν: <<στη ποσότητα αυτή του υδρογονάνθρακα μπορούν να προστεθούν μέχρι και 0,2 mol HCl. >> Οπότε θα είχαμε μοναδική λύση το αιθένιο.
Ή
<στη ποσότητα αυτή του υδρογονάνθρακα μπορούν να προστεθούν 0,32 mol HCl.> Οπότε θα είχαμε μοναδική λύση το αιθίνιο.
Κύριε Παπαστεργιαδη καλημέρα σας και καλή χρονιά με υγεία! Σας ευχαριστώ πολύ για τον σχολιασμό και παράθεση της όμορφης ενδεικτικής λύσης! Προφανώς και όταν λέω απαιτεί για πλήρη αντίδραση εννοώ ότι είναι το μέγιστο που μπορεί να προστεθεί! Σας ευχαριστώ ωστόσο για την επισήμανση γιατί είναι έναυσμα αλλαγής στις διατυπώσεις για επόμενες αντίστοιχες αναρτήσεις!
Καλησπέρα Τόνια. Από ένα συνταξιούχο πλέον καθηγητή, αν θες ακούς μια συμβουλή σχετικά με προτεινόμενα θέματα. Πρέπει να έχουν ακρίβεια, σαφήνεια και επιστημονική εγκυρότητα. Καμμιά σημασία ΔΕΝ έχει τι εννοεί ο συγγραφέας, αλλά τι παρουσιάζει η άσκηση!
Σχετικά με το <πλήρη αντίδραση> σου θυμίζω ερώτημα από τις πανελλήνιες εξετάσεις του 2023.
Δ2. Τα 3 g προπανόλης (C3H7OH) οξειδώνονται πλήρως με 70 mL υδατικού
διαλύματος K2Cr2O7 συγκέντρωσης 1/3 Μ, παρουσία H2SO4, και σχηματίζεται
μίγμα αλδεΰδης και οξέος. Να υπολογίσετε το ποσοστό μετατροπής της προπανόλης σε οξύ.
Σχετικά με την αξιολόγηση κάθε ενδεικτικής λύσης δεν εξετάζουμε μόνο το αποτέλεσμα αν είναι σωστό, στην άσκησή σου το αιθένιο, αλλά εξετάζουμε ΟΛΗ την πορεία με βάση την οποία καταλήγουμε στην απάντηση. Αναφερόμενος στην ενδεικτική λύση του κύριου Τσιλογιάννη η απάντηση είναι σωστή, η πορεία με βάση την οποία καταλήγουμε στην απάντηση στηρίζεται στο δεδομένο ότι η τελική ποσότητα του CxHωClλ είναι 0,2 mol!!! . Αυτό δεν υπάρχει στην εκφώνηση. Με βάση δε την χημική εξίσωση που παρουσιάζει , η τελική ποσότητα του CxHωClλ έπρεπε να ήταν a mol και όχι 0,2 mol. Προφανώς λανθασμένη παρουσίαση.
Η σωστή απάντηση βγαίνει συμπωματικά! Φαντάσου την ίδια ακριβώς άσκηση με μοναδική αλλαγή τα 0,2 mol σε 0,4 mol. Η προτεινόμενη αντιμετώπιση θα έδινε x=1, που είναι αδύνατον! Μια σωστή όμως αντιμετώπιση..
(ποσότητα/mol) CxHψ + λHCl→ CχH(ψ+λ)Clλ
Αντ./παρ a aλ a
Τότε aλ=0,4. Οπότε για λ=1 => a=0,4 και λόγω(1) x=1 απορρίπτεται
Για λ=2 => a=0,2 και λόγω(1) x=2 και επειδή 2x+2=ψ+2λ =>4+2=ψ+4=>ψ=2.
Μ.Τ: C2H2 (αιθίνιο)
Για λ=3 => a=0,4/3 και λόγω(1) x=3 απορρίπτεται . Σε τρείς άνθρακες δεν υπάρχουν διπλός και τριπλός δεσμός.
Για λ≥4 => a≤0,1και λόγω(1) x≥4 απορρίπτεται
Κύριε Παπαστεργιαδη φυσικά και οι συμβουλές σας είναι χρήσιμες και προσωπικά τις λαμβάνω υπόψιν! Πολύ εύστοχο το παράδειγμα των πανελληνίων!