-
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Επηρεάζει η διατροφή το DNA μας; πριν από 1 μέρα, 12 ώρες
Για λόγους περιεκτικής παρουσίασης στο δίκτυο στο κείμενο που αντέγραψα εγραψα ορισμένα βασικά σημεία του άρθρου.. Ωστόσο πατώντας στο λινκ μπορείτε να το διαβάσετε ολόκληρο
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 1 μέρα, 12 ώρες
Επηρεάζει η διατροφή το DNA μας;
 Μια χημικός τροφίμων εξηγεί: Η διατροφή και το DNA συνδέονται πολύ πιο βαθιά απ’ όσο πιστεύαμε μέχρι σήμερα. Κάθε γεύμα λειτουργεί σαν ένα βιολογι […]
Μια χημικός τροφίμων εξηγεί: Η διατροφή και το DNA συνδέονται πολύ πιο βαθιά απ’ όσο πιστεύαμε μέχρι σήμερα. Κάθε γεύμα λειτουργεί σαν ένα βιολογι […] -
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Άσκηση καύσης, μαθηματικές μεταβλητές και αλογονοφορμικη αντίδραση πριν από 1 εβδομάδα
Πραγματοποίησα( και με πρόταση συναδέλφου)μία παραλλαγή -διαφορετική εκφώνηση στην άσκηση
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 1 εβδομάδα, 1 μέρα
Άσκηση καύσης, μαθηματικές μεταβλητές και αλογονοφορμικη αντίδραση
 Μία κορεσμένη οργανική ένωση περιέχει στο μόριο της άνθρακα ( C) ,υδρογόνο (H) και ένα άτομο οξυγόνου (O). Διαθέτουμε ποσότητα μάζας ίση με 3ω mol από τ […]
Μία κορεσμένη οργανική ένωση περιέχει στο μόριο της άνθρακα ( C) ,υδρογόνο (H) και ένα άτομο οξυγόνου (O). Διαθέτουμε ποσότητα μάζας ίση με 3ω mol από τ […] -
Ο/Η Τόνια Βουδούρη άλλαξε φωτογραφία προφίλ πριν από 1 εβδομάδα, 1 μέρα
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 1 εβδομάδα, 4 μέρες
-
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Χρόνια πολλά και όμορφα για το 2026 πριν από 3 εβδομάδες, 2 μέρες
Χρόνια σας πολλά!!!!!
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 3 εβδομάδες, 4 μέρες
Η αλκοόλη της Χημικής Ισορροπίας σε μία αλυσίδα αντιδράσεων
 Μία συνδυαστική άσκηση ,η οποία χρησιμοποιεί την αλκοόλη της Χημικής Ισορροπίας της εστεροποίησης σε μία σειρά οργανικών και ανόργανων αντιδράσεων ,”παίζ […]
Μία συνδυαστική άσκηση ,η οποία χρησιμοποιεί την αλκοόλη της Χημικής Ισορροπίας της εστεροποίησης σε μία σειρά οργανικών και ανόργανων αντιδράσεων ,”παίζ […] -
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Συγκέντρωση ή Αριθμητική Τιμή [Η3Ο+] σε mol/L πριν από 1 μήνα
Κύριε Μάργαρη σας ευχαριστώ πολύβγια τον χρήσιμο σχολιασμό και εμπλουτισμό!! Κύριε Τσιλογιαννη ομοίως σας ευχαριστώ πολύ και θα μελετήσω αυτό που παραθέσατε!!
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 1 μήνα
Συγκέντρωση ή Αριθμητική Τιμή [Η3Ο+] σε mol/L
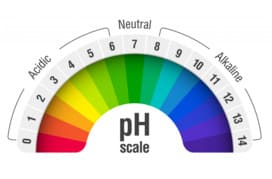 Καλησπέρα σας και χρόνια πολλά με υγεία και ευλογία! Επειδή θεωρώ πολύ σημαντική μία παρατήρηση που μου διατυπώθηκε σε ανάρτηση από τον Χημικό κύριο Θωμά […]
Καλησπέρα σας και χρόνια πολλά με υγεία και ευλογία! Επειδή θεωρώ πολύ σημαντική μία παρατήρηση που μου διατυπώθηκε σε ανάρτηση από τον Χημικό κύριο Θωμά […]-
Καλησπέρα και χρόνια πολλά Τόνια.
Επιτέλους και ένα ερώτημα στο φόρουμ της Χημείας!
Οπότε δεν μένει παρά να απαντήσω άμεσα 🙂
Όσον αφορά την ουσία του ερωτήματος, προφανώς έτσι είναι, αφού ο λογάριθμος ορίζεται μόνο για καθαρούς (αδιάστατους) αριθμούς.
Συνεπώς οπουδήποτε στην επιστήμη χρησιμοποιούμε λογαρίθμους ή θα είναι λογάριθμος πηλίκου ομοειδών μεγεθών π.χ. το έργο σε μια ισόθερμη μεταβολή, είτε “σιωπηλα” μιλάμε για λογάριθμο συγκέντρωσης, παίρνοντας το λογάριθμο της αριθμητικής τιμής του μεγέθους και “ξεχνάμε” τις μονάδες.
Σκέψου να θέλουμε το pH διαλύματος 0,01Μ και κάποιος να γράψει:
pH=-log{H+)=-log(0,01M)=-log0,01- logM=2-logM και να ψάχνει το δεκαδικό λογάριθμο της μονάδας Molarity… -
Τόνια καλησπέρα και χρόνια πολλά.
Συμπληρώνοντας αυτά που γράφει ο Διονύσης, να αναφέρω ότι σύμφωνα με την IUPAC pH = -lg(α(Η+)) όπου α(Η+) η ενεργότητα των κατιόντων υδρογόνου που είναι αδιάστατο μέγεθος.
Επίσης στην 2η έκδοση του Quantities, Units and Symbols in Physical Chemistry της IUPAC είχε μια εναλλακτική διατύπωση: pH = -lg (cH+)/(molXdm-3), δηλ. διαιρεί τη συγκέντρωση των κατιόντων υδρογόνου με τη μονάδα μέτρησης της συγκέντρωσης (mol/L ή mol/dm-3) έτσι ώστε να υπάρχει στον λογάριθμο αδιάστατο μέγεθος.
Για περισσότερες πληροφορίες μπορείς να ανατρέξεις στο άρθρο “Covington, A.K., Bates, R.G. and Durst, R.A., Definition of pH Scales, Standard Reference
Values, Measurement of pH and Related Terminology, Pure Appl. Chem. 57 (1985) 53 1—542.” το οποίο είναι ελεύθερα διαθέσιμο. -
Κύριε Μάργαρη σας ευχαριστώ πολύβγια τον χρήσιμο σχολιασμό και εμπλουτισμό!! Κύριε Τσιλογιαννη ομοίως σας ευχαριστώ πολύ και θα μελετήσω αυτό που παραθέσατε!!
-
-
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Easter Bunny – Chem Edition πριν από 1 μήνα, 1 εβδομάδα
Σας ευχαριστω πολύ!! Καλές γιορτές με υγεία και ευλογία!!
Εννοείται η εικόνα και ο τίτλος διαλεχθηκαν με μεγάλη προσοχή! -
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 1 μήνα, 1 εβδομάδα
Easter Bunny – Chem Edition
 Αέριο μείγμα δύο αλκενίων -Καύση- Υδραλογόνωση Ένα αέριο μείγμα περιέχει δύο αλκένια για τα οποία ισχύει V1=V2 όπου V1, V2 οι όγκοι των δύο α […]
Αέριο μείγμα δύο αλκενίων -Καύση- Υδραλογόνωση Ένα αέριο μείγμα περιέχει δύο αλκένια για τα οποία ισχύει V1=V2 όπου V1, V2 οι όγκοι των δύο α […] -
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Μη συμμετρικό αλκίνιο και αντίδραση με μεταλλικό Κάλιο πριν από 1 μήνα, 2 εβδομάδες
Καλησπέρα σας κύριε Παπαστεργιαδη,σας ευχαριστώ πολύ! Επαναδιατύπωσα την πρόταση με την αλκοόλη ώστε να μην φαίνεται σαν κάτι που πραγματοποιήθηκε! Σχετικά με τα προϊόντα ενυδάτωσης, καθώς δεν έδωσα ποσοτικά δεδομένα φτιάχνοντας την άσκηση έλαβα υπόψιν πως υπάρχουν δύο περιπτώσεις είτε να είναι κύριο/ δεύτερον- που προκύπτει από αλκινια με όξινο…[Περισσότερα]
-
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Μη συμμετρικό αλκίνιο και αντίδραση με μεταλλικό Κάλιο πριν από 1 μήνα, 2 εβδομάδες
Κύριε Παπαστεργιαδη σας ευχαριστώ πάρα πολύ! Για να είναι πιο διακριτικό και να μην εμπλακεί το αλκινιο( ώστε να αποκλειστεί η περίπτωση που είπατε)εκανα μια αλλαγή στην εκφώνηση, αναφέροντας αντίδραση μόνο αλκοόλης- SOCl^2 και όχι με όλο το μείγμα.Καλο σας βράδυ!!
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 1 μήνα, 2 εβδομάδες
Μη συμμετρικό αλκίνιο και αντίδραση με μεταλλικό Κάλιο
 Διαθέτουμε ένα ισομοριακό μείγμα μάζας m=10 g που περιέχει μία (άκυκλη) κορεσμένη μονοσθενή αλκοόλη και ένα (άκυκλο) αλκίνιο. Εαν εκθέταμε την […]
Διαθέτουμε ένα ισομοριακό μείγμα μάζας m=10 g που περιέχει μία (άκυκλη) κορεσμένη μονοσθενή αλκοόλη και ένα (άκυκλο) αλκίνιο. Εαν εκθέταμε την […]-
Καλησπέρα Τόνια και πολλά-πολλά μπράβο για τίς ιδέες σου. Γράφω μια άλλη εκφώνηση, γιατί πιστεύω αρχικά ότι το παραγόμενο HCl δεσμεύεται όλο από το υπάρχον αλκίνιο. Τότε το HCl τελικά δεν παράγεται.
ΑΣΚΗΣΗ: Σε 10g υγρού ισομοριακού μείγματος , που αποτελείται από μία (άκυκλη) κορεσμένη μονοσθενή αλκοόλη Α και ένα (άκυκλο) αλκίνιο Β, προσθέτουμε 0,21 mol SOCl2. Τελικά ελευθερώνεται 0,1 mol ανόργανου αερίου.
Να γράψετε τις χημικές εξισώσεις των αντιδράσεων, που πραγματοποιήθηκαν, με τη χρήση του γενικού μοριακού τύπου για τις ενώσεις των Α και Β.
Να γράψετε τους (συνεπτυγμένους) συντακτικούς τύπους των Α και Β, αν γνωρίζετε ότι η προσθήκη της ένωσης Β σε υδατικό διάλυμα Hg/ H2SO4 έχει ως αποτέλεσμα την παραγωγή δύο ενώσεων, οι μάζες των οποίων είναι περίπου ίσες μεταξύ τους.
Δίνονται: Ar(H)=1, Ar(C)=12, Ar(O)=16.
Ενδεικτική λύση:
(n/mol) CνH2ν+1OH + SOCl2 → CνH2ν+1Cl + SO2 + HCl
αντ./παρ. x x x x x
(n/mol) CμH2μ-2 + HCl → CμH2μ-1Cl
αντ./παρ. x x x
To αέριο που ελευθερώθηκε είναι το SO2, συνεπώς x=0,1.
Mr(A) =14ν+18=> (m/n)= [(14ν+18)g/1mol]=>m(A)= 0,1(14ν+18)g
Mr(B) =14μ -2=> (m/n)= [(14μ -2)g/1mol]=>m(A)= 0,1(14μ -2)g
m(μείγματος)= m(A) + m(B) =>10=0,1(14ν+18)+ 0,1(14μ -2)=> ν+ μ=6.
Για να παραχθούν δύο ισομερείς κετόνες περίπου με αναλογία μαζών 1:1, πρέπει οι άνθρακες του τριπλού δεσμού να ενώνονται με διαφορετικά αλκύλια, αφού στα ίδια συντακτικά αλκύλια παράγεται μοναδικό προϊόν. Επειδή μ<6 έχουμε μοναδική λύση: μ=5 και ν=1.
Συνεπώς Α: CH3OH και Β: CH₃–C≡C–CH₂–CH₃. -
Κύριε Παπαστεργιαδη σας ευχαριστώ πάρα πολύ! Για να είναι πιο διακριτικό και να μην εμπλακεί το αλκινιο( ώστε να αποκλειστεί η περίπτωση που είπατε)εκανα μια αλλαγή στην εκφώνηση, αναφέροντας αντίδραση μόνο αλκοόλης- SOCl^2 και όχι με όλο το μείγμα.Καλο σας βράδυ!!
-
Τόνια καλημέρα! Επαναλαμβάνω ότι η/ο συγγραφέας έχει ΠΑΝΤΑ τον πρώτο λόγο.
Έρχομαι σε πολύ δύσκολη θέση όταν δημόσια πρέπει να γράψω, ότι σε κάτι δεν συμφωνώ. Πολλές φορές αντιπροτείνω την ίδια άσκηση ως νέα και πάντα γράφω την ενδεικτική λύση, που κατά την γνώμη μου βαθμολογείται με άριστα. Αυτό διευκολύνει, σε ένα πιθανό διαγώνισμα, τον βαθμολογητή. Δίνω έτσι την δυνατότητα και στην/στον συγγραφέα να συγκρίνει τις δύο λύσεις. Όταν π.χ η προτεινόμενη άσκησή σου αξιολογείται με 12 μονάδες, αυτές επιμερίζονται, στις απαραίτητες αντιδράσεις και στους απαραίτητους υπολογισμούς. Όταν εσύ παρουσιάζεις στην λύση διερεύνηση και αντίδραση που δεν χρειάζεται , πως θα γίνει η επι μέρους βαθμολόγηση; (Η αλκοόλη που είναι 0,1 mol με περίσσεια Κ ελευθερώνει 0,05 mol H2. Συνεπώς δεν εξετάζω τι είναι το αλκίνιο, γιατί ήδη γνωρίζω ότι δεν έχει όξινο υδρογόνο.
Όταν εσύ γράφεις :
CνΗ2ν+1ΟΗ + SOCl2 → CνΗ2ν+1Cl + SO2 + HCl
a mol a mol a mol
χωρίς να αναφέρεις αν τα mol του καθένα είναι τα αρχικά; Είναι τα τελικά; Είναι παραγόμενα;… Και εγώ γράφω :
(n/mol) CνH2ν+1OH + SOCl2 → CνH2ν+1Cl + SO2 + HCl
αντ./παρ. x x x x x
Πρέπει να αξιολογηθούμε με τον ίδιο βαθμό;
Ο βαθμολογητής που βλέπει :
Ισχύει :2a mol = 0,2 mol
a =0,1 mol
Πρέπει να το θεωρήσει σωστό;;; (από την πρώτη ισότητα μετα από απλοποίηση προκύπτει : 2a=0,2=>a=0,1!!!)
Αν αυτό το έγραφες μόνο εσύ ΔΕΝ θα έλεγα τίποτε. Υπάρχουν όμως πολλοί-πολλοί, που ίσως αγνοούν το σύμβολο της ισότητας ή δεν αντιλαμβάνονται την έννοια της αντικατάστασης ή…( a=0,1mol ΔΗΛΩΝΕΙ στην λύση ότι η ποσότητα είναι ίση με 0,2 mol∙mol!!! H ποσότητα ουσίας ή κατ’ εμέ η ποσότητα μάζας είναι θεμελιώδες μέγεθος στο S.I με αντίστοιχη μονάδα το mol και ΟΧΙ το mol∙mol )Η κάθε εκφώνηση πρέπει να <μυρίζει> χημεία. Δηλαδή να σε παραπέμπει σε πειράματα που γίνονται και δεν είναι ΧΑΡΤΟΧΗΜΕΙΑ.
Η έκφραση< Εάν εκθέσουμε την ποσότητα της αλκοόλης που περιέχεται στο μείγμα σε περίσσεια SOCl2 παράγονται 0,2 mol….> με την έκφραση< Εάν εκθέταμε όλη την ποσότητα της αλκοόλης που περιέχεται στο μείγμα σε περίσσεια SOCl2 θα παράγονται 0,2 mol….> ΔΕΝ είναι ισοδύναμη!Στην πρώτη δηλώνουμε ότι το πείραμα έγινε. Αυτό σημαίνει ότι όλη η αλκοόλη χρησιμοποιήθηκε, κάτι που έχει ως αποτέλεσμα στη συνέχεια να μην υπάρχει!
Θα μπορούσε να ήταν: Όταν σε ποσότητα αλκοόλης, ίση με αυτή που περιέχεται στο μείγμα προσθέσουμε 0,27 mol SOCl2…….
Χημική παρατήρηση:
Η ενυδάτωση αλκινίου γίνεται παρουσία καταλυτών.
<Η ενυδάτωση του αλκινίου παρουσία καταλυτών, έχει ως αποτέλεσμα την παραγωγή δύο ενώσεων , οι οποίες έχουν περίπου ίση μάζα> από μόνη της σου δηλώνει ότι το αλκίνιο δεν έχει όξινο υδρογόνο!
-
Καλησπέρα σας κύριε Παπαστεργιαδη,σας ευχαριστώ πολύ! Επαναδιατύπωσα την πρόταση με την αλκοόλη ώστε να μην φαίνεται σαν κάτι που πραγματοποιήθηκε! Σχετικά με τα προϊόντα ενυδάτωσης, καθώς δεν έδωσα ποσοτικά δεδομένα φτιάχνοντας την άσκηση έλαβα υπόψιν πως υπάρχουν δύο περιπτώσεις είτε να είναι κύριο/ δεύτερον- που προκύπτει από αλκινια με όξινο Η -είτε να είναι σε ίδια αναλογία μάζας.Ετσι το σκέφτηκα και το προσέγγισα εγώ τουλάχιστον για αυτό έκανα και την διερεύνηση. Ωστόσο προσέθεσα μια σημείωση στην άσκηση για να είναι διακριτό πως λαμβάνουμε υπόψιν και τα δύο ενδεχόμενα
-
Τόνια σε χαιρετώ και πάλι. Πως αντιμετωπίζω την ενυδάτωση αλκινίου.
Κάθε συμμετρικό αλκίνιο δίνει μοναδικό προϊόν.
Για το μη συμμετρικό αλκίνιο έχουμε δύο περιπτώσεις.
Ι. Τα δύο άτομα C του τριπλού δεσμού να ενώνονται το ένα με Η και το άλλο με C (1-αλκίνιο). Τότε έχουμε κύριο και δευτερεύον προϊόν.( περίπου 85% – 15%)
ΙΙ. Τα δύο άτομα C του τριπλού δεσμού να ενώνονται με διαφορετικά αλκύλια. Τότε έχουμε δύο προϊόντα με σχεδόν ίδια ποσοστά, όχι όμως ίσα. Την απάντηση ΔΕΝ τη δίνει , όπως διατυπώνεται στο σχολικό βιβλίο ο κανόνας του Markovnikov. Στο πανεπιστήμιο γνωρίζουμε ότι παίζουν ρόλο τα αλκύλια. Π.χ η προσθήκη HCl στο 2-πεντένιο έχει ως αποτέλεσμα την παραγωγή δύο προϊόντων (2-χλωροπεντάνιο και 3-χλωροπεντάνιο) περίπου με το ίδιο ποσοστό, όχι όμως με 50% – 50%.
-
-
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Υδρόλυση Εστέρα και Ιοντισμός Οξέος πριν από 1 μήνα, 2 εβδομάδες
Κύριε Παπαστεργιαδη σας ευχαριστώ πολύ και πάλι για όλα! Οι επισημάνσεις σας είναι πολύ σημαντικές γιατί συμβάλλουν στην διόρθωση λαθών και επεκτείνουν τις γνώσεις γύρω από το θέμα! Πολύ όμορφη η άσκηση σας !
-
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Υδρόλυση Εστέρα και Ιοντισμός Οξέος πριν από 1 μήνα, 2 εβδομάδες
Κύριε Παπαστεργιαδη καλημερα σας . Σας ευχαριστω πολυ ! Αρχικα οσον αφορα στην προταση με τις δυο ισορροπιες ενεμπιμπτε στον τιτλο και οχι στο περιεχομενο της ασκησης ( το εγραψα γιατι θεωρησα πως ηταν μια ομορφη προταση για να συνδεσει τις δυο αντιδράσεις χρησιμοποιωντας σχετικες εννοιες ,παροτι δεν δινονται με αριθμητικο τροπο στα…[Περισσότερα]
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 1 μήνα, 3 εβδομάδες
Υδρόλυση Εστέρα και Ιοντισμός Οξέος
 Διαθέτουμε εστέρα με ποσότητα μάζας n=a mol και μάζα m=102 x g . Ο εστέρας αυτός υδρολύεται με την επίδραση νερού υπό τις κατάλληλες συνθήκες ,με αποτέλ […]
Διαθέτουμε εστέρα με ποσότητα μάζας n=a mol και μάζα m=102 x g . Ο εστέρας αυτός υδρολύεται με την επίδραση νερού υπό τις κατάλληλες συνθήκες ,με αποτέλ […]-
Τόνια καλή σου μέρα! Ως ιδέα ΑΡΙΣΤΑ. Να συνδέσω μια χημική ισορροπία που έχω στην υδρόλυση, με μια άλλη χημική ισορροπία που έχω στον ιοντισμό του ασθενούς οξέος. Στο δια ταύτα όμως αυτό δεν γίνεται στην άσκηση. Δίνεις μάζα και ποσότητα μάζας του εστέρα, χωρίς να δώσεις δεδομένα για την υδρόλυση. ΦΥΣΙΚΑ και είναι ΔΙΚΑΙΩΜΑ σου , αλλά η άσκηση δεν συνδέει τις δύο ισορροπίες. Δική σου επιλογή!
Η λύση που δίνεις είναι λανθασμένη! Ενώ κάνεις <την γνωστή προσέγγιση>
C- [H3O+]=C , στη συνέχεια καταλήγεις ότι C= [H3O+]!!!
Αν θέλεις να κρατήσεις την άσκηση πρέπει [H3O+]=χ/8 (δεν ξέχασα τη μονάδα Μ, αλλά το [H3O+] είναι η αριθμητική τιμή της συγκέντρωσης των οξωνίων σε Μ, οπότε είναι καθαρός αριθμός). Η γνωστή προσέγγιση εδώ δεν γίνεται. Έτσι
Κα=[H3O+]∙ [H3O+]/(C- [H3O+])=> C=2∙ [H3O+]
Στην πράξη η γνωστή προσέγγιση γίνεται μόνο στον υπολογισμό των οξωνίων. Δεν υπολογίζουμε τα οξώνια από τον αυτοϊοντισμό του νερού. -
Κύριε Παπαστεργιαδη καλημερα σας . Σας ευχαριστω πολυ ! Αρχικα οσον αφορα στην προταση με τις δυο ισορροπιες ενεμπιμπτε στον τιτλο και οχι στο περιεχομενο της ασκησης ( το εγραψα γιατι θεωρησα πως ηταν μια ομορφη προταση για να συνδεσει τις δυο αντιδράσεις χρησιμοποιωντας σχετικες εννοιες ,παροτι δεν δινονται με αριθμητικο τροπο στα δεδομενα ) .Ωστοσο την εσβησα. Σας ευχαριστω πολυ για την δευτερη επισημαναση την οποια διορθωσα και στην εκφωνηση και στο drive …εχετε απολυτο δικιο . Επίσης σταθηκα πολυ στην αναφορα σας για την μοναδα στην συγκεντρωση των οξωνιων . Πραγματι το [ Η3ο+] ειναι αριθμητικη τιμή και όχι συγκέντρωση οπως συνηθιζεται αφού στο -logpH χρησιμοποιείται μονο με αριθμητικη τιμη αλλιως θα λεγαμε και -logM .
Σας ευχαριστω πολυ και παλι και χαιρομαι που σας αρεσε και η ιδεα! -
Τόνια και πάλι σε χαιρετώ! Συνέχισε να προσπαθείς και μην σε απογοητεύει ένα λάθος. Άλλωστε < όποιος πλένει πιάτα, σπάει πιάτα, <λέει> ο πάνσοφος λαός. Το πολύ- πολύ θετικό σε εσένα είναι, ότι αντιλαμβάνεσαι το λάθος και το αναγνωρίζεις. Συνέχισε πιο ΔΥΝΑΤΑ!
Άσκηση <κλεμμένη> από την αρχική σου επιθυμία.
Αλκοόλη Α(CνH2ν+2O) προστίθεται σε υδατικό διάλυμα ΚΟΗ/Ι2, χωρίς στη συνέχεια να καταβυθίζεται κίτρινο ίζημα.
Οξύ Β (CμH2μΟ2) συνολικής μάζας 3mg διαλύεται σε νερό, οπότε δημιουργείται διάλυμα όγκου 2,5 L, για το οποίο ισχύει pKa(B)=pH=5.
1. Nα γράψετε τον (συνεπτυγμένο) συντακτικό τύπο του οξέος Β.
Δημιουργούμε ισομοριακό μείγμα του οξέος Β και της αλκοόλης Α, συνολικής μάζας 180g, μέσα σε κενό δοχείο. Μετά από χρόνο, το σύστημα καταλήγει σε ισορροπία σύμφωνα με την αντίδραση: Β + Α ⇌ εστέρας (Ε) +νερό , με Κc=4.
Τελικά στο δοχείο υπήρχαν σε ισορροπία 30g οξέος Β, εκτός των άλλων ουσιών.
2. Nα γράψετε τον (συνεπτυγμένο) συντακτικό τύπο του εστέρα Ε.
Δίνονται: Αr(H)=1, Αr(C)=12, Αr(O)=16.
Υπενθύμιση: Για δύο ρητούς αριθμούς κ, λ μπορούμε να δεχθούμε ότι
κ +λ =κ , αρκεί να ισχύει: λ< 0,1κ.
Ενδεικτική απάντησηΓια κάθε μονοβασικό οξύ ΗΑ συγκέντρωσης C M, με βάση τον ιοντισμό του, προκύπτει ο παρακάτω πίνακας τιμών:
(συγκέντρωση/Μ) ΗΑ +Η2Ο ⇌ A- + H3O+
αρχικά C
αντ./παρ. X X X
Χ.Ι C-X X X
(Αφού pH=5 , δεν συνυπολογίζονται τα οξώνια του νερού, γιαυτό και στα αρχικά δεν γράφω αριθμητική τιμή για τα οξώνια)
Ισχύει η σχέση: Κα=[Η3Ο+]∙[Α-]/[ΗΑ] ,οπότε με αντικατάσταση αρχικά έχουμε:
χ=χ∙ χ/(C-x) => C-x=x =>C=2x. Άρα C(HA)=2∙10-5M, αφού pH=5.
Όμως C(HA)= n(HA)/ V(HA)=> n(HA) =2∙10-5M∙2,5L=0,05mmol.
m(HA)= n(HA)∙ Mr(HA)g/mol =>3mg=0,05mmol∙ Mrg/mol=> Mr=60.
Έτσι 12μ+2μ+2∙16=60 => μ=2. Επομένως Σ.Τ(Β): CH3COOH.Με βάση την εστεροποίηση , προκύπτει ο παρακάτω πίνακας τιμών:
(ποσότητα/mol) Α + B ⇌ E + Η2Ο
αρχικά n n
αντ./παρ. ω ω ω ω
Χ.Ι n-ω n-ω ω ω
Ισχύει: Κc=[E][H2O]/[A][B] και Vδιαλύματος=V L . Τότε
4=(ω/V) (ω/V)/[[(n-ω)/V]∙[(n-ω)/V]] και επειδή 0<ω<n καταλήγουμε:
2=ω/(n-ω)=> 2n=3ω (1)
Επίσης nB(X.I)=(30/60)mol=0,5mol=(n-ω)mol=>(1/2)=n-ω=>1=2n-2ω , οπότε λόγω (1) 1=3ω-2ω =>ω=1 και n=1,5.
mΒ(αρχ)=1,5∙60g=90g. Συνεπώς mΑ(αρχ)=(180-90) g=90g => 1,5∙ΜrA=90
=>14ν+18=60 =>ν=3. Μ.Τ(Α):C3H8O . Αυτόν το μοριακό τύπο τον έχουν και δύο αλκοόλες . Η 1-προπανόλη , η οποία δεν δίνει την αλογονοφορμική αντίδραση και η 2-προπανόλη , η οποία δίνει την αλογονοφορμική αντίδραση. Τελικά
Σ.Τ(Ε):CH3COOCH2CH2CH3
-
Κύριε Παπαστεργιαδη σας ευχαριστώ πολύ και πάλι για όλα! Οι επισημάνσεις σας είναι πολύ σημαντικές γιατί συμβάλλουν στην διόρθωση λαθών και επεκτείνουν τις γνώσεις γύρω από το θέμα! Πολύ όμορφη η άσκηση σας !
-
-
H/o Τόνια Βουδούρη έγραψε ένα νέο άρθρο πριν από 2 μήνες
H Βιταμίνη C- Vol.3
 Διαθέτουμε έναν χυμό πορτοκαλιού (χυμός 1) συγκέντρωσης C1 σε βιταμίνη C ( ασκορβικό οξύ) και ένα χυμό πορτοκαλιού (χυμός 2) συγκέντρωσης C2 σε βιταμί […]
Διαθέτουμε έναν χυμό πορτοκαλιού (χυμός 1) συγκέντρωσης C1 σε βιταμίνη C ( ασκορβικό οξύ) και ένα χυμό πορτοκαλιού (χυμός 2) συγκέντρωσης C2 σε βιταμί […] -
Ο/η Τόνια Βουδούρη σχολίασε το άρθρο Συνδυάζοντας δύο τιμές pH σε μία άσκηση οργανικής πριν από 2 μήνες
Σε ευχαριστώ πάρα πολύ Παναγιώτη και σε σένα το ίδιο για τις όμορφες αναρτήσεις σου !
- Φόρτωσε Περισσότερα

Για λόγους περιεκτικής παρουσίασης στο δίκτυο στο κείμενο που αντέγραψα εγραψα ορισμένα βασικά σημεία του άρθρου.. Ωστόσο πατώντας στο λινκ μπορείτε να το διαβάσετε ολόκληρο