 Σε ορισμένα συγγράμματα αναφέρεται ότι:
Σε ορισμένα συγγράμματα αναφέρεται ότι:
<< Όταν η θέση μιας Χ.Ι. μετατοπίζεται δεξιά, τότε η απόδοση της αντίδρασης αυξάνεται και όταν η θέση μιας Χ.Ι. μετατοπίζεται αριστερά, τότε η απόδοση της αντίδρασης μειώνεται . >>
Η παραπάνω πρόταση, που κατέστη δυστυχώς και αυτή στερεότυπο δεν ισχύει πάντα όπως αποδεικνύεται στις παρακάτω ασκήσεις.
Άσκηση 1η
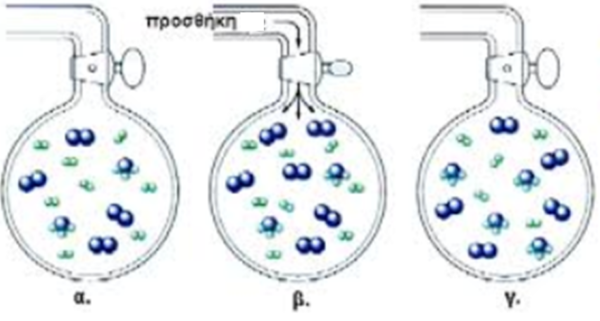
Σε δοχείο Δ1 όγκου VL στους θοC διαβιβάζονται 1mol Α(g) , 2mol Β(g) και αποκαθιστάται η χημική ισορροπία Α2(g) + Β2(g) ↔ 2ΑΒ(g) για την οποία Κc = 4.
Στο δοχείο Δ1 στους θοC διαβιβάζονται 1mol Α οπότε αποκαθιστάται νέα χημική ισορροπία.
Βρείτε την απόδοση της αντίδρασης στις δυο παραπάνω περιπτώσεις και σχολιάστε τα αποτελέσματα.
Λύση:
Α2(g) + Β2(g) ↔ 2ΑΒ(g)
1-x 2-x 2x
Κc= 4 = 4×2 / (1-x) (2-x) =>= x=2/3 και α=(2/3)/1= 2/3 =>
Α= 66,66%.
Προσθέτοντας 1mol Α η θέση της Χ.Ι. μετατοπίζεται δεξιά οπότε
Α2(g) + Β2(g) ↔ 2ΑΒ(g)
1η Χ.Ι 1/3 4/3 4/3
Προσθέτω 1 – –
Αντ/παρ. -y -y +2y
Τελικα. 4/3-y 4/3-y 4/3+2y
Κc = 4 = (4/3+2y) 2 / (4/3-y)2 => y = 1/3 και α=(2/3+1/3)/2= 1/2 => Α= 50%.
Mια πιο εύκολη λύση είναι η έξης:
Θεωρώ ότι με την προσθήκη του 1mol Α είναι σαν να ξεκινάμε με 2mol Α(g) και 2mol Β(g)
Α2(g) + Β2(g) ↔ 2ΑΒ(g)
2-x 2-x 2x
και καταλήγουμε 4= 4×2/ (2-x)2 => x=1 και α=1/2=0,5 => Α= 50%.
Άσκηση 2η
Σε δοχείο Δ1 όγκου VL στους θοC διαβιβάζονται 2mol Α(g) , 2mol Β(g) και αποκαθιστάται η χημική ισορροπία
Α2(g) + Β2(g) ↔ 2ΑΒ(g) για την οποία Κc = 4.
Από το δοχείο Δ1 στους θοC αφαιρούμε κατάλληλα 1mol Α οπότε αποκαθίσταται νέα χημική ισορροπία.
Βρείτε την απόδοση της αντίδρασης στις δυο παραπάνω περιπτώσεις και σχολιάστε τα αποτελέσματα.
Λύση
Α2(g) + Β2(g) ↔ 2ΑΒ(g)
2-x 2-x 2x
και καταλήγουμε 4= 4×2/ (2-x)2 => x=1 και α=1/2=0,5 => Α= 50%.
Με την αφαίρεση του 1mol Α η ισορροπία μετατοπίζεται αριστερά, άρα σύμφωνα με το στερεότυπο πρέπει να βγάλουμε μικρότερη απόδοση.
Οψόμεθα:
Θεωρώ ότι με την αφαίρεση του 1mol Α είναι σαν να ξεκινάμε με 1mol Α(g) και 2mol Β(g)
Α2(g) + Β2(g) ↔ 2ΑΒ(g)
1-x 2-x 2x
Κc= 4 = 4×2 / (1-x) (2-x) =>= x=2/3 και α=(2/3)/1= 2/3 => Α= 66,66%.
H απόδοση αντίθετα με το στερεότυπο βγήκε μεγαλύτερη.
Στην ιοντική ισορροπία στην αραίωση και τη συμπύκνωση των διαλυμάτων των ασθενών ηλεκτρολυτών , είναι προφανέστατο όπως θα δούμε στο αντίστοιχο κεφάλαιο ότι δεν ισχύει η παραπάνω πρόταση ( στερεότυπο)
![]()
Πολύ ωραία Παύλο. Καλή χρονιά. Στους μαθητές μου Παύλο, θέλοντας να επισημάνω σημεία του θέματος που θίγεις, δίνω το ακόλουθο κείμενο:
"Όταν η θέση της χημικής ισορροπίας μετατοπίζεται προς τα δεξιά λόγω μεταβολής της πίεσης ή της θερμοκρασίας, τότε η απόδοση της αντίδρασης πάντα αυξάνεται.
Όταν όμως η ισορροπία μετατοπίζεται προς τα δεξιά λόγω αύξησης της συγκέντρωσης κάποιου αντιδρώντος, σε κάποιες περιπτώσεις η απόδοση δεν αυξάνεται.
Για παράδειγμα, στις αντιδράσεις που έχουμε μόνο ένα αντιδρών:
i) Aν με μετατόπιση της ισορροπίας προς τα δεξιά αυξάνονται τα συνολικά moles των σωμάτων που εμφανίζονται στην έκφραση της Kc (Δn > 0), η απόδοση ελαττώνεται
(π.χ. Α(g) ↔ Β(g) + Γ(g) , Kc=α2C/1-α : C αυξάνεται => α ελαττώνεται).
ii) Aν με μετατόπιση της ισορροπίας προς τα δεξιά δε μεταβάλλονται τα συνολικά moles των σωμάτων που εμφανίζονται στην έκφραση της Kc (Δn = 0), η απόδοση παραμένει σταθερή διότι είναι ανεξάρτητη από την αρχική συγκέντρωση του αντιδρώντος
(π.χ. 2Α(g)↔Β(g) + Γ(g) Kc=α2/4(1-α)2 : α ανεξάρτητο του C)."
Φίλτατε Θεόδωρε ΧΡΟΝΙΑ ΠΟΛΛΑ.
Συζήτησα με συναδέλφους το θέμα της καταχώρησης και συγκεκριμένα:
Υπάρχει περίπτωση η ισορροπία να μετατοπίζεται δεξιά και η απόδοση να μειώνεται, επ΄αυτού απάντησα όπως ακριβώς αναφέρομαι στο βιβλίο μου 1ος τόμος σελ.403.
Καλά κάνεις και αναλύεις το θέμα περισσότερο άλλωστε αυτή είναι η δύναμη του υλικονέτ, καθώς πληροφορούμαι ότι μετά από ανάλογες καταχωρήσεις που κάναμε παλιότερα επήλθαν διορθώσεις στα εν΄λόγω συγγράμματα
Γεια σας! Μια ερώτηση.. Συνάντησα σε μια άσκηση ανάλογη περίπτωση, μόνο που αφού είχε αποκατασταθεί η χημικη ισορροπία, αφαιρούνταν ποσότητα ενός από τα προϊόντα. Τι αλλάζει τότε στην απόδοση; Δοκιμασα να βρω την νέα απόδοση χρησιμοποιώντας την ουσία από την οποία αφαιρέσαμε ποσότητα και απετυχε…
Καλημέρα Ειριάννα.
Θα σου πρότεινα να ξεκινήσεις μια νέα συζήτηση στο φόρουμ, δίνοντας όμως συγκεκριμένο παράδειγμα με αριθμητικά δεδομένα, για να δούμε πού είναι το πρόβλημα και ποια η λύση του.