-
Ο/η Κεφαλάς Δημήτριος σχολίασε το άρθρο Ταχύτητα αντίδρασης πριν από 2 έτη, 1 μήνα
Μιλάει για την αρχική ταχύτητα πως θα επηρεασθεί κάποιο διαγώνισμα και θεωρεί ότι δεν επηρεάζεται
-
H/o Κεφαλάς Δημήτριος έγραψε ένα νέο άρθρο πριν από 2 έτη, 1 μήνα
Ταχύτητα αντίδρασης
 Στην θερμική διάσπαση του KClO3(s) η αρχική ταχύτητα της αντίδρασης δεν εξαρτάται από το μέγεθος των κόκκων του KClO3;
Στην θερμική διάσπαση του KClO3(s) η αρχική ταχύτητα της αντίδρασης δεν εξαρτάται από το μέγεθος των κόκκων του KClO3; -
H/o Κεφαλάς Δημήτριος έγραψε ένα νέο άρθρο πριν από 3 έτη
σύγκριση μεγέθους κατιόντων
 Σύγκριση μεγέθους κατιόντος Li (Ζ=3) και κατιόντος Να (Ζ=11) Οι 2 παράγοντες που επηρεάζουν δηλαδή το δραστικό πυρηνικό φορτίο και ο αριθμός των στιβάδων αντικρούονται Τι συμβαίνει τελικά;
Σύγκριση μεγέθους κατιόντος Li (Ζ=3) και κατιόντος Να (Ζ=11) Οι 2 παράγοντες που επηρεάζουν δηλαδή το δραστικό πυρηνικό φορτίο και ο αριθμός των στιβάδων αντικρούονται Τι συμβαίνει τελικά;-
Καλημέρα Δημήτρη.
Το κατιόν του Νατρίου αφού έχει δύο στοιβάδες, μία περισσότερη από το αντίστοιχο του λιθίου, δεν θα έχει και μεγαλύτερο όγκο;
Όταν μελετάμε την επίδραση του δραστικού πυρηνικού φορτίου στο μέγεθος, δεν κάνουμε σύγκριση ατόμων με ίδιο n; -
Καλησπέρα. Δημήτρη η λογική που το προσεγγίζουμε είναι αυτή που λέει ο Διονύσης. Θεωρούμε τον αριθμό στιβάδων πιο καθοριστικό.
-
-
H/o Κεφαλάς Δημήτριος έγραψε ένα νέο άρθρο πριν από 4 έτη, 2 μήνες
Καλησπερα συνάδελφοι. Ξεφυλλίζοντας το τελευταίο βιβλίο του ΣΑΛΤΕΡΗ έπεσα σε ερώτηση υβριδισμού. Συγκεκριμένα για το συμπλοκο [NiCl4]^2_ δίνει υβριδισμο sp3 ενώ για το [Cu(NH3)4]^2+ δίνει dsp2. Έχετε κάποια εξήγηση;

-
Δημήτρη καλησπέρα. Τα πειραματικά δεδομένα μας καθοδηγούνε. Γράφει ο Σαλτερής ότι το σύμπλοκο του νικελίου είναι τετραεδρικό, ενώ το σύμπλοκο του χαλκού (επίπεδο) τετραγωνικό. H τετραεδρική γεωμετρία αντιστοιχεί σε sp3 υβριδισμό, ενώ η τετραγωνική σε dsp2 (δίνει και 2 άλλες επιλογές οι οποίες δεν αντιστοιχούν σε 4 υποκαταστάτες)
-
Φυσικά δεν συμφωνώ να ζητηθεί κάτι τέτοιο από τους μαθητές διότι δεν γνωρίζουν για υβριδισμό με συμμετοχή d τροχιακών και ειδικά σε σύμπλοκα που είναι πιο δύσκολη η εξήγηση. Αυτή η ερώτηση δηλαδή πρέπει να απαντηθεί αποκλείοντας τις άλλες επιλογές που δίνονται ως απάντηση.
-
-
Ο/η Κεφαλάς Δημήτριος σχολίασε το άρθρο Αριθμός δεσμών υδρογόνου πριν από 4 έτη, 7 μήνες
Ευχαριστώ Θοδωρή όμως σύμφωνα με τον Σαλτερή: Η2Ο 4 δεσμοί αλλά HF 2 δεσμοί. Σελ. 47 από το τεύχος ΔΙΑΜΟΡΙΑΚΕΣ κλπ
-
H/o Κεφαλάς Δημήτριος έγραψε ένα νέο άρθρο πριν από 4 έτη, 7 μήνες
Συνάδελφοι καλημέρα και καλή χρονιά. Εδώ και πολύ καιρό διαβάζω διάφορες εντελώς αντικρουόμενες θεωρίες για το πλήθος των δεσμών υδρογόνου που μπορεί να δημιουργήσει μια ένωση. Υπάρχει καμία υπεύθυνη απάντηση ;

-
Καλησπέρα Δημήτρη. Αν εννοείς: “Πόσους δεσμούς Η μπορεί να σχηματίσει το μόριο μιας ένωσης;” θα έλεγα όσα είναι τα Η που συνδέονται με F, O ή Ν συν τον αριθμό των μη δεσμικών ζευγών ηλεκτρονίων που έχει κάθε άτομο F, O ή Ν. Έτσι, για παράδειγμα τα μόρια Η2Ο, ΝΗ3 και HF μπορεί το καθένα να σχηματίσει 4 δεσμούς Η. Αυτό βέβαια δε σημαίνει ότι αν διαθέτεις μια ποσότητα π.χ. HF τότε κάθε μόριο HF ότι θα σχηματίζει τόσους δεσμούς Η.
-
Ευχαριστώ Θοδωρή όμως σύμφωνα με τον Σαλτερή: Η2Ο 4 δεσμοί αλλά HF 2 δεσμοί. Σελ. 47 από το τεύχος ΔΙΑΜΟΡΙΑΚΕΣ κλπ
-
Αυτό Δημήτρη είναι στατιστικός μέσος όρος και συμβαίνει διότι τα άτομα Η δεν επαρκούν να σχηματιστούν περισσότεροι δεσμοί Η. Στο υγρό νερό π.χ. σχηματίζονται κατά μέσο όρο 3,2 δεσμοί Η ανά μόριο…
-
-
-
Λέει στο βιβλίο του καθηγητή Κλούρα “Βασική Ανόργανη Χημεία” 4η έκδοση, 2000, σελ. 299: Το άτομο του F στο ΗF διαθέτει 3 ελεύθερα ζεύγη ηλεκτρονίων και ένα μόνο άτομο Η. Σε πολυμοριακά συγκροτήματα HF ένα δεδομένο μόριο HF μπορεί να σχηματίσει μέχρι 4 γέφυρες υδρογόνου, όμως επειδή δεν υπάρχει επαρκής αριθμός ατόμων Η, ο ανώτερος αριθμός γεφυρών Η ανά μόριο HF περιορίζεται στο στατιστικό μέσο όρο που είναι 2″.
-
Κάτι ανάλογο επίσης πρέπει να συμβαίνει και στην ΝΗ3, όπου εκεί δεν επαρκούν τα μη δεσμικά ζεύγη ηλεκτρονίων του Ν και πάλι ο στατιστικός μέσος όρος δεσμών Η ανά μόριο είναι 2.
-
Καλησπέρα συνάδελφοι.Σε κάποιο blog ένας συνάδελφος δημοσίευσε τον εξής πρακτικό κανόνα (που προκύπτει από τύπους και μελέτες) : χ τα άτομα Η, ψ τα μη δεσμικά ζευγη του Ο η΄Ν ή F.Πολλαπλασιάζεις τον μικροτερο απ αυτους τους αριθμούς επί 2 και βρίσκεις το πλήθος των δ. υ.
-Πάντως ”λειτουργει ” ο κανονας και στον πάγο και στο HF και στην NH3 !
-
-
Ο/η Κεφαλάς Δημήτριος σχολίασε το άρθρο Θέματα Πανελλαδικών εξετάσεων στη Χημεία 2021 πριν από 4 έτη, 10 μήνες
Στην ογκομετρηση του οξέος αρχικά pH περίπου 3. Άρα τα Η3Ο+ του νερού 10^-11 άρα ο βαθμός ιοντισμου του νερού 10^-11/55,5. Κάποια στιγμή θα εχω pH=7. Τότε τα οξωνια του νερού θα είναι της τάξης του 10^-7 και λίγο λιγότερα. Άρα ο βαθμός ιοντισμου του νερού θα είναι της τάξης 10^-7/55,5. Άρα μεγαλώνει και επομένως ο αυτοιοντισμος του νερού αυξ…[Περισσότερα]
-
Ο/η Κεφαλάς Δημήτριος σχολίασε το άρθρο Κύλινδρος σε οριζόντιο επίπεδο εκτελεί κχο πριν από 5 έτη
Ευχαριστώ Διονύση. Συνάδελφος είμαι και εχω απλά κάποιους προβληματισμούς σε σχέση με τη στατική τριβή που υπήρχε στο κεκλιμένο απαραίτητα για να γίνεται η κύλιση και στο οριζόντιο μηδενίζεται. Πάντως ευχαριστώ
-
H/o Κεφαλάς Δημήτριος έγραψε ένα νέο άρθρο πριν από 5 έτη
Κύλινδρος m,R αφού κατέλθει σε κεκλιμένο επίπεδο συνεχίζει να κινείται σε οριζόντιο επίπεδο εκτελώντας ΚΧΟ. Θα συνεχίσει να κινείται ομαλά ;
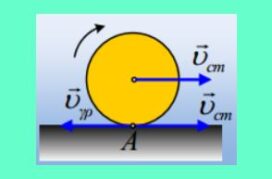
-
Θα συνεχίσει να κινείται ομαλά Δημήτρη, αλλά μήπως αποπροσανατολίζεσαι;
Η μελέτη της κίνησης δεν είναι στην ύλη που πρόκειται να εξετασθείς!-
Ευχαριστώ Διονύση. Συνάδελφος είμαι και εχω απλά κάποιους προβληματισμούς σε σχέση με τη στατική τριβή που υπήρχε στο κεκλιμένο απαραίτητα για να γίνεται η κύλιση και στο οριζόντιο μηδενίζεται. Πάντως ευχαριστώ
-
-
Καλησπέρα Δημήτρη και Διονύση.
Δεν έχω καταλάβει την ερώτηση.
Σκέφτομαι δύο άσχετα θέματα:- Όταν ένας κύλινδρος φτάνει με μια ταχύτητα στη βάση κεκλιμένου επιπέδου μπαίνει στο οριζόντιο με ταχύτητα μικρότερη από αυτήν που έφτασε. (Διατήρηση στροφορμής ως προς σημείο επαφής).
- Όταν αποκτά την όποια ταχύτητα και τη όποια γωνιακή ταχύτητα στο οριζόντιο επίπεδο, θα παραμείνουν αυτές σταθερές; Ναι αν είναι rigid body , όχι αν είναι πραγματικό στερεό (τριβή κύλισης).
-
Καλησπέρα Γιάννη.
Γράφαμε μαζί.
Εγώ άλλο κατάλαβα…-
Γεια σου Διονύση.
Αν η ερώτηση είναι αυτή τότε ισχύουν όσα λες στο επόμενο σχόλιο.
Ένα rigid body δεν σταματά ποτέ.
Σταματούν οι πραγματικοί κύλινδροι.
-
-
Kαλησπέρα Γιάννη και Διονύση.Καλησπερα σε ολους Γιάννη εκατσα και σκεφτηκα το 1.που γραφεις.Για να εφαρμόσουμε την αρχη διατηρηση της στροφορμης ως προς το σημειο Β του οριζοντιου επιπεδου που ειναι το ενα εκ των δυο σημειων επαφης και να βρουμε την ταχυτητα στο οριζοντιο επιπεδο , τεχνικα δεν αρκει η τριβη.Αν θεωρησουμε οτι την μειωμενη ταχυτητα στο οριζοντιο επιπεδο την αποκτα ακαριαια, τοτε πρεπει να υπαρχει ενας μηχανισμος που να μπορει να δωσει πολυ μεγαλες δυναμεις,για παραδειγμα σαν αυτον στο σχημα οπου ενα εξογκωμα στο οριζοντιο επιπεδο μπαινει σε μια εσοχη στον κυλινδρο,ωστε να δημιουργηθουν συνθηκες κρουσης..Οταν η μεταβατικη κατασταση της κρουσης περασει,τοτε προφανως οπως ειπες οι ταχυτητες θα παραμενουν σταθερες χωρις υπαρξη τριβης οπου οπως εξηγησε και ο Διονύσης,δεν χρειαζεται.
https://1.bp.blogspot.com/-9jSSRy2l7Xs/YHnZbJdRBRI/AAAAAAAAKCU/zSqw9WD4W3wSt9fLNHEs58dV2m1N-DVLQCLcBGAsYHQ/w480-h640/1%25CE%25B1.jpg
-
Δημήτρη, συγνώμη για την παρεξήγηση.
Δεν ξέρω γιατί, αλλά θεώρησα ότι είσαι μαθητής…
Στο ερώτημα τώρα.
Στο κεκλιμένο επίπεδο υπάρχει στατική τριβή γιατί “υποχρεώνεται” να εμφανιστεί για να εξασφαλίζεται η κύλιση. Επιταχύνεται μεταφορικά ο κύλινδρος, οπότε πρέπει να επιταχυνθεί και στροφικά.
https://1.bp.blogspot.com/-rJ25jbeVETQ/YHht5SCS1bI/AAAAAAAAKBo/uQ2KBeLYchUjY4KpKHCH2K5mQduWGDVNwCLcBGAsYHQ/w640-h190/4%25CF%2587.PNGΦτάνοντας στο οριζόντιο επίπεδο κυλίεται και ισχύει η εξίσωση υcm=ω∙R (1).
Έστω τώρα ότι εμφανίζεται μια τριβή προς τα αριστερά (πρώτο σχήμα). Τότε ο κύλινδρος θα αποκτούσε μια αρνητική επιτάχυνση κέντρου μάζας, με αποτέλεσμα να μειώνεται η ταχύτητα υcm, ενώ η ροπή της τριβής θα επιτάχυνε την στροφική κίνηση με αποτέλεσμα να αυξάνεται η γωνιακή ταχύτητα. Έτσι η σχέση (1) θα έπαυε να ισχύει, αλλά κυρίως (μας ενδιαφέρει…) το σημείο επαφής με το έδαφος θα αποκτούσε ταχύτητα προς τα αριστερά, άρα αυτομάτως η τριβή θα έπρεπε να αλλάξει κατεύθυνση και να είναι προς τα δεξιά.
Αυτό όμως θα είχε το αντίθετο αποτέλεσμα!
Θα είχαμε αύξηση του υcm και μείωση του ω, οπότε και πάλι η ταχύτητα του σημείου Γ θα ήταν προς τα δεξιά και η τριβή πρέπει να πάει στα αριστερά…(δεύτερο σχήμα).
Συμπέρασμα; Ούτε το ένα δεν μπορεί να ισχύσει ούτε το άλλο. Η τριβή παίρνει την τιμή Τ=0 και ο κύλινδρος συνεχίζει να κυλίεται με σταθερή υcm και με σταθερή γωνιακή ταχύτητα ω, ώστε να ισχύει διαρκώς η σχέση (1). -
Καλησπέρα Κωνσταντίνε.
Ο κύριος δράστης είναι η Ν. Δεν έχει ροπή ως προς το σημείο επαφής.-
Φυσικά και η τριβή παίρνει μεγάλες τιμές (διότι είναι μεγάλη η Ν). Με συντελεστή μ=1 αποκαθίσταται κύλιση χωρίς ολίσθηση ακαριαία.
Με μικρό συντελεστή μ=0,1 η καθυστέρηση είναι ελάχιστη.
Η προσομοίωση την καταγράφει δύσκολα και μόνο με την συνδρομή του “κασετόφωνου”.-
Αν το οριζοντιο επιπεδο ητανε λειο τι θα γινοτανε?
-
Πάλι θα διετηρείτο η στροφορμή, όμως θα είχαμε και διατήρηση της ιδιοστροφορμής (όποιας θα είχε αποκτήσει κατά την κάθοδο).
Το θέμα όμως θα λυνόταν ευκολότερα με ανάλυση ταχύτητας κάθετα και παράλληλα στο οριζόντιο επίπεδο. Θα έμενε μόνο η οριζόντια συνιστώσα.-
Αρα με αναλυση ταχυτητας οπως ειπες προκυπτει ευκολα οτι η ταχυτητα του κεντρου μαζας θα μειωθει. Αν στην συνεχεια το οριζοντιο επιπεδο λιγο πιο δεξια παψει να ειναι λειο,.η εχει ενα μηχανισμο οπως αυτο του σχηματος μου,θα αποκατασταθει κανονικη κυλιση αφου θα προσαρμοστει και η γωνιακη ταχυτητα.Αρα για να δικαιολογησουμε απλως την μειωμενη ταχυτητα κυλισης μετα την μεταβαση στο οριζοντιο επιπεδο δεν ειναι απαραιτητο να επικαλεστουμε διατηρηση στροφορμης, γινεται και με πιο στοιχειωδεις μεθοδους.
-
Έστω ότι είναι λείο για μεγάλη απόσταση. Μετά συναντά ένα τραχύ δάπεδο. Θα δράσει τριβή η οποία θα το αναγκάσει να κυλίεται χωρίς ολίσθηση. Υπολογισμοί γίνονται και βρίσκουμε την τελική γωνιακή ταχύτητα και την τελική ταχύτητα.
Οι υπολογισμοί γίνονται και κλασικά(ΣF=m.α και Στ=Ι.αγ). Όμως οι υπολογισμοί γίνονται πολύ ταχύτερα αν δουλέψουμε με στροφορμή ως προς ακίνητο σημείο του εδάφους. Δεν είναι η μοναδική λύση, όμως είναι ταχύτερη της κλασικής.-
Για παράδειγμα:
Μια μπάλα έχει αρχική ταχύτητα υο και αρχική γωνιακή ταχύτητα ωο. (Ανάποδο φάλτσο). Ποια είναι η τελική της ταχύτητα;
Το πρόβλημα αυτό λύνεται και εντελώς μαθητικά. Όμως λύνεται “ακαριαία” με διατήρηση στροφορμής ως προς σημείο του εδάφους.-
Εχει μια τετοια ασκηση ο Ηalliday στο βιβλιο που εχεις ασκηση 36 σελ.293.
-
Θα την δω. Είχα δει σε ανάρτηση του Ανδρέα Κασσέτα την τεχνική.
Την υιοθέτησα και την χρησιμοποίησα σε αναρτήσεις κρούσεων με τριβή.Θέματα ολίσθησης, όταν δεν είχαμε περικοπές στο στερεό, δεν εμφανίστηκαν ποτέ. Έκανα καλού κακού δύο τέτοια, λυμένα όμως με τον κλασικό τρόπο. Ήμουν σίγουρος σχεδόν πως δεν θα πέσουν.
-
-
-
-
-
-
-
-
-
Αυτό που έγραψα πριν επιβεβαιώνεται σε προσομοίωση.
-
-
H/o Κεφαλάς Δημήτριος έγραψε ένα νέο άρθρο πριν από 5 έτη
Μπορεί μια μονόδρομη αντίδραση με αντιδρόντα σε στοιχειομετρική αναλογία να έχει απόδοση μικρότερη του 1; Εγώ πιστεύω πως μπορεί να συμβεί ανάλογα με τις συνθήκες.

-
Ναι γίνεται, φαντάσου να σκάει μία παράλληλη αντίδραση η οποία να ευνοείται επειδή π.χ. μπορεί να πέφτει ίζημα και παράλληλα να φτιάχνεται κάτι άλλο μέσω άλλης αντίδρασης το οποίο όμως να είναι διαλυτό, έχεις όμως ήδη χάσει αρκετή ποσότητα στο ίζημα της παράλληλης αντίδρασης. Οι συνθήκες όπως σωστά αναφέρεις παίζουν σίγουρα ρόλο, όπως ο δ/της-ες, το pH, θερμοκρασία, φυσικά η στοιχειομετρία, ακόμη και το μέγεθος των κόκκων του στερεού κτλ.) Σε ένα δ/μα γίνεται χαμός από χημικές οντότητες, που προφανώς δε μπορούμε να τις ξέρουμε όλες και γενικά συμβαίνουν αντιδράσεις και μηχανισμοί που δε ξέρουμε και ίσως δε μάθουμε και ποτέ…Πέρυσι στα θέματα της χημείας αν δεις το Δ2 είναι παράδειγμα μονόδρομης αντίδρασης που δεν έχει απόδοση 100 % επειδή τα προϊόντα αντιδρούν μεταξύ τους.
-
Καλησπέρα κι από μένα. Δημήτρη οι βασικοί λόγοι που μία αντίδραση έχει απόδοση μικρότερη από 1 είναι τρεις: α) Η αντίδραση είναι αμφίδρομη β) γίνονται παράπλευρες αντιδράσεις γ) έχουμε απώλειες κατά την απομόνωση των προϊόντων. Ξέρεις, αυτός ο τελευταίος λόγος, αν και δεν οφείλεται στην αντίδραση αυτή καυθεαυτή, δεν είναι καθόλου ασήμαντος. Μια καθηγήτρια στο Πανεπιστήμιο έλεγε: “Ένα θέμα είναι να φτιάξεις την επιθυμητή ουσία μέσω της κατάλληλης αντίδρασης και ένα άλλο -μεγάλο- θέμα είναι να καταφέρεις να την πάρεις χωρίς πολλές απώλειες σε καθαρή κατάσταση.” θέλοντας να επισημάνει πόσο δύσκολη και επίπονη διαδικασία είναι η ποσοτική απομόνωση της ουσίας από το μείγμα της αντίδρασης.
-
Συμφωνώ απόλυτα με όλα. Όσον αφορά αυτό που τονισατε στην τριτη περίπτωση που αφορά την πειραματική απόδοση που στις περισσότερες περιπτώσεις και θυμάμαι στα εργαστήρια της οργανικής είναι απίθανο να είναι 1 λόγω της δυσκολίας της απομόνωσης του προϊόντος, που μάλιστα σε μερικές περιπτώσεις είναι πιο επίπονη και χρονοβόρα ως διαδικασία από την διαδικασία που ακολουθείται για την παρασκευή της ουσίας που θέλουμε και για την οποία μετρουμε την απόδοση. Αυτό βέβαια είναι δύσκολο να το ξέρουν τα παιδιά γιατί δεν εκτελούν πειραματα. Να θυμίσω εδώ ότι αυτό μπορούσε να τονιστεί με την παλιά ύλη που περιείχε την οργανική και τονίζε ότι η απόδοση στην αντίδραση υποκατάστασης αλκοολών με SOCl2 προς παρασκευή του αντίστοιχου αλκυλαλογονιδιου και αν το δοχείο είναι ανοιχτό τα παραπροϊόντα είναι το SO2 και το HCl που είναι αέρια σε συνήθη θ και πίεση και επομένως από αρχή Le Chatelier η αντίδραση μετατοπίζεται πλήρως στα δεξιά και επίσης αν τα αντιδρωντα είναι σε στοιχείο μετρική αναλογία δεν απαιτείται διαχωρισμός της ουσίας με κάτι που παραμένει στο δοχείο.
Ωραίο πχ της δεύτερης περίπτωσης αποτελεί πάλι η επίδραση ΝαΟΗ ή ΚΟΗ σε αλκυλαλογονιδιου που ανάλογα με τις συνθήκες γίνονται δύο παράλληλες αντιδράσεις. Σε αλκοολούχο διάλυμα ευνοείται η απόσπαση οπότε παράγεται κυρίως αλκενιο, ενώ σε υδατικό ευνοείται η υποκατάσταση και έχουμε παραγωγή της αντίστοιχης αλκολης. Ακόμα στην απόσπαση λόγω κανονα Saytzeff μπορούμε να έχουμε κύριο και δευτερεύον προϊόν, οπότε μιλάμε για 3 παράλληλες αντιδρασεις.Όμως και στις δύο περιπτώσεις της υποκαταστασης δηλ. και της απόσπασης δεν παρεμποδίζεται πλήρως η άλλη αντιδραση και παράγεται πάντα και σε μικρότερη ποσότητα ένα από τα δύο προϊόντα που αναφέρθηκαν και ενδεχομένως και τρίτο από την απόσπαση όπως αναφέρθηκε. Και ενώ ο βαθμός μετατροπής του αλκυλαλογονιδιου είναι 1 αν δεν είναι σε περίσσεια και λάβουμε υπόψη μας και τις δύο ή 3 αντιδράσεις που στη μία η στις 2 ένα μέρος του γίνεται αλκενιο ,και ενδεχομένως ενα αλλο μέρος του ισομερες αλκενιο μέρος ενώ στην αλλη το υπόλοιπο μέρος του αλκοόλη, η απόδοση για κάθε αντίδραση δεν θα είναι 1, αλλά το άθροισμα των αποδόσεων των 2 ή 3 παράπλευρων αντιδράσεων ισούται με την μονάδα. Και σε μια πιο απλή περίπτωση που είναι εντός ύλης( έχει διδαχθεί στη β λυκείου) στην προσθήκη πχ σε αλκενιο που αν παράγεται κύριο και δευτερεύον προϊόν από κανόνα Markovnikov η απόδοση για κάθε αντίδραση είναι μικρότερη του 1, αλλά το άθροισμα των αποδόσεων και των δύο αντιδράσεων είναι 1.
Φυσικά και στις αμφίδρομες ισχύει πάντα και η απόδοση ειναι μικρότερη του ένα όπως αναφέρετε στην αρχή. Συμφωνώ απόλυτα!!
-
-
Γεια σου Σοφία (επίτρεψέ μου τον ενικό). Αλήθεια, επειδή το ανέφερες, έχεις κάποια εξήγηση γιατί σε υδατικό διάλυμα βάσης ευνοείται η υποκατάσταση των RX ενώ σε αλκοολικό η απόσπαση;
-
-
Ο/η Κεφαλάς Δημήτριος σχολίασε το άρθρο Βαθμός ιοντισμού ασθενούς οξέος πριν από 5 έτη
Καλησπερα και ευχαριστώ Πέτρο. Εχω την ίδια άποψη με σένα αλλά με προβληματίζει το γεγονός ότι αν σε διάλυμα ΗΑ 1Μ όγκου 1L με Κα=10^-4 προσθέσω 0,1mol KOH ο νέος βαθμός ιοντισμού δεν θα είναι μικρότερος ;
-
H/o Κεφαλάς Δημήτριος έγραψε ένα νέο άρθρο πριν από 5 έτη
Καλημέρα.
Σχετικα με την μεταβολή του βαθμού ιοντισμού ασθενους οξέος όταν στο διαλυμα προσθεσω μικρη ποσοτητα ΚΟΗ προκυπτουν αντιφατικα πραγματα. Τελικα αυξανεται ή μειώνεται;
Αφου η ΧΙ μετατοπιζεται […]

-
Καλημέρα Δημήτρη.
Μετέφερα το ερώτημα στο φόρουμ, αφού αν έμενε στις δραστηριότητες, δεν θα το έβλεπε κανείς… -
Καλησπέρα Δημήτρη
Κοίτα, έχουμε Ka / [H3+O] = [A-] / [HA]. Προσθέτοντας ΟΗ- μειώνονται τα Η3Ο+, λόγω εξουδετέρωσης, η ισορροπία του ιοντισμού του οξέος πάει προς τα δεξιά και αφού Κa σταθερό, αυξάνονται τα δύο ίσα κλάσματα. Δεν ξεχνάμε όμως ότι όσο αυξάνεται το Α- , τόσο μειώνεται και το ΗΑ, άρα ο βαθμός ιοντισμού του οξέος θα αυξάνεται. Μας αφήνει αδιάφορους η ΕΚΙ, γιατί και μόνο που αυξάνεται η [Α-], αυτό σημαίνει μείωση ταυτόχρονα της [ΗΑ], συνεπώς αύξηση του βαθμού ιοντισμού. Δες πως λειτουργεί ο δείκτης- ασθενές οξύ, ΗΔ. Προσθέτοντας υδροξείδια η βασική μορφή του δείκτη Δ- υπερισχύει της όξινης ΗΔ και ο βαθμός ιοντισμού αυξάνεται.
Δες το και έτσι: Ισχύει α= [A-] / [HA]+[Α-] . Προσθέτοντας ΟΗ-, σιγά-σιγά θα έχουμε:
[ΗΑ] << [Α-] , που σημαίνει ότι ο βαθμός ιοντισμού θα αυξάνεται και θα γίνει σιγά-σιγά α= [A-] / [Α-]=1.-
Καλησπερα και ευχαριστώ Πέτρο. Εχω την ίδια άποψη με σένα αλλά με προβληματίζει το γεγονός ότι αν σε διάλυμα ΗΑ 1Μ όγκου 1L με Κα=10^-4 προσθέσω 0,1mol KOH ο νέος βαθμός ιοντισμού δεν θα είναι μικρότερος ;
-
Καλησπέρα Δημήτρη, καλησπέρα Πέτρο.
Δημήτρη βρίσκεις ότι μειώνεται ο βαθμός ιοντισμού στο διάλυμα που προκύπτει, παίρνοντας t=0 (που λέμε στη Φυσική…) τη στιγμή που έχει πραγματοποιηθεί η αντίδραση εξουδετέρωσης και βρίσκεις τι ποσοστό των μορίων του οξέος με “αρχική συγκέντρωση” 0,9Μ ιοντίζονται, παρουσία του άλατος ΚΑ 0,1Μ. Και σωστά το βρίσκεις…
Αν όμως δεν ξεκινήσουμε από αυτό το σημείο, αλλά από την κατάσταση ΗΑ1Μ, όπου ο αρχικός βαθμός ιοντισμού είναι 0,01 (έχουμε δηλαδή στο διάλυμα Α- με συγκέντρωση 0,01Μ), τι θα βρούμε για τον βαθμό ιοντισμού μετά την προσθήκη του ΚΟΗ;
Θα γράψουμε την εξουδετέρωση και στο ερώτημα ποια η τελική συγκέντρωση των ιόντων Α, θα απαντήσουμε 0,1Μ! (μετά τις προσεγγίσεις).
Δεν έχουμε αύξηση από 0,01Μ σε 0,1Μ;
Αυτό περιγράφει παραπάνω και ο Πέτρος.
ΥΓ
Πέτρο με την ευκαιρία, η διερεύνησή σου στην τελευταία ανάρτηση, θυμίζει… Φυσικό!!!
🙂 🙂
-
-
-
Επισης απο τη σχεση α=Ka/Ka+[H3O+] μπορουμε να συμπερανουμε οτι η μειωση της [Η3Ο+] με την προσθηκη της βασης θα αυξησει τον α.Σε θεωρητικη ερωτηση επομενως πρεπει να πουμε οτι αυξανει.Το θεμα ειναι οταν ζητειται να υπολογισθει με αριθμητικα δεδομενα οπως αυτα που αναφερει ο Δημητρης.Επειδη το σχολικο θεωρει ως αρχικη κατασταση,t=0 οπως πολυ περιγραφικα ανεφερε ο Διονυσης,την κατασταση μετα τις μονοδρομες αντιδρασεις που πραγματοποιουνται δηλαδη ΗΑ 0,9Μ και NaA 0,1M και με βαση το παραδειγμα 5.11 νομιζω πρεπει να απαντησουμε οτι α =10^-3 και οχι α=0,1.Υπαρχει σαφως εδω ενα θεμα οσο δεν ξεκαθαριζεται το θεμα της αρχικης καταστασης στο σχολικο.
-
Προσπαθώντας να σκεφτώ όπως οι μαθητές μας:
Οταν έχουμε ΗΑ 0,9 Μ και ΚΑ 0,1Μ ισχύει η προσεγγιστική σχέση α=Κα/Cβ., όπως προκύπτει από την Henderson/Hasselbalch.
Συνεπώς αν εκεί προστεθεί ΚΟΗ η Cβ θα αυξηθεί , άρα ο α θα μειωθεί.
-
-
Κεφαλάς Δημήτριος εγγράφηκε πριν από 5 έτη
Καλησπέρα Δημήτρη.
Νομίζω ότι πάντα η ταχύτητα αντίδρασης ενός στερεού εξαρτάται από το βαθμό κατάτμισής του.
Αλλά αυτό πώς θα φανεί στην παραπάνω καμπύλη της αντίδρασης; Στον χρόνο ολοκλήρωσης της αντίδρασης. Σε αυτό αποσκοπεί η ερώτηση ή σε κάτι άλλο που δεν καταλαβαίνω;
Μιλάει για την αρχική ταχύτητα πως θα επηρεασθεί κάποιο διαγώνισμα και θεωρεί ότι δεν επηρεάζεται