-
H/o Παναγιώτης Κουτσομπόγερας έγραψε ένα νέο άρθρο πριν από 2 μήνες
Βατραχοδηλητήρια και δολοφονίες
 Μια πρόσφατη υπόθεση που έχει προκαλέσει διεθνείς αντιδράσεις σχετικά με «δηλητήριο από βατράχους» και τον ρόλο του στην περίπτωση του πολιτικού Αλεξέι Ναβά […]
Μια πρόσφατη υπόθεση που έχει προκαλέσει διεθνείς αντιδράσεις σχετικά με «δηλητήριο από βατράχους» και τον ρόλο του στην περίπτωση του πολιτικού Αλεξέι Ναβά […] -
H/o Ανδρέας Ριζόπουλος έγραψε ένα νέο άρθρο πριν από 2 μήνες
Ένας μικρός μαγνήτης αφήνεται πάνω από οριζόντιο δαχτυλίδι
 Ένας μικρός κυλινδρικός μαγνήτης νεοδύμιου (κράμα Nd₂Fe₁₄B), αφήνεται ελεύθερος να πέσει πάνω από ένα οριζόντιο μεταλλικό δακτύλιο, με το βόρειο πόλο […]
Ένας μικρός κυλινδρικός μαγνήτης νεοδύμιου (κράμα Nd₂Fe₁₄B), αφήνεται ελεύθερος να πέσει πάνω από ένα οριζόντιο μεταλλικό δακτύλιο, με το βόρειο πόλο […]-
Η ανάρτηση αφιερώνεται στο Χρήστο Αγριόδημα, αφού πηγή αποτέλεσε η δική του
-
Πολύ καλή Ανδρέα!
-
Καλημέρα παιδιά. Πολύ καλή ανάλυση Ανδρέα! Το 4ο ερώτημα απαιτητικό ακόμη και για τους υποψήφιους της Θετικής.
-
Καλησπέρα Γιάννη και Αποστόλη. Σας ευχαριστώ. Για τους περισσότερους μαθητές η επαγωγή είναι Βυl. Το πέρασμα μαγνήτη από δακτύλιο, η αναπήδηση δακτυλίου έχει πάει στα αζήτητα. Ευτυχώς που κάνουμε το εναλλασσόμενο και την αυτεπαγωγή.
-
Καλησπέρα Ανδρέα
Σε ευχαριστώ για την αφιέρωση.
Το κάλυψες πλήρως το θέμα. Όπως λες επαγωγή δεν είναι μόνο το Βul. -
Καλησπέρα Χρήστο. Να είσαι καλά! Προσωπικά μου αρέσουν πολύ τέτοιες ασκήσεις, παρά με ράβδους 1m που κάνουν πολλά μέτρα μέχρι να φτάσουν την οριακή ταχύτητα. Οι θεματοδότες προτιμούν βέβαια τις ράβδους, οπότε και εμείς…
-
Καλό απόγευμα Ανδρέα.
Συγχαρητήρια για το θέμα που μας παρουσίασες. Ένα πολύ όμορφο, αλλά και πολύ δυνατό θέμα!
Προσωπικά, για λόγους διδακτικούς, προτιμώ τις κινήσεις αγωγών και πλαισίων, αφού το επίπεδο δυσκολίας αυξάνεται κατακόρυφα με ασκήσεις οπως η παραπάνω.
Όμως αν κάποιος μαθητής μπορεί να την πλησιάσει, αυτό είναι απόδειξη ότι έχει κατανοήσει σε βάθος, πάρα πολλά πράγματα και δεν αναμασά βήματα που έμαθε, από πάρα πολλές ασκήσεις που είδε και έλυσε…
Η λογική του θέματος του 1993 σε πλήρη εκδοχή! -
Ναι Ανδρέα, αυτή ακριβώς την ερώτηση μου θύμισες…
-
Καλησπέρα Διονύση. Σε ευχαριστώ για τον έπαινο και το σχολιασμό. Για όσους μαθητλες μας διαβάζουν μάλλον εννοείς την ερώτηση του 93
-
Πολύ ωραία ανάρτηση Ανδρέα.
-
Καλησπέρα Παύλο. Σε ευχαριστώ.
-
Καλησπέρα Ανδρέα.
Τα είπες όλα!!!
Συγχαρητήρια.
-
-
H/o Διονύσης Μάργαρης έγραψε ένα νέο άρθρο πριν από 2 μήνες
Ένας αγωγός επιταχύνεται σε μαγνητικό πεδίο.
 Ο αγωγός ΑΓ, μήκους l=1m, μάζας m=0,5kg και αντίστασης r=0,5Ω, ξεκινά από την ηρεμία για t=0 και επιταχύνεται προς τα δεξιά, με την επίδραση σταθερής οριζό […]
Ο αγωγός ΑΓ, μήκους l=1m, μάζας m=0,5kg και αντίστασης r=0,5Ω, ξεκινά από την ηρεμία για t=0 και επιταχύνεται προς τα δεξιά, με την επίδραση σταθερής οριζό […]-
Διονύση, καλημέρα (βρέχει, κάτι κάνει φέτος, Δερβένι 102mm από 1/1/26).
Άσκηση με απαίτηση βασικών εννοιών Φυσικής.
Κρίσιμα σημεία το βραχυκύκλωμα και το μη ακαριαίο στη μεταβολή της ταχύτητας (και όχι μόνο). -
Καλημέρα Ντίνο και σε ευχαριστώ για το σχόλιο.
Καλές είναι οι βροχές, έστω και αν στιγμιαία, φέρνουν και κάποια ταλαιπωρία…
Στην Αθήνα, τις τελευταίες μέρες.. .τίποτα, αλλά δυτικά (Ιόνιο μεριά…) μου λένε ότι το έχει παρακάνει!!!! -
Καλημέρα Διονύση
Πολύ καλή η διευρένιση στους ρυθμούς μεταβολής και άκρως διδακτική που απαιτεί κατανόηση φυσικής. -
Καλησπέρα Διονύση. Διδακτική η άσκησή σου που θίγει βασικές έννοιες απαραίτητες στη φαρέτρα γνώσεών του υποψηφίου.
Το βραχυκύκλωμα που λέει και ο Ντίνος είναι κομβικό σημείο για τη λύση της άσκησης.
Πολλοί μαθητές δεν το παίρνουν είδηση…
Τα ερωτήματα που θέτεις είναι εύστοχα ως συνήθως.
Μια φορά Δάσκαλος για πάντα Δάσκαλος! -
Χρήστο και Πρόδρομε, καλό απόγευμα και σας ευχαριστώ για το σχολαισμό.
Είπα να ξικινήσω την επαγωγή με κάτι από τα πολύ γνωστά και σίγουρα διδαγμένα, (ρυθμοί μεταβολής), για να δοθεί η ευκαιρία τους μαθητές, να δουν αν τα έχουν εμπεδώσει ή τα έχουν μάθει τυπικά… -
Καλησπέρα Διονύση. Τι σου κάνει ένας διακόπτης. Πριν ήταν αρκετή η δύναμη για να παρέχει στο σύστημα την ηλεκτρική ενέργεια, αλλά μετά χρειάζεται να “τραβάει” και από την κινητική ενέργεια για να δώσει την ηλεκτρική ενέργεια που χρειάζεται το κύκλωμα. Μάλιστα, πριν υπολογίσουμε το ρυθμό dK/dt φαίνεται ότι η δύναμη Laplace μετασχηματίζει περισσότερη ενέργεια από ότι παίρνει…
Όσον αφορά τη βροχή, εδώ στην Πάτρα δε λέει να σταματήσει. Στην Ακτή Δυμαίων, παραλιακός δρόμος, χρειάζεται φουσκωτό. Συσκέψεις επί συσκέψεων Περιφέρεια, Δήμος, Λιμενικό, χρόνια τώρα: “Μα γιατί γεμίζει νερά;”
Η θάλασσα είναι στα 100m. Κάποια αυλάκια με σχάρες δε θα έκαναν τη δουλειά; 🙁
-
-
H/o Παναγιώτης Κουτσομπόγερας έγραψε ένα νέο άρθρο πριν από 2 μήνες
Μερική εξουδετέρωση μείγματος ασθενών βάσεων
 Αναμιγνύουμε τα παρακάτω 3 διαλύματα: Υ1: 400 mL διαλύματος αμίνης Α: R₁NH₂ 0,1 M Υ2: 200 mL διαλύματος αμίνης Β: R₂NH₂ 0,2 M Υ3: 400 mL διαλύμ […]
Αναμιγνύουμε τα παρακάτω 3 διαλύματα: Υ1: 400 mL διαλύματος αμίνης Α: R₁NH₂ 0,1 M Υ2: 200 mL διαλύματος αμίνης Β: R₂NH₂ 0,2 M Υ3: 400 mL διαλύμ […]-
Καλησπέρα Παναγιώτη. Η συγκέντρωση του HCl δεν χρειάζεται ή ξέχασες να τη γράψεις;
-
Καλησπερα Θοδωρή, είναι εμμέσως ζητούμενη για το pH αργοτερα – δινονται το ποσοστα (%) των βάσεων RNH₂ που αντέδρασαν
-
Καλησπερα Δημητρη, για σταδιακη εισαγωγη στην ασκηση και περαιτερω εξοικειωση με τους λογαριθμους
-
Παναγιώτη καλησπέρα. Γιατί ζητάς το pH αφού δίνεις τη συγκέντρωση των ΟΗ;
Επίσης, το ποσοστό που δίνεις για τις βάσεις, σε τι αφορά; Στην αντίδραση με το HCl ή στο συνολικό φαινόμενο και με τους ιοντισμούς; Δεν είναι ξεκάθαρο τι ακριβώς έχουμε ως δεδομένο. -
ΑΠΑΝΤΗΣΕΙΣ:
1. pH τελικού διαλύματος (πρώτη ανάμιξη)
pH = 10,7
2. Σταθερά Kb(R₁NH₂)
Kb1 = 4 * 10⁻⁴
3. Σταθερά Kb(R₂NH₂)
Kb2 = 6,25 * 10⁻⁴
4. pH διαλύματος Υ3
pH = 1
5. Συντακτικοί Τύποι (Σ.Τ.) των αμινών
Αμίνη Α: CH₃NH₂
Αμίνη Β: CH₃CH₂NH₂
6. Ευκολότερη υγροποίηση
Η αμίνη Β (CH₃CH₂NH₂), λόγω μεγαλύτερης σχετικής μοριακής μάζας – ισχυρότερων δυνάμεων London.
7. pH μετά την προσθήκη 800 mL Υ3 και συμπύκνωση στο 1 L
pH = 5,9 -
Δημητρη καλησπερα, το ποσοστό (%) της βάσης RNH₂ αναφερεται στην αντιδραση με το HCl – ιοντισμο δεν θα ειχαμε ουτως ή άλλως;
-
Παναγιώτη καλησπέρα. Αναρτώ τις απαντήσεις μου. Αυτή είναι η πρώτη σελίδα:
-
και αυτή είναι η δεύτερη. Έχουμε μια μικρή διαφορά στο τελευταίο ερώτημα.
Η ερώτησή μου Παναγιώτη αφορά στο εξής. Για να λύσουμε την άσκηση θεωρούμε ότι έχουμε δύο ρυθμιστικά και οι συγκεντρώσεις τους είναι αυτές που προκύπτουν από τις αντιδράσεις με το HCl. Ωστόσο, όπως φάνηκε στη συζήτηση για τα οξέα, μπορούμε να θεωρήσουμε ότι γίνονται επιπλέον αντιδράσεις. Οπότε προφανώς το ποσοστό αλλάζει (έστω και κατά πολύ λίγο). Αλλά μάλλον δεν έχει ιδιαίτερο ενδιαφέρον το τόσο πολύ σκάλισμα. Και πάλι συγχαρητήρια για τις ασκήσεις σου. -
Παναγιώτη και Δημήτρη καλησπέρα.
Παναγιώτη συγχαρητήρια για τις όμορφες ασκήσεις ιοντικής που ανεβάζεις. Μια παρατήρηση μόνο σχετικά με τις προσεγγίσεις. Στην 2η αμίνη (αιθυλαμίνη) Kb/C= 0.0156 > 0.01. Δεν ασχολήθηκα βέβαια να υπολογίσω το σφάλμα που προκύπτει.
Δημήτρη συμφωνώ με τα αποτελέσματα που έβγαλες, εκτός από το 7ο . Εμένα μου βγαίνει (x+c)^2=1.64*10^-12, x+y=ρίζα1,64*10^-6 και ph=6-0.107=5.89 -
Καλησπερα Δημητρη και Ανέστη κι ευχαριστω για τον χρονο και τα σχολια σας – δικο μου λαθος για το 7ο ερωτημα, πρέπει να δωσω οτι log164=2,2 οποτε το pH βγαινει 5,9.
1. Υπολογισμός moles
· Αμίνη Α (R1NH2): n = C * V = 0,1 M * 0,4 L = 0,04 mol.
· Αμίνη Β (R2NH2): n = C * V = 0,2 M * 0,2 L = 0,04 mol.
· HCl (από το Υ3): n = C * V = 0,1 M * 0,8 L = 0,08 mol.
2. Αντίδραση Εξουδετέρωσης
Προσθέτοντας το HCl, οι δύο βάσεις αντιδρούν πλήρως:
R1NH2 + HCl -> R1NH3Cl
R2NH2 + HCl -> R2NH3Cl
Συνολικά moles βάσεων = 0,04 + 0,04 = 0,08 mol.
Moles HCl = 0,08 mol.
Επειδή τα moles είναι ίσα, έχουμε πλήρη εξουδετέρωση. Στο διάλυμα υπάρχουν μόνο τα άλατα των αμινών (τα συζυγή τους οξέα R1NH3+ και R2NH3+).
3. Συγκεντρώσεις και Σταθερές (στο 1 L)
· Συγκέντρωση άλατος Α (C1): 0,04 mol / 1 L = 0,04 M.
· Συγκέντρωση άλατος Β (C2): 0,04 mol / 1 L = 0,04 M.
· Σταθερά Ka1: Kw / Kb1 = 10^-14 / (4 * 10^-4) = 2,5 * 10^-11.
· Σταθερά Ka2: Kw / Kb2 = 10^-14 / (6,25 * 10^-4) = 1,6 * 10^-11.
4. Υπολογισμός [H3O+]
Για μείγμα δύο ασθενών οξέων:
[H3O+] = ρίζα( Ka1C1 + Ka2C2 )
[H3O+] = ρίζα( 2,510^-11 * 0,04 + 1,610^-11 * 0,04 )
[H3O+] = ρίζα( 0,04 * (2,510^-11 + 1,610^-11) )
[H3O+] = ρίζα( 0,04 * 4,1 * 10^-11 )
[H3O+] = ρίζα( 0,164 * 10^-11 ) = ρίζα( 1,64 * 10^-12 )= ρίζα( 164 * 10^-14 )
5. Υπολογισμός pH
pH = 7 – 2,2/2
pH = 5,9Ανεστη σωστη η παρατηρηση σου επισης – μου διεφυγε – θα αλλαχτει, ισως και με το ΕΚΙ να μειωθει εντος οριων ο βαθμος ιοντισμου της αμινης, ευχαριστω πολυ και παλι για τις ορθες παρατηρησεις σας
-
Τελικά το έκανα το αριθμητικό. Έχω γράψει 5/8 Χ 10^-4 αντί του σωστού 5/8Χ10^-3.
-
Παναγιώτη καλησπέρα και πάλι. Όντως λόγω ΕΚΙ το y θα μικρύνει και το σφάλμα τελικά είναι πολύ μικρό. Απλώς μπορεί να προβληματίσει τους μαθητές
-
-
H/o Ανδρέας Ριζόπουλος έγραψε ένα νέο άρθρο πριν από 2 μήνες
Δυο πειράματα με δακτύλιους
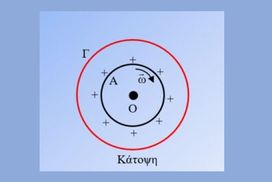 Πείραμα 1ο Όπως φαίνεται στην κάτοψη του διπλανού σχήματος, δύο ομόκεντροι δακτύλιοι, Α από μονωτικό υλικό και Γ από μέταλλο, τοποθετούν […]
Πείραμα 1ο Όπως φαίνεται στην κάτοψη του διπλανού σχήματος, δύο ομόκεντροι δακτύλιοι, Α από μονωτικό υλικό και Γ από μέταλλο, τοποθετούν […]-
Καλό μεσημέρι Ανδρέα.
Προχωρημένα περιβάλλοντα έχει το σημερινό μενού!
Βλέπω προχωράτε στην επαγωγή… -
Γεια σου Ανδρέα, ωραίος ο τρόπος να δημιουργηθεί μεταβαλλόμενο ρεύμα και ΗΕΔ από επαγωγή.
-
Καλημέρα συνάδελφοι. Ευχαριστώ για τα σχόλια.
Διονύση έτσι όπως έχει γίνει πλέον το σχολείο, δεν ξέρουμε κάθε βδομάδα πόσες ώρες θα χαθούν για διάφορες δράσεις, οπότε προχωράμε και βλέπουμε…
Παύλο ήθελα δυο διαφορετικούς τρόπους μεταβολής ροής στο ίδιο πρόβλημα, για να συγκρίνουν οι μαθητές. -
Καλησπέρα Ανδρέα και συγχαρητήρια για την άσκηση!!
Απαιτείται παραγωγική και συνθετική σκέψη ,κάτι που…ξεχωρίζει την ήρα από το στάρι.
Πρέπει να υπάρχει κάποιο τέτοιο θέμα στις πανελλήνιες.
Νάσαι καλά.
-
-
H/o Αποστόλης Παπάζογλου έγραψε ένα νέο άρθρο πριν από 2 μήνες
Πώς θα κινηθεί η ράβδος;
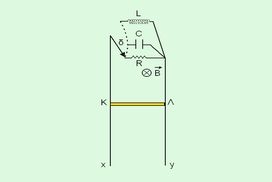 Δύο κατακόρυφοι μεταλλικοί αγωγοί χωρίς αντίσταση απέχουν απόσταση d και βρίσκονται σε οριζόντιο ομογενές μαγνητικό πεδίο, κάθετο στο επίπεδο των αγωγών, μ […]
Δύο κατακόρυφοι μεταλλικοί αγωγοί χωρίς αντίσταση απέχουν απόσταση d και βρίσκονται σε οριζόντιο ομογενές μαγνητικό πεδίο, κάθετο στο επίπεδο των αγωγών, μ […] -
H/o Διονύσης Μάργαρης έγραψε ένα νέο άρθρο πριν από 2 μήνες
Κλείνοντας έναν – έναν τους διακόπτες.
 Στο κύκλωμα του διπλανού σχήματος, οι διακόπτες είναι ανοικτοί, τα όργανα ιδανικά, ενώ δίνονται για την πηγή, ΗΕΔ Ε=20V και r=2Ω, ενώ οι δυο αντιστάτε […]
Στο κύκλωμα του διπλανού σχήματος, οι διακόπτες είναι ανοικτοί, τα όργανα ιδανικά, ενώ δίνονται για την πηγή, ΗΕΔ Ε=20V και r=2Ω, ενώ οι δυο αντιστάτε […]-
Γεια σου Διονύση πολύ όμορφη και χρήσιμη ανάρτηση. Με μια άσκηση μελετάς πως επηρεάζει ενα κύκλωμα το κλείσιμο του διακόπτη σε συνδυασμό και με βραχυκύκλωμα.
-
Καλημέρα Παύλο και καλή Κυριακή.
Σε ευχαριστώ για το σχολιασμό και χαίρομαι που σου άρεσε. -
Καλημέρα Διονύση, τώρα που πέρασε το “εορταστικό” τριήμερο, όλοι οι “αναξιοπαθούντες” , vegan, προληπτικοί, μη-“ερωτευμένοι”, αναμένοντας
το αποκριάτικο “ξεφάντωμα”…. απολαμβάνουν φυσική, main stream και alternativeΑν και στην προσωπική ζωή οι επιλογές μου ήταν σχεδόν πάντα alternative, στην
φυσική προτιμώ main stream επιλογές…Μία τέτοια είναι και η παραπάνω ανάρτησή σου, με ουσιαστικό διδακτικό αποτύπωμα.
Συμπληρώνω κάτι που ξέχασες να γράψεις
ι) όταν (δ1) κλειστός, η ισχύς της πηγής Pηλ=EI(2)=80W,
ii) όταν (δ1) και (δ2) κλειστοί, η ισχύς της πηγής Pηλ=EI(β)=200W
Θα πρόσθετα ως ερώτημα,
“σε ποια από τις τρεις περιπτώσεις η πηγή αποδίδει στο φορτίο των 3C συντομότερα, την ενέργεια που υπολογίστηκε”
Ελπίζοντας σε ένα repeat της χθεσινής νίκης-εμφάνισης και στο βασικό οπαδικό άθλημα στη συμπρωτεύουσα
-
Καλό μεσημέρι Θοδωρή και σε ευχαριστώ για το σχόλιο και την… υπενθύμιση!
Το ερώτημα που πρότεινες το πρόσθεσα, στο τέλος…
-
-
H/o Χρήστος Αγριόδημας έγραψε ένα νέο άρθρο πριν από 2 μήνες
Παράλληλα επιβραδύνεται, σε σειρά επιταχύνεται…
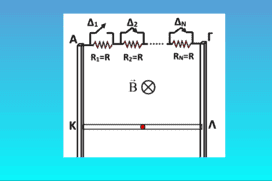 Ένας ομογενής αγωγός ΚΛ μήκους ℓ, μάζας m και μηδενικής ωμικής αντίστασης βρίσκεται σε επαφή με δύο κατακόρυφους μεταλλικούς οδηγούς Ay1 και Γy2 που έχο […]
Ένας ομογενής αγωγός ΚΛ μήκους ℓ, μάζας m και μηδενικής ωμικής αντίστασης βρίσκεται σε επαφή με δύο κατακόρυφους μεταλλικούς οδηγούς Ay1 και Γy2 που έχο […]-
Δεν είναι στα πλαίσια εξετάσεων, αλλά έχει την πλάκα της.
-
Καλημέρα Χρήστο και καλές απόκρηες!
Τι έφτιαξες!!!
Αν δεν είχαμε Ν διακόπτες αλλά 2, δεν θα ήταν και θέμα εξετάσεων; -
Καλημέρα Διονύση, καλές απόκριες.
Το εχω ήδη έτοιμο με δύο αντιστάσεις σαν β θεμα. ..
Θα δημοσιευθεί και εδω ή σε διαγωνισμα αν μπει ή μονο του. -
Καλημέρα, πολύ ωραία ανάλυση Χρήστο!
-
Σε ευχαριστώ Παύλο.
Να σαι καλά -
Καλησπέρα Χρήστο. Πολύ δουλειά! Μετά από αυτήν την άσκηση, το θέμα “κλείνει ο διακόπτης” έκλεισε. Η light έκδοση με δυο διακόπτες θα είναι καλό β΄ θέμα, πιο μαθητικό, οπότε την αναμένουμε.
-
Αντρέα καλησπέρα.
Σε ευχαριστώ για το σχόλιο. Να σου πω την αλήθεια και εγώ προτιμώ την πιο απλή διάταξη.
-
-
H/o Διονύσης Μάργαρης έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Άλλη μια ισορροπία αγωγού.
 Ο ευθύγραμμος αγωγός ΑΔ του σχήματος έχει μάζα m=0,4kg, μήκος l=0,8m και κρέμεται κατακόρυφα από δύο ελατήρια, με το ίδιο φυσικό μήκος. Ό […]
Ο ευθύγραμμος αγωγός ΑΔ του σχήματος έχει μάζα m=0,4kg, μήκος l=0,8m και κρέμεται κατακόρυφα από δύο ελατήρια, με το ίδιο φυσικό μήκος. Ό […]-
Σαράντα++ μάλλον πενήντα – χρόνια φούρναρης ξέρεις πως με απλά υλικά να φτιάχνεις ζυμωτό ψωμί, τέτοιο ώστε …. να τρώει ο πατέρας και του παιδιού να μην δίνει….
Προφανώς αναφέρομαι στο (iv) ερώτημα και στη διερεύνηση που κάνειςΕυχαριστούμε
-
Καλημερα Διονυση. Ωραια ασκηση μηχανικης με ολιγον απο δυναμη Laplace. Eνα ερωτημα που ισως θα μπορουσε να κανει ενας μαθητης ειναι πως ξερουμε οτι η δυναμη Laplace εφαρμοζεται στο μεσον το αγωγου.Η εξηγηση ειναι μεν απλη αλλα δεν θυμαμαι αν το σχολικο γραφει κατι επ αυτου.
-
Καλημέρα Θοδωρή, καλημέρα Κωνσταντίνε και σας ευχαριστώ για το σχολιασμό.
Θοδωρή, αν λάβεις υπόψη σου ότι από το 2ο έτος του πανεπιστημίου, έκανα ιδιαίτερα μαθήματα, πέρασα πια τα 50 χρόνια!!!
Βέβαια συμπληρώνω 12 χρόνια, που έχω σταματήσει κάθε είδους διδασκαλία… Οπότε δεν ξέρω αν πρέπει να κάνουμε αφαίρεση…
Κωνσταντίνε, με μια πρώτη ματιά στο σχολικό, βλέπω να έχεις δίκιο!!!
Δεν βρήκα να γράφει κάτι για το σημείο εφαρμογής της δύναμης Laplace…
Ίσως επειδή, όταν γράφονταν τα βιβλία, οι συγγραφείς ήξεραν ότι όλοι οι μαθητές θα διδάσκονταν στη γ.π. τα βασικά του ηλεκτρομαγνητισμού.
Έτσι στη φυσική της γενικής παιδείας διαβάζουμε:https://i.ibb.co/b5Yy7pCM/aa.png
Κόψε από εδώ, άλλαξε το άλλο, τροποποίησε το τρίτο, άντε να μην δημιουργούνται κενά και να μπορεί να υπάρξει σοβαρή διδασκαλία…
-
Καλησπέρα Διονύση. Πολύ καλή για επανάληψη. Η Laplace είναι ένα μικρό μέρος της ανάρτησης, στην οποία κυριαρχεί η ισορροπία στερεού, με το 4ο ερ΄ωτημα εξαιρετικό.
Σε αυτό που λέει τώρα ο Κωνσταντίνος, ας σκεφτούμε πόσες ασκήσεις κυκλοφορούν με τμήμα αγωγού εντός πεδίου, που η επίσημη θεωρία δεν υποστηρίζει!
Αν θεωρήσουμε ότι η Φυσική Γενικής το καλύπτει, γιατί να μην είναι στην ύλη π.χ. και οι πυκνωτές; -
Καλησπέρα Διονύση
Εξαιρετική ασκηση και βέβαια το 4ο ερώτημα είναι ο πρωταγωνιστής.
Θοδωρή όσα χρόνια και αν περάσουν άλλα τα μάτια του λαγού… -
Καλημέρα Ανδρέα, καλημέρα Χρήστο και καλό ΣΚ.
Σας ευχαριστώ για το σχολιασμό.
ΥΓ
Γιορτάζετε σήμερα; Να ευχηθώ χρόνια πολλά!!! -
Καλημέρα Διονύση,, ρωτάς για τα τελευταία 12 χρόνια;
Με 4500 αναρτήσεις και όσα έχεις “υποφέρει” από διάφορους “επιστήμονες”,
όχι μόνο μετράνε, αλλά είναι “βαρέα και ανθυγειανά”Επίσης, σήμερα νομίζω πως “γιορτάζουν” όλοι
-
Καλό μεσημέρι Θοδωρή.
Πετυχημένο σύνθημα…
-
-
H/o Παύλος Αλεξόπουλος έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
-
Καλησπέρα Παίλο. Πολύ όμορφη! Μια παρόμοια προσεγγιση φορμαλιστική.
Καταλήγει ότι αυτος ο λόγος είναι ανεξάρτητος της γωνίας κλίσης φ:https://i.ibb.co/tMBsZpJz/feb-90.png -
Γεια σου Γιώργο χαίρομαι που σου αρέσει και σε ευχαριστώ πολύ για την αναλυτική σου λύση και για τα πολύ όμορφα συμπεράσματα που κατέληξες, να είσαι καλά!
-
Καλημέρα Παύλο. Ωραία άσκηση για το ρόλο της στατικής τριβής. Για πολύ καλούς μαθητές προφανώς, γιατί οι περισσότεροι δεν καταλαβαίνουν το ρόλο της στατικής τριβής οπυτε στο βάδισμα.
Έφτιαξα και ένα i.p. ΕΔΩ
Βλέπουμε ότι η στατική τριβή- σε λείο κεκλιμένο παραμενει μηδενική και στην κάθοδο.
- σε τραχύ κεκλιμένο αλλάζει φορά στην κάθοδο.
-
Καλημέρα και καλο Σαββατοκύριακο. Ανδρεα χαίρομαι που σου αρέσει η άσκηση και σε ευχαριστώ πολύ για το ip.
-
H/o Παναγιώτης Κουτσομπόγερας έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Μερική εξουδετέρωση μείγματος ασθενών οξέων
 ΕΚΦΩΝΗΣΗ 1 Αναμιγνύονται τα παρακάτω 3 διαλύματα: 500 mL διαλύματος CH3COOH 0,1 M 200 mL διαλύματος HCOOH 0,25 M 100 mL διαλύματος NaOH […]
ΕΚΦΩΝΗΣΗ 1 Αναμιγνύονται τα παρακάτω 3 διαλύματα: 500 mL διαλύματος CH3COOH 0,1 M 200 mL διαλύματος HCOOH 0,25 M 100 mL διαλύματος NaOH […]-
Παναγιώτη καλησπέρα. Στα άδυτα της ιοντικής! Βρήκα pH=4 και (100/6)%. Οπότε μπορούμε να πούμε κατευθείαν ότι το ποσοστό του άλλου οξέος, του HCOOH, που αντέδρασε είναι (500/6)%. Αυτό δεν ισχύει πάντα όμως, έτσι; Δηλαδή το άθροισμα των δύο ποσοστών να είναι 100%.
-
Θοδωρη ταχυτατος, μπραβο (και ηθελα να κανω αλλαγες …κλαψ) νομιζω οτι αλγεβρικα και χημικα πρεπει το άθροισμα των δύο ποσοστών να είναι 100%.
-
Έχει πέσει ανάλογη το 2020 στις επαναληπτικές πανελλαδικές του παλαιού συστήματος!! Είναι πλεόν λίγο (έως πολύ) too much νομίζω!
-
ακριβως (ειναι too much, αλλα happy brainwork!) – κι εγω απο εκει την θυμηθηκα
-
Νομίζω Παναγιώτη ότι το άθροισμα των ποσοστών δεν είναι πάντα 100%. Είναι μόνο όταν η βάση είναι σε στοιχειομετρική αναλογία με καθένα από τα δύο οξέα.
-
αν υπολογισεις και το ποσοστο του HCOOH εδω νομιζω ειναι 5/6 (αν εχω καταλαβει τι εννοεις)
-
Επειδή το’χα ψάξει παλαιότερα, με αφορμή την ερώτηση μιας μαθήτριας!!, θυμάμαι ότι όταν τα αρχικά mol της βάσης είναι σε στοιχειομετρική αναλογία με τα αρχικά mol κάθε οξέος, όπως εδώ που είναι 1:1 με κάθε οξύ, αφού τα αρχικά mol όλων είναι 0,05, τότε ισχύει ότι το άθροισμα είναι 100%. Αν όμως τα mol της βάσης δεν ήταν 0,05 αλλά π.χ. 0,07, τότε το άθροισμα δεν είναι 100%.
-
Καλησπέρα Θοδωρή, πολύ σωστή η παρατήρηση σου
-
Έτσι θυμάμαι. Αν το δοκιμασουμε θα το επιβεβαιώσουμε. Απλά τώρα βαριέμαι να μπω σε πράξεις.
-
Παναγιώτη καλημέρα. Και πάλι ωραίος. Νασαι καλά, να γράφεις.
-
Καλημέρα κύριε Παπαστεργιάδη, εξαιρετικη η λύση, ευχαριστουμε πολυ – οι τιμες των σταθερων επιλεγονται για την πιο ευκολη
αλγεβρικη επιλυση, σε μια ‘φορτωμενη’ ουτως ή άλλως ασκηση. Να ειστε καλα -
Καλημερα αγαπητε Δημητρη, ευχαριστω που αντεξες και διαβασες την ασκηση – να εισαι πάντα καλα – περιμενω και το δικο σου πόνημα !
-
Παναγιώτη και πάλι για σου. Πώς θα σου φαινόταν η ακόλουθη πρόταση: Το φορμικό είναι ισχυρότερο οξύ, οπότε θα αντιδράσει πλήρως και θα περισσέψει όλο το οξικό. Άρα, συντελεστής μετατροπής του οξικού 0%.
-
Καλησπέρα σε όλους. Δημήτρη ανάβεις φωτιές! Για να το πεις αυτό πρέπει η Ka των δύο οξέων να διαφέρει σημαντικά, συνήθως 2 τάξεις μεγέθους και πάνω. Αν η ισχύς ειναι παραπλήσια, δεν … Τουλάχιστον αυτό ξέρω εγώ!
-
Καλησπέρα Δημήτρη – ειναι μια προταση που έχει περάσει πιθανώς απο το μυαλο ολων μας – ειδικοτερα αν ειχαμε μαζι ενα ισχυρο κι ενα σθενες οξυ, αν συμφωνεις – νομιζω ομως οτι τα OH- δεν μπορουν να ‘διακρινουν’ την προελευση των H3O+, αρα μαλλον θα εξουδετερωθουν και τα 2 οξεα, με μια μικρη ‘προτιμηση’ οπως φαινεται στο πιο ισχυρο απο τα 2 οξεα.
-
Η σκέψη μου Παναγιώτη βασίζεται σε κάτι άλλο. Αν υποθέσουμε ότι έχουμε ένα διπρωτικό οξύ. Στην ογκομέτρηση δεν περιμένουμε να έχουμε δύο ισοδύναμα σημεία; Κατανάλωση για τη μία μορφή, και μετά για την άλλη. Το γεγονός ότι έχουμε δύο οξέα, από την άποψη της αντίδρασης με τα ιόντα υδροξειλίου, δεν παρουσιάζει κάποια διαφορά. Τι λες;
-
Δημήτρη είδες την απάντηση μου;
-
Θοδωρή καλησπέρα. Μόλις τώρα έχω πάλι επαφή με υπολογιστή και διάβασα τα σχόλια. Εξακολουθώ να έχω την ίδια απορία. Όταν αντιμετωπίζουμε μια ογκομέτρηση διπρωτικού οξέος, με δύο ισοδύναμα σημεία, ολοκληρώνεται ο ένας ιοντισμός και μετά παίρνουμε τον δεύτερο (γι’ αυτό και δύο ΙΔ, συνοπτικά φυσικά αυτό που γράφω). Η επίλυση της άσκησης του Παναγιώτη δεν χρησιμοποιεί τη διαφορά των Κα. Οπότε το ερώτημα είναι γιατί η διαφορετική προσέγγιση στα δύο προβλήματα;
Τώρα όσον αφορά στη διαφορά των Κα Θοδωρή σου στέλνω μια παραπομπή και να μου πεις τη γνώμη σου. (Simultaneous determination of mixtures of acids by potentiometric titration, https://doi.org/10.1016/S0003-2670(98)00185-8) -
…..η γνώμη μου είναι επίσης ότι η βασική ιδέα της ανάρτησης για τους μαθητές είναι να χειρίζονται τα εν λόγω δεδομένα για εξοικείωση κυρίως και λιγότερο να μπορούν να αιτιολογήσουν την διαφορά στα πολυπρωτικα οξέα και στα μείγματα οξέων
-
Καλησπέρα , ίσως να παίζει ρόλο και το ακόλουθο: Στα πολυπρωτικά οξέα υπάρχει μεγάλη διαφορρά μεταξύ των διαδοχικών Ka (Ka1 >> Ka2 >> Ka3). Κάθε αποπρωτονίωση αυξάνει το αρνητικό φορτίο της χημικής οντότητας, οπότε η επόμενη γίνεται πολύ δυσκολότερα. Γι’ αυτό η εξουδετέρωση γίνεται διαδοχικά και εμφανίζονται ξεχωριστά στάδια.
Σε ένα μείγμα δύο διαφορετικών οξέων, όπως εδώ οι τιμές Ka είναι συνήθως πιο κοντινές και τα οξέα είναι ανεξάρτητα μεταξύ τους. Έτσι συμβάλλουν ταυτόχρονα στο pH και η βάση κατανέμεται μεταξύ τους, οδηγώντας σε παράλληλη μερική εξουδετέρωση.
-
Παναγιώτη ευχαριστώ για την απάντηση. Όσον αφορά την αξία της άσκησής σου, έχεις δίκιο για τους μαθητές και τον στόχο σου.
Πάντως σκέφτομαι να λύσω την άσκηση ως εξής, μόλις βρω χρόνο. Να αντιδράσει η βάση με το ένα οξύ (ισότητα mol) και μετά να προσθέσω το 2ο οξύ και να υπολογίσω ποσοστό μετατροπής και pH. Ίσως έχει ενδιαφέρον. -
Καλησπέρα. Παναγιώτη συμφωνώ αλλά θα κάνω ακόμα ένα σχόλιο. Θωμά σε διάλυμα ασθενούς μονοπρωτικού οξέος κάνουμε προσέγγιση όταν α <= 0,1. Κάνουμε δηλαδή δεκτό σφάλμα μέχρι και 10%. Όταν κάνουμε προσεγγίσεις δεν κάνουμε “εκπτώσεις” στην επιστημονική εγκυρότητα. Οι προσεγγίσεις γίνονται ώστε, όταν δεν απαιτείται πολύ μεγάλη ακρίβεια, να απλοποιήσουμε τους υπολογισμούς.
Δημήτρη και Θωμά μεταφέρω και κάτι από το έγκυρο βιβλίο “Σύγχρονες Μέθοδοι στη Χημική Ανάλυση” των Pecsok-Shields-Cairns-McWilliam, απόδοση στα ελληνικά Σταύρος Βολιώτης, Εκδόσεις Πνευματικός : σελ. 510 “Αν οι διαδοχικές pK ενός διπρωτικού οξέος διαφέρουν κατά 3 ή περισσότερο, η καμπύλη τιτλοδότησης αποτελείται από δύο μονοπρωτικές καμπύλες. Καθώς οι τιμές pK πλησιάζουν η μία την άλλη, οι δύο καμπύλες συγχονεύονται σε μια απλή, και το ισοδύναμο σημείο του πρώτου πρωτονίου εξαφανίζεται” (έχει και τα σχετικά σχήματα). Και παρακάτω: Για να πετύχουμε ένα ικανοποιητικό τέλος τιτλοδότησης σε ένα σύστημα πολυπρωτικού οξέος, δύο τουλάχιστον διαδοχικές τιμες pK πρέπει να διαφέρουν το λιγότερο κατά 3, και το τέλος της τιτλοδότησης να γίνεται σε pH από 4 έως 10″. Νομίζω αυτά δικαιολογούν αυτά που έχω ισχυριστεί έως τώρα. -
Δημήτρη εγώ σε ευχαριστώ για τον χρόνο σου και τις ιδέες σου , τσεκαρε αυτό που λες , έχει ενδιαφέρον
-
Θοδωρή καλησπέρα.
Μάλλον με παρεξήγησες. Δεν αμφισβητώ τίποτα από αυτά που αναφέρεις. Ολόσωστα. Απλά ανέφερα το άρθρο (έπεσα πάνω του πριν από 10 ημέρες) γιατί μου έκανε εντύπωση. Προσδιορίζει ποσοτικά μίγμα οξέων, με ποτενσιομετρία, ανεξάρτητα από ka.
Έτσι κι αλλιώς, το όλο θέμα ξεκίνησε από την ερώτηση που είχα θέσει, που όμως είναι λάθος γιατί παραλείπει την επίδραση που θα έχει στο pH η προσθήκη του επόμενου οξέος.
Καλό βράδυ. -
Kαλημέρα σε όλους. Θα ήθελα να ρωτήσω πως θα υπολογίζατε το pH ενός διαλύματος στο οποίο προσθέτουμε 0,1mol CH3COOH, 0,1mol CH3COONa, 0,2mol HCOOH και 0,2mol HCOONa με τελικό όγκο 1L.
-
Καλημέρα Άγγελε (πολύ καλή ερώτηση) και στους υπολοιπους
Με Gemini ιδέες και λιγο βιαστικα
Kw = 10⁻¹⁴
Ka(CH3COOH) = 2·10⁻⁵
Ka(HCOOH) = 5·10⁻⁴
Πως θα υπολογίζατε το pH ενός διαλύματος στο οποίο προσθέτουμε 0,1mol CH3COOH, 0,1mol CH3COONa, 0,2mol HCOOH και 0,2mol HCOONa με τελικό όγκο 1L.
pH=3,3 αν γινουν οι πραξεις με το HCOOH
pH=4,7 αν γινουν οι πραξεις με το CH3COOHΓιατί δεν χρησιμοποιούμε το οξικό σύστημα;Αν δοκιμάσετε να υπολογίσετε το pH χρησιμοποιώντας το οξικό σύστημα με τις αρχικές του συγκεντρώσεις, θα βρήκατε pH = 4,7. Ωστόσο, επειδή το μυρμηκικό σύστημα απελευθερώνει περισσότερα H3O+, η ισορροπία του οξικού μετατοπίζεται προς τα αριστερά (σύμφωνα με την αρχή Le Chatelier), καταναλώνοντας οξικά ιόντα και παράγοντας αδιάστατο οξικό οξύ, μέχρι η σχέση [CH3COO-]/[CH3COOH] να προσαρμοστεί στο pH = 3,3 που επέβαλε το ισχυρότερο οξύ.
εαν θεωρησουμε
Kw = 10⁻¹⁴
Ka(CH3COOH) = 10⁻⁵
Ka(HCOOH) = 10⁻⁴έχουμε αντιστοιχα
pH=4 αν γινουν οι πραξεις με το HCOOH
pH=5 αν γινουν οι πραξεις με το CH3COOHΠροφανως μαλλον οχι καταλληλο θεμα για παιδιά
Αντιγραφω μια ασκηση του Θοδωρη Βαχλιωτη (είδες που φύλαξα το pdf;) με πιο ΄κατάλληλη διατυπωση’
Υδατικό διάλυμα Δ περιέχει τα ασθενή μονοπρωτικά οξέα ΗΑ 0,1 Μ και ΗΒ 0,5 Μ και τα άλατά τους NaA 0,2 Μ και NaB 0,1 Μ.
α. Να υπολογίσετε το pH του διαλύματος Δ. [pH=4]
β. Να συγκρίνετε την ισχύ των οξέων ΗΑ και ΗΒ. [HA>HB]
Δίνεται για το οξύ ΗΑ: Ka=2.10-4.Καλημέρα σε όλους
-
Καλησπέρα. Σε αυτήν την περίπτωση Άγγελε γίνεται η αντίδραση
HCOOH + CH3COO- <=> HCOO- + CH3COOH
με Κc = Ka(HCOOH) / Ka(CH3COOH) = 5*10^-4 / 2*10^-5 = 25.
Αν υπολογίσεις το Qc = 1 < Κc και γίνεται αντίδραση προς τα δεξιά.
Ξεφύγαμε!
-
Καλησπερα σε ολους
Δημητρη πολυ καλη η ιδεα σου.
Η τιμη του pH του διαλυματος που θα προτεινα θα ηταν 4 (όχι 4 ή 5) αν περναμε υποψη μας το γεγονος οτι το pH το καθοριζει το
ισχυρο οξυ κυριως, για τα ακολουθα δεδεομεναKw = 10⁻¹⁴
Ka(CH3COOH) = 10⁻⁵
Ka(HCOOH) = 10⁻⁴
pH ενός διαλύματος στο οποίο προσθέτουμε 0,1mol CH3COOH, 0,1mol CH3COONa, 0,2mol HCOOH και 0,2mol HCOONa με τελικό όγκο 1L.Ωστόσο μάλλον ο πιο γενικόw τροπος ειναι η επιλυση μεσω της μέθοδου του ισοζυγίου φορτίου
[H3O+] + [Na+] = [OH-] + [HCOO-] + [CH3COO-]
για τα ακολουθα δεδεομεναKw = 10⁻¹⁴
Ka(CH3COOH) = 10⁻⁵
Ka(HCOOH) = 10⁻⁴
pH ενός διαλύματος στο οποίο προσθέτουμε 0,1mol CH3COOH, 0,1mol CH3COONa, 0,2mol HCOOH και 0,2mol HCOONa με τελικό όγκο 1L.Είναι ο πιο αυστηρός επιστημονικά τρόπος για να λυθεί οποιοδήποτε πρόβλημα ιοντικής ισορροπίας, (δεν βασίζεται σε παραδοχές).
Το αποτέλεσμα που προκυπτει απο GEMINI ειναι pH=4,3
Αν παρατηρηστε ειναι κοντα στην τιμη 4 αν περναμε υποψη μας το γεγονος οτι το pH το καθοριζει το
ισχυρο οξυ κυρίως, η συνεισφορα του +0,3 οφειλεται και στην υπαρξη του CH3COOH. -
ισως εχει να κανει και με την παρουσια του CH3COONa, εχω ενσωματωσει και την απαντηση απο το gemini στα google docs
-
Καλησπέρα. Παναγιώτη μήπως το pH βγαίνει περίπου 3,7; Τόσο το υπολόγισα. Η συνεισφορά του αιθανικού πρέπει να ελαττώνει το pH κατά 0,3.
Και στο chatgtp 3,7 το βγάζει. -
ΠΡΟΒΛΗΜΑ ΙΣΟΡΡΟΠΙΑΣ ΜΕΙΓΜΑΤΟΣ ΡΥΘΜΙΣΤΙΚΩΝ ΔΙΑΛΥΜΑΤΩΝ
1. ΔΕΔΟΜΕΝΑ
· CH3COOH (Οξικό οξύ): 0,1 mol (Αρχικά)
· CH3COONa (Οξικό νάτριο): 0,1 mol (Αρχικά)
· HCOOH (Μυρμηγκικό οξύ): 0,2 mol (Αρχικά)
· HCOONa (Μυρμηγκικό νάτριο): 0,2 mol (Αρχικά)
· Τελικός όγκος: 1 L
· Ka(CH3COOH) = 10^-5 (pKa = 5)
· Ka(HCOOH) = 10^-4 (pKa = 4)
2. ΜΕΘΟΔΟΣ ΙΣΟΖΥΓΙΟΥ ΦΟΡΤΙΟΥ (Charge Balance)
Η θεμελιώδης εξίσωση για το διάλυμα είναι:
[H3O+] + [Na+] = [OH-] + [CH3COO-] + [HCOO-]
Γνωρίζουμε ότι:
· [Na+] = 0,3 M (0,1 από το οξικό + 0,2 από το μυρμηγκικό νάτριο)
· [CH3COO-] = C(ολικό1) * Ka1 / (Ka1 + [H3O+])
· [HCOO-] = C(ολικό2) * Ka2 / (Ka2 + [H3O+])
3. ΜΑΘΗΜΑΤΙΚΗ ΕΠΙΛΥΣΗ
Αντικαθιστώντας τις τιμές στην εξίσωση φορτίου (θέτοντας x = [H3O+]):
x + 0,3 = (0,2 * 10^-5) / (10^-5 + x) + (0,4 * 10^-4) / (10^-4 + x)
Με την παραδοχή x << 0,3 και λύνοντας τη δευτεροβάθμια εξίσωση που προκύπτει:
x^2 – (3 * 10^-5)x – 10^-9 = 0
Η διακρίνουσα είναι Δ = 49 * 10^-10.
Η θετική ρίζα της εξίσωσης είναι:
x = 5 * 10^-5 M
4. ΤΕΛΙΚΟ ΑΠΟΤΕΛΕΣΜΑ
[H3O+] = 5 * 10^-5 M
pH = -log(5 * 10^-5) = 5 – log5 = 5 – 0,7
pH = 4,3
5. ΕΠΑΛΗΘΕΥΣΗ ΠΟΣΟΤΗΤΩΝ (Ανά 1 Λίτρο)
Λόγω της διαφοράς ισχύος των οξέων, έγινε η αντίδραση:
HCOOH + CH3COO- <-> HCOO- + CH3COOH
Κατά την οποία αντέδρασαν περίπου 0,067 mol.
Τελικές συγκεντρώσεις ισορροπίας:
· [CH3COOH] = 0,167 M
· [CH3COO-] = 0,033 M
· [HCOOH] = 0,133 M
· [HCOO-] = 0,267 M
Επαλήθευση μέσω Henderson-Hasselbalch:
pH = 5 + log(0,033/0,167) = 4,3
pH = 4 + log(0,267/0,133) = 4,3 -
Παναγιώτη καλημέρα. Αναρτώ την απάντηση που σου ανέφερα. Ίσως έχει κάποιο ενδιαφέρον. Για την απάντησή σου στον Άγγελο, δεν κατάλαβα κάτι. Όταν υπολογίζεις το pH με το HCOOH παίρνεις μία τιμή και με το CH3COOH παίρνεις άλλη; Αν λες αυτό δεν μπορεί να είναι σωστό. Το pH έχει μία τιμή. Μήπως κάτι δεν κατάλαβα;
https://i.ibb.co/Rknk0qHJ/23d.jpg -
Με πιο ακριβείς τιμές Ka βγαίνει πιο κάτω. Το chatgtp με Κα=10-4 και 10-5 το βγάζει 3,8 το pH.
-
Τώρα μου το βγάζει 4,15 το chatgtp. Μάλλον εσύ έχεις δίκιο Παναγιώτη
-
Άγγελε καλησπέρα. Και εγώ pH 3,7 βρήκα λύνοντας τη δευτεροβάθμια. Αλλά το chatgtp δίνει άλλο αποτέλεσμα. Δεν ξέρω ποια είναι η ακριβής τιμή.
-
Θα ήταν καλό αν μπορούσαμε να το ελέγξουμε πειραματικά. Στα σχολικά εργαστήρια βέβαια δεν διαθέτουμε τα αντιδραστήρια αλλά και τα πεχάμετρα δεν είναι πλέον βαθμονομημένα.
-
Παναγιώτη καλημέρα. Μία ερώτηση. Στη λύση που παραθέτεις γράφεις: [CH3COO-] = C(ολικό1) * Ka1 / (Ka1 + [H3O+]). Πώς προκύπτει αυτό και τι είναι το C(ολικό1). Ευχαριστώ.
-
Δημητρη, απο gemini:
Στην άσκησή μας, βάλαμε 0,1 mol CH3COOH και 0,1 mol CH3COONa. Άρα: C(ολικό1) = 0,1 + 0,1 = 0,2 M.
Ξεκινάμε από τη σταθερά ιοντισμού (Ka): Ka = [H3O+] * [CH3COO-] / [CH3COOH] (Σχέση 1)
Και από το ισοζύγιο μάζας (αυτό που είπαμε παραπάνω): C(ολικό) = [CH3COOH] + [CH3COO-] (Σχέση 2)
Από τη Σχέση 2, λύνουμε ως προς το αδιάστατο οξύ: [CH3COOH] = C(ολικό) – [CH3COO-]
Αντικαθιστούμε αυτό στη Σχέση 1 (της Ka): Ka = [H3O+] * [CH3COO-] / (C(ολικό) – [CH3COO-])
Κάνουμε χιαστί: Ka * (C(ολικό) – [CH3COO-]) = [H3O+] * [CH3COO-] Ka * C(ολικό) – Ka * [CH3COO-] = [H3O+] * [CH3COO-]
Μεταφέρουμε το [CH3COO-] στο ίδιο μέλος: Ka * C(ολικό) = [H3O+] * [CH3COO-] + Ka * [CH3COO-]
Βγάζουμε κοινό παράγοντα το [CH3COO-]: Ka * C(ολικό) = [CH3COO-] * ([H3O+] + Ka)
Λύνουμε ως προς [CH3COO-] και έχουμε τον τύπο μας: [CH3COO-] = C(ολικό) * Ka / (Ka + [H3O+])
-
Τα είχαμε πεί κάποτε Θοδωρή …
https://i.ibb.co/fZg22qF/2427c064-3bf4-4ee4-a5f4-9cf034230fe2-1771149658-2037.jpg
-
Θοδωρή κι εγώ βγάζω 4,15. Επισυνάπτω τη λύση μου. Άλλαξα τους συβολισμούς των οξέων για συντομία.
-
Συγνώμη που καθυστέρησα λόγω υποχρεώσεων να απαντήσω. Θοδωρή κι εγώ όταν υπέβαλα το ερώτημα στο forum, είχα προσεγγίσει το θέμα σαν ισορροπία των 4 ειδών, αλλά το είχα συνεχίσει εκεί που είπες ότι ξεφύγαμε με επίλυση δευτεροβάθμιας, αλλά την είχα πάρει ανάποδα με Kc=0,04, βρήκα ότι θα πάει αριστερά κατά 0,082mol και κατέληξα σε pH=3,7. Στο ίδιο αποτέλεσμα καταλήγει και το pHsolver του webqc.org η οποία είναι η μόνη μηχανή υπολογισμού pH που βρήκα (από όσες έψαξα) που δέχεται πολλά συστατικά στο διάλυμα.
https://i.ibb.co/qF3sJTnm/Screenshot-2026-02-14-220440-1771099919-4707.png
-
Καλησπέρα. Αντώνη δεν έχεις βάλει λάθος τη συγκέντρωση του HCOOH στην Ka; Είναι 0,1175 όχι 0,0175. Αν βάλεις 0,1175 βγαίνει pH 3,7.
ΥΓ: Πολλά είχαμε πει κάποτε, αλλά μπορούμε να πούμε κι άλλα … Αν θες …
-
Νομίζω αυτό έχω βάλει … να σου πω την αληθεια “ούτε που με νοιάζει”. Η άσκηση λύνεται ως ΧΙ κτλ και καταλήγουμε σε “εκεινο” το θέμα των πανελληνίων ( επί δεσμών ) που είχε τις ουσίες ( ή εννοούσε ότι είχε ) σε ισορροπία.
Το μόνο ενδιαφέρων που θα συζητούσα θα ήταν η ποιοτική μελέτη της σύγκρισης της τιμής της Qc ( 1 ) με την Kc ( 25 ). Μοιάζει αυτή η διαφορά να μην είναι αρκετή για να θεωρήσουμε μια ισορροπία ώς μονόδρομη ( μεταφέροντας το 10 % της αποδεκτής προσέγγισης της ισοντικής στη “μοριακή” ισορροπία ).
Θα το ψάξω ( λέμε τώρα ).
Για αρχή πρέπει να βρούμε την ανάρτηση που είχε αναδείξει το θέμα πριν από ( 100 ? ) χρόνια. Νομίζω συντάκτης ήταν ο Ελευθερίου ( ή ο Πολυνίκης ) με τίτλο “ανάμειξη ρυθμιστικων δ/των ).
Θα δώσω 5 min στην αναζήτηση … ( αλλά βαριέμαι :-).
-
Την βρήκα … 2010 !!! …. 15 χρόνια πριν …
Ακόμα ανακαλύπταμε τη χημεία ( Τι βλακείες γράφαμε ).
-
Μια συνάδελφος φιλόλογος, πιο έμπειρη από εμένα τότε, μου είχε πει πριν από χρόνια: “Αγοράκι μου, αν δεν βγάλεις ρυτίδες μερικά πράγματα δεν…” Αυτό που με ανησυχεί είναι ότι, ακόμα, δεν έχω βγάλει ρυτίδες! Χαχα
-
-
H/o Παναγιώτης Κουτσομπόγερας έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Πορφυρογέννητοι βασιλιάδες, ταπεινά κοχύλια και Br
 Το Βυζάντιο συνδέθηκε όσο λίγοι πολιτισμοί με το χρώμα και τον συμβολισμό του. Η περίφημη πορφύρα ήταν κάτι πολύ περισσότερο από βαφή: αποτελούσε […]
Το Βυζάντιο συνδέθηκε όσο λίγοι πολιτισμοί με το χρώμα και τον συμβολισμό του. Η περίφημη πορφύρα ήταν κάτι πολύ περισσότερο από βαφή: αποτελούσε […]-
Καλησπέρα Παναγιώτη. Πολύ ενδιαφέρουσες πληροφορίες. Το Br στον τίτλο που κολλάει; Στο βρώμιο αναφέρεσαι;
-
α, σόρι, τωρα κατάλαβα, υπάρχει βρώμιο στο μόριο της πορφύρας
-
Καλησπέρα αγαπητέ Πορφυρογέννητε Θοδωρή !
-
Γεια σου Παναγιώτη. Για το Tyrian Purple ένα άρθρο, που κατά σύμπτωση διάβασα χθες. Λέγεται ότι για να παραχθεί ένα γραμμάριο βαφής, έπρεπε να χρησιμοποιηθούν περίπου 12000 πορφύρες!
-
Καλησπέρα Αποστολε Παλαιολογε! Πολύ χρήσιμη η πληροφορία σου , δεν ήξερα την τόσο μεγάλη αξία της χρωστικής. Σ’ ευχαριστώ πολυ
……. Μήπως να κάνεις ένα τομέα για οικονομικά μαθηματα κατεύθυνσης στο Υλικονετ ; Καλό απόγευμα -
Παναγιώτη, είμαι ο τελευταίος που θα μπορούσε να κάνει κάτι τέτοιο. Ομολογώ ότι δεν σκαμπάζω τίποτε από οικονομικά, εκτός από αυτό: τα όμορφα πράγματα στη ζωή μας δεν αποτιμώνται με οικονομικούς όρους.
-
Αποστόλη τα είπες όλα με το ‘….τα όμορφα πράγματα στη ζωή μας δεν αποτιμώνται με οικονομικούς όρους.’
-
-
H/o Διονύσης Μάργαρης έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Κίνηση φορτισμένου σφαιριδίου
 Ένα μικρό σφαιρίδιο μάζας m=80g είναι δεμένο στο άκρο κατακόρυφου μονωτικού νήματος μήκους l=0,4m, το άλλο άκρο του οποίου έχει δεθεί σε σταθερό σημεί […]
Ένα μικρό σφαιρίδιο μάζας m=80g είναι δεμένο στο άκρο κατακόρυφου μονωτικού νήματος μήκους l=0,4m, το άλλο άκρο του οποίου έχει δεθεί σε σταθερό σημεί […] -
H/o Αποστόλης Παπάζογλου έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Bungee τραμπολίνο
 Το bungee τραμπολίνο είναι ένα παιχνίδι, αποτελούμενο από σύστημα ελαστικών ιμάντων, τα πάνω άκρα των οποίων είναι ακλόνητα στερεωμένα. Ο αναβάτης δένεται […]
Το bungee τραμπολίνο είναι ένα παιχνίδι, αποτελούμενο από σύστημα ελαστικών ιμάντων, τα πάνω άκρα των οποίων είναι ακλόνητα στερεωμένα. Ο αναβάτης δένεται […]-
Καλησπέρα Αποστόλη. Ωραία άσκηση. Μόλις την είδα δεν πρόσεξα ότι είναι στην Α και άρχισα να υπολογίζω τη σταθερά επαναφοράς της α.α.τ., η οπoία παρεπιπτόντως για μικρές μετατοπίσεις βγαίνει 2k.
-
Καλημέρα Ανδρέα και σε ευχαριστώ. Αν η ελαστική δυναμική ενέργεια διδασκόταν στην Α Λυκείου, θα μπορούσε να είχε και συνέχεια. Τώρα περιοριζόμαστε στην ισορροπία.
-
-
H/o Διονύσης Μάργαρης έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Το ελατήριο και η τριβή.
 Ένα σώμα μάζας m=2kg, ηρεμεί σε οριζόντιο επίπεδο, δεμένο στο άκρο ιδανικού ελατηρίου σταθεράς k=60Ν/m, το οποίο έχει το φυσικό μήκος του l0 (θέση Α). Ο […]
Ένα σώμα μάζας m=2kg, ηρεμεί σε οριζόντιο επίπεδο, δεμένο στο άκρο ιδανικού ελατηρίου σταθεράς k=60Ν/m, το οποίο έχει το φυσικό μήκος του l0 (θέση Α). Ο […] -
H/o Ανδρέας Ριζόπουλος έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Μια διάσπαση και η συνάντηση μέσα σε μαγνητικά πεδία
 Στον χώρο υπάρχουν δύο οριζόντια ομογενή μαγνητικά πεδία, με εντάσεις μέτρων Β1 / Β2 = 4/3. H κατεύθυνση των δυναμικών γραμμών φαίνεται στο παρακάτω σχήμ […]
Στον χώρο υπάρχουν δύο οριζόντια ομογενή μαγνητικά πεδία, με εντάσεις μέτρων Β1 / Β2 = 4/3. H κατεύθυνση των δυναμικών γραμμών φαίνεται στο παρακάτω σχήμ […]-
Αφιερωμένη στο Διονύση, που έδωσε ΕΔΩ την ιδέα με τις συντεταγμένες.
-
Το λιγότερο εντυπωσιακή…. δεν τολμώ να σκεφτώ πόσο χρόνο διέθεσες
για όλα αυτά….και μέχρι να καταλήξεις στα κατάλληλα αριθμητικά δεδομέναΜπράβο Ανδρέα
-
Καλησπέρα Αντρέα
Θα συμφωνήσω με το Θοδωρή πως η άσκηση κρύβει πολύ δουλειά από πίσω.
Νομίζω το ξεκίνημα είναι το πιο δύσκολο. Αναφέρομαι στη διατήρηση του ηλεκτρικού φορτίου. Γιατί όσο και να τονίζεται στη Γ γυμνασόυ στο λύκειο δεν χρησιμοπιείται όπως η διατήρηση της ορμής η οποία θα είναι από τις πρώτες σκέψεις κάποιου διαβάζοντας την άσκηση. -
Καλησπέρα συνάδελφοι. Σας ευχαριστώ. Θοδωρή η μελέτη εργασιών άλλων καλών συναδέλφων του υλικού, δημιουργεί γενέσεις, όπως ένα σουπερνόβα γίνεται αιτία νέας αστρογένεσης. Μακάρι να αξιοποιηθεί από κάποιον η άσκηση.
Χρήστο, να θυμηθούμε ότι στην Πυρηνική Φυσική εξοικειώνονταν οι μαθητές με την ΑΔΗΦ, αλλά πάνε αυτές οι εποχές… -
Καλημέρα Ανδρέα και συγχαρητήρια για το πόνημά σου!!
Ευρηματική, ενδιαφέρουσα, πρωτότυπη η άσκησή σου.
Να είσαι πάντα καλά. -
Καλησπερα Ανδρέα. Πολύ όμορφη.
Θα την δυσκολευες αν:
α) Ζητούσες να αποδειχθεί ποτέ θα συναντηθούν (όταν το α κάνει μια “περιστροφή” ανεβαίνει έστω κατα Ψ ενώ το b σε μια περιστροφή ανεβαίνει κατά 2ψ ,έτσι συναντώνται(ΕΚΠ) όταν το b έχει κάνει μια περιστροφή και το α δυο.(βγαίνει από την σχέση των ακτίνων περιστροφής)
Β) Ξερουμε την μια ακτίνα αφού σε μέτρα έχουν ίδιες ορμές άρα ο λόγος των ακτίνων είναι 3/4 (=R1/R2) -
Καλησπέρα συνάδελφοι. Σας ευχαριστώ. Πρόδρομε οι κινήσεις των φορτισμένων σωματιδίων σε ηλεκτρικά και μαγνητικά πεδία, είναι ένας πολύ ενδιαφέρον τομέας αν σκεφτούμε π.χ. τους επιταχυντές. Και μπορούν να δώσουν πολλά θέματα…
Γιώργο πολύ ωραία η πρότασή σου. Η μεθοδος με το ΕΚΠ είναι και εύκολα κατανοητή από τους μαθητές. -
Καλημέρα Ανδρεα.
.Σίγουρα η άσκηση δεν είναι εύκολη για τους μαθητές.
Στοχεύει περισσοτερο στις δεξιότητές τους και ειναι λιγοτερο διδακτική.
Απευθυνομενοι σε κάποιους πολύ καλούς μαθητές μπορεί η παρέμβαση μου να τους προβληματισει δημιουργικα και να συνεισφέρει στις δεξιότητές τους. -
Καλό απόγευμα Ανδρέα και σε ευχαριστώ για την αφιέρωση.
Ωραίο σενάριο!!!
ΥΓ
Άργησα λίγο να την δω… αλλά ποτέ δεν είναι αργά… -
Καλησπέρα Διονύση. Εσύ έβαλες τους άξονες. Απλώς έβαλα ένα άτομο στο Ο…
-
-
H/o Παναγιώτης Κουτσομπόγερας έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Ανίχνευση προπανίου
 Η ανίχνευση του προπανίου είναι σημαντική για την προστασία από διαρροές εύφλεκτου αερίου σε οικιακούς και βιομηχανικούς χώρους. Μπορεί να γίνει συνήθως […]
Η ανίχνευση του προπανίου είναι σημαντική για την προστασία από διαρροές εύφλεκτου αερίου σε οικιακούς και βιομηχανικούς χώρους. Μπορεί να γίνει συνήθως […]-
Για περισσότερα, εδώ: https://www.draeger.com/el_gr/Products/Short-term-Tubes
-
Καλημέρα Παναγιώτη και καλή Κυριακή.
Οξειδώνεται το προπάνιο από το διχρωμικό;
Με ξάφνιασες… -
Καλημέρα αγαπητέ Διονύση και καλή Κυριακή. Ναι είναι όντως διαφορετικό, αν δεις στα φιαλίδια ανίχνευσης μεταβάλλεται όντως το χρώμα του διχρωμικού ιόντος, οξειδώνονται και άλλα αλκάνια όπως και άλλοι υδρογονάνθρακες, το Cr μπορεί να παίξει και τον ρολο καταλύτη/οξειδωτικου. Εδώ μερικές πηγές: https://www.sciencedirect.com/science/article/abs/pii/S0920586111007541
-
Καλημέρα Παναγιώτη.
Από τη στιγμή που το έγραψες εσύ, δεν είχα καμιά αμφιβολία, ότι η αντίδραση γίνεται!
Δεν χρειάζονται αποδείξεις!
Απλά εξέφρασα τον ξάφνιασμά μου, αφού για χρόνια δίδασκα το αντίθετο… -
ΑΠΑΝΤΗΣΕΙΣ
1. Αριθμός οξείδωσης (Α.Ο.) κάθε C στο C3H8- Ακραίοι C (CH3): -3
- Κεντρικός C (CH2): -2
2. Μέσος Α.Ο. των ατόμων C
((-3 + (-2) + (-3))/3 = -8/3
3 εξίσωση
3 C3H8 + 10 K2Cr2O7 + 40 H2SO4 → 9 CO2 + 10 Cr2(SO4)3 + 10 K2SO4 + 52 H2O
4.Συνολική μεταβολή Α.Ο. του αναγωγικού
60
5.Χρωματική μεταβολή- Κ2Cr2O7 (πορτοκαλί) → Cr2(SO4)3 (πράσινο)
6.Mol K2Cr2O7 που χρησιμοποιήθηκαν
- 2,5 mL × 0,4 M = 0,001 mol
Mol C3H8 που αντέδρασαν
- 3 C3H8 : 10 K2Cr2O7 → n(C3H8) = 0,001 × 3/10 = 0,0003 mol
Όγκος C3H8 σε STP
- V = 0,0003 × 22,4 L = 0,00672 L
Συγκέντρωση σε ppm στον χώρο
- ppm = 0,00672 / 1344 × 10⁶ = 5 ppm
- Πολύ κάτω από το όριο 250 ppm → χώρος ασφαλής
-
Σύγχρονοι αισθητήρες (από GEMINI) (Physics & Chemistry together ! )
Οι σύγχρονοι αισθητήρες έχουν αντικαταστήσει τους χημικούς σωλήνες (σαν αυτόν με το διχρωμικό) γιατί προσφέρουν συνεχή παρακολούθηση και ταχύτητα δευτερολέπτου. Στη βιομηχανία χρησιμοποιούνται κυρίως τρεις τεχνολογίες:
1. Καταλυτικοί Αισθητήρες (Pellistors)
Είναι οι πιο συνηθισμένοι για την ανίχνευση του προπανίου.- Πώς λειτουργούν: Μέσα στον αισθητήρα υπάρχει ένα μικρό σπιράλ πλατίνας (καταλύτης) που θερμαίνεται. Όταν το προπάνιο έρθει σε επαφή μαζί του, “καίγεται” (οξειδώνεται) πάνω στην επιφάνεια του καταλύτη.
- Το αποτέλεσμα: Η καύση αυτή αυξάνει τη θερμοκρασία του σπιράλ, η οποία αλλάζει την ηλεκτρική του αντίσταση. Αυτή η μεταβολή μεταφράζεται ακαριαία σε ένδειξη συγκέντρωσης (ppm).
2. Αισθητήρες Υπερύθρων (NDIR – Non-Dispersive Infrared)
Αυτοί είναι “έξυπνοι” γιατί δεν χρειάζονται οξυγόνο ή χημική αντίδραση.- Πώς λειτουργούν: Το προπάνιο έχει την ιδιότητα να απορροφά το υπέρυθρο φως σε ένα πολύ συγκεκριμένο μήκος κύματος. Ο αισθητήρας στέλνει μια δέσμη υπερύθρων· αν υπάρχει προπάνιο, η δέσμη εξασθενεί.
- Το πλεονέκτημα: Δεν “δηλητηριάζονται” από άλλα χημικά και αντέχουν χρόνια χωρίς συντήρηση.
3. Φωτοϊονισμός (PID – Photo-Ionization Detectors)
Αυτοί χρησιμοποιούνται για εξαιρετικά υψηλή ακρίβεια (όπως τα 5 ppm που βρήκαμε στην άσκησή σου).- Πώς λειτουργούν: Μια λάμπα UV “βομβαρδίζει” τα μόρια του αερίου και τα ιονίζει (τους αποσπά ηλεκτρόνια). Τα ιόντα παράγουν ένα μικρό ηλεκτρικό ρεύμα που μετράται.
-
Καλημέρα Διονύση -χρειάζονται έντονες συνθήκες – σ’ ευχαριστώ, αλλά πολλές φορές κάνω λάθη – έβαλα κι ενα υπολογιστικό ερώτημα για την ασφάλεια του προσωπικού, ελπίζω να σου αρέσει! Η αντίδραση που αναγράφεται έχει προσαρμοστεί για τις ανάγκες/γνώσεις των μαθητών. Καλή Κυριακή !
-
CH3 – CH2 – CH3 —- > 3 CO2
CH3 – σε CO2 … από (-3) σε (+4) ==> 7 αύξηση
-CH2- σε CO2 … από (-2) σε (+4) ==> 6 αύξηση
CH3 – σε CO2 … από (-3) σε (+4) ==> 7 αύξησηΣυνολική αύξηση ΑΟ : 20 ( συντελεστής στο Cr2(SO4)3 … 10 )
Συνολική μείωση ΑΟ : 3 ( συντελεστής στο 3 CO2 …3 … οπότε 9 CO2 )ΣΜΑΟ αύξησης 3×20 = 60
ΣΜΑΟ μείωσης 10x2x3 = 60( H χρήση του 8/3 δεν είναι χημικώς ορθή )
-
Καλημέρα σας. Παναγιώτη ενδιαφέρουσες πληροφορίες και επίκαιρες για την ανίχνευση του προπανίου. Διονύση πολλές οργανικές ουσίες οξειδώνονται με τα συνήθη οξειδωτικά, υπερμαγγανικό και διχρωμικό. Τα προγράμματα σπουδών στη β/θμια και τα βιβλία μάλλον έχουν γραφτεί με τη λογική “τι οξειδώνεται χωρίς διάσπαση ανθρακικής αλυσίδας”. Αναφέρονται στην οξείδωση των αλκοολών, των αλδευδών και δύο καρβοξυλικών οξέων. Σε αυτές έχουμε οξείδωση που οδηγεί στο σχηματισμό άλλης λειτουργικής (χαρακτηριστικής) ομάδας χωρίς διάσπαση ανθρακικής αλυσίδας, ενώ στην περίπτωση των οξέων σχηματίζεται CO2 χωρίς όμως πάλι διάσπαση ανθρακικής αλυσίδας (με εξαίρεση μια διάσπαση στο οξαλικό). Το γιατί έχει γίνει αυτή η επιλογή, δεν ξέρω. Κάτι που μπορώ να υποθέσω είναι ότι, συνήθως, χρησιμοποιούμε τις οργανικές αντιδράσεις για να κάνουμε μετασχηματισμούς σε λειτουργικές ομάδες, στην προσπάθειά μας να συνθέσουμε κάποια οργανική ένωση. Οι οξειδώσεις σε έντονες συνθήκες που οδηγούν σε διάσπαση αλυσίδας ίσως, σε πολλές περιπτώσεις, δεν έχουν μεγάλη παρασκευαστική αξία διότι τα προιόντα δεν είναι πολύ ελεγχόμενα. Έτσι, μάλλον θεώρησαν “too much” το να συμπεριλάβουν στο πρόγραμμα τέτοιες οξειδώσεις. Ωστόσο σε πανεπιστημιακά βιβλία Οργανικής Χημείας αλλά και σε ξενόγλωσσα δευτεροβάθμιας που έχω δει, αναφέρονται οι οξειδώσεις υδρογονανθράκων. Στο λύκειο λέμε ότι οι τριτοταγείς αλκοόλες και οι κετόνες δεν οξειδώνονται χωρίς διάσπαση της ανθρακικής τους αλυσίδας. Κάτι ανάλογο ίσως θα έπρεπε να λέμε και για τους υδρογονάνθρακες.
-
Έλα ρε Αντώνη, έγραφα και τώρα είδα την απάντησή σου! Καλως τονα!
ΥΓ. Κι ας άργησε! -
Και ας διαφωνούμε! Εγώ νομίζω ότι η χρήση του -8/3 μια χαρά είναι!
-
Μαθηματικώς λειτουργεί … χημικώς υπάρχει ΜΟ των ΑΟ ατόμων C ?
Εάν (όλοι) οι C δεν έδιναν κοινό προϊόν πως θα κάναμε ισοστάθμιση ?
Προφανως αφου πολλαπλασιάζεται ( η διαφορά (+4) – ( -8/3) ) το 20/3 με το 3 ( από τους άνθρακες ) και μετά ξανά από το 3 ( του συντελεστή ) δίνει το ίδιο ΣΜΑΟ ( 60 ).
Απλά δεν χρησιμοποιώ μέσους όρους στους ΑΟ … (Ίσως να είναι ) γούστα ( μόνο ) αυτά …No worries
-
Εγώ θεωρώ ότι μέσος όρος μπορεί να εκφραστεί για οποιοδήποτε σύνολο τιμών. Αυτό δεν παραβιάζει τη χημεία! Αυτή είναι η γνώμη μου. Έτσι κι αλλιώς, ο αριθμός οξείδωσης είναι μια θεωρητική επινόηση των χημικών, ένα “λογιστικό σύστημα” παρακολούθησης των μετατοπίσεων των ηλεκτρονίων στις οξειδοαναγωγικές αντιδράσεις. Δεν αντιστοιχεί σε κάποια φυσική ποσότητα. Με τον μέσο όρο των ΑΟ βρίσκουμε τη μεταβολή του ΑΟ ανά άτομο, δηλαδή τον μέσο όρο της μεταβολής. Θεωρώ ότι είναι μια εναλλακτική “τεχνική” που μας βοηθά να ισοσταθμίσουμε. Έτσι κι αλλιώς, η κάθε διαδικασία ισοστάθμισης μια τεχνική είναι. Αλλά οκ, δεν νομίζω ότι είναι τόσο σημαντικό το θέμα. Ας επιλέξει ο καθένας ότι θέλει.
-
-
H/o Διονύσης Μάργαρης έγραψε ένα νέο άρθρο πριν από 2 μήνες, 1 εβδομάδα
Τρία ιόντα του χαλκού στο σύνθετο πεδίο.
 Ένα μονοσθενές ιόν του 63Cu+ (ιόν Α) εισέρχεται με ταχύτητα υ σε μια περιοχή, στην οποία συνυπάρχουν δύο ομογενή πεδία, ένα ηλεκτρικό με ένταση όπως στο σ […]
Ένα μονοσθενές ιόν του 63Cu+ (ιόν Α) εισέρχεται με ταχύτητα υ σε μια περιοχή, στην οποία συνυπάρχουν δύο ομογενή πεδία, ένα ηλεκτρικό με ένταση όπως στο σ […]-
Έτσι πρέπει να είναι τα θέματα.
4 ερωτήματα χωρίς εμπλοκή ετερόκλητων. -
Καλό απόγευμα Γιάννη.
Σε ευχαριστώ για το σχόλιο και για τις 4 ερωτήσεις 🙂
Έτσι διαπίστωσα ότι είχα κάνει λάθος την αρίθμηση, αφού οι ερωτήσεις ήταν 6! -
Καλημέρα Διονύση. Πολύ καλή. Πλήρης διερεύνηση του φίλτρου ταχυτήτων και της επίδρασης του σύνθετου πεδίου. Τα τρία ιόντα που έχεις επιλέξει, δίνουν τη δυνατότητα να παίξει ο υποψήφιος με τους παράγοντες, φορτίο και μάζα εξάγοντας χρήσιμα συμπεράσματα.
Ο χαλκός έχει 28 ραδιενεργά ισότοπα, από Cu 55, ως Cu 84. Μόνο αυτά που έχεις στην άσκηση ειναι σταθερά. -
Καλό απόγευμα Ανδρέα και σε ευχαριστώ για το σχολιασμό.
Δίκιο έχεις για τα ισότοπα του χαλκού. Γι΄αυτό και η επιλογή τους… -
Καλησπέρα Διονύση,
Το ξετίναξες. Θεωρώ πολύ σημαντικό την αρχικό σταδιο που επιταχύνονται από την τάση V τα φορτία όπου παίζει ρόλο και η μάζα και το φορτίο για την ταχύτητα εισόδου στο σύνθετο πεδίο. -
Καλημέρα και καλή βδομάδα Χρήστο.
Σε ευχαριστώ για το σχολιασμό.
-
-
H/o Διονύσης Μάργαρης έγραψε ένα νέο άρθρο πριν από 2 μήνες, 2 εβδομάδες
H Σοφία Ζαχαράκη και το Εθνικό Απολυτήριο.
 Τους βασικούς άξονες και μια πρώτη αποτύπωση του σχεδιασμού για το Εθνικό Απολυτήριο έδωσε σήμερα στη δημοσιότητα το Υπουργείο Παιδείας […]
Τους βασικούς άξονες και μια πρώτη αποτύπωση του σχεδιασμού για το Εθνικό Απολυτήριο έδωσε σήμερα στη δημοσιότητα το Υπουργείο Παιδείας […]-
Καλημέρα Διονύση.
Και πριν τελειώσω την ανάγνωση το πρώτο διαμάντι:
Στο επίκεντρο τίθεται όχι μόνο το τι μαθαίνουν οι μαθητές, αλλά και ποιες γνώσεις και δεξιότητες χρειάζεται να αποκτήσουν ώστε να μπορούν να συμμετέχουν ενεργά στην κοινωνία. -
Καλημέρα Γιάννη και Διονύση.
Γιάννη δές και παρακάτω:
Παράλληλα αναφέρθηκε και στην πρόθεση να μειωθεί τόσο ο αριθμός των εξεταζόμενων μαθημάτων όσο και η εξεταστέα ύλη, με στόχο την αποσυμφόρηση του προγράμματος σπουδών και την ενίσχυση της ουσιαστικής μάθησης -
Γεια σου Γρηγόρη.
Έχουν αποφασίσει και το ποια είναι η ουσιαστική μάθηση!!
Σώσον Κϋριε. -
Καλημέρα παιδιά. Μην γκρινιάζουμε. Ο Γιάννης έχει γράψει πολάκις ότι θα πάμε σε απόκτηση δεξιοτήτων του είδους πώς να περνάμε τις γριες στο απέναντι πεζοδρόμιο. Και όσο η χώρα μας γερνάει, αυτό θα είναι όλο και πιο απαραίτητο 🙂
-
Διαβάζω:
Σύμφωνα με την κυρίαρχη πρόταση, τα γραπτά των μαθητών θα διορθώνονται σε πρώτο στάδιο ενδοσχολικά, στη συνέχεια όμως θα ψηφιοποιούνται και μέσω σκαναρίσματος του QR code θα υπόκεινται σε δειγματοληπτικούς ελέγχους, ώστε να αποτρέπεται το φαινόμενο της υπερβαθμολόγησης.Σήμερα τα γραπτά είναι καλυμμένα.
Βαθμολογούνται από ανθρώπους που μένουν και δουλεύουν σε άλλες περιοχές. Που δεν έχουν κανένα λόγο να υπερβαθμολογήσουν το άγνωστο γραπτό.
Τα θέματα παραδίδονται από αγνώστους συναδέλφους οι οποίοι και επιτηρούν.
Πολύ δύσκολα θα μπορέσει κάποιο μέλος της επιτροπής του σχολείου να βοηθήσει, υπαγορεύσει λύσεις, υποδείξει το σωστό από τα σου-λου ή πολλαπλής επιλογής. Εκτίθεται. Θα συμβεί το ίδιο σε ένα σχολείο μικρής περιοχής ή σε ένα σχολείο που οι σχέσεις των διδασκόντων με μαθητές και γονείς είναι άλλες;Το σύστημα των Εξετάσεων έχει και σήμερα προβλήματα αλλά είναι κατά τεκμήριο αδιάβλητο. Αν και αυτό το καταστρέψουμε …..
Εκτός βέβαια αν αυτό που ενδιαφέρει είναι το άδειασμα των δημόσιων σχολείων.
Να μην πληρώνουμε και πολλούς μισθούς. -
Αποστόλη για τις δεξιότητες έχω γράψει στο:
Ο απατεώνας και ο αφελής.
Οι δεξιότητες εκτιμώνται και ο όρος έχει αποκτήσει θετικό πρόσημο.
Έτσι βλέπουμε και το Skills4life
Να το μεταφράσουμε ως “ζωτικές δεξιότητες” ή ως “δεξιότητες για τη ζωή”; -
Διαβάζω ακόμα ότι η Τράπεζα Θεμάτων επικαιροποιείται και ενισχύεται με 2.500 νέα θέματα, βασισμένα στα νέα προγράμματα σπουδών.
Πολλά;
Ο Διονύσης έχει ξεπεράσει τα 4.460 θέματα!!
Αν κάποιος σκέφτηκε ότι “Ουκ εν τω πολλώ το ευ” ας τα συγκρίνει με τα Τραπεζικά θέματα. -
Γεια σας παιδιά.
Το 1996 είμαστε έτοιμοι να εφαρμόσουμε το Εθνικό Απολυτήριο. Το είχε μελετήσει ο τότε υπουργός, Γιώργος Παπανδρέου.
Ένας ανασχηματισμός του Σημίτη, το ανέβαλε μέχρι ο Αρσένης να φέρει το δικό του νόμο.
Εντάξει μόνο 30 χρόνια έχουν περάσει, ακόμη το ψάχνουμε το …Απολυτήριο! Πού θα μας πάει; Θα το εφαρμόσουμε…
Όσον αφορά Γιάννη για τις εξετάσεις, οι σημερινές πανελλαδικές παραμένουν λέει, προς το παρόν, μέχρις ότου…
Απλά δεν ξέρω τότε για ποιο πράγμα μιλάμε. Τι θα κάνει το νέο εθνικό; Θα αποκτήσει αξία το Απολυτήριο;
Ποια αξία; -
Καλησπέρα συνάδελφοι. Επανέρχεται η ΕΣΑ = Εθνικό Σώμα Αξιολογητών, μην το μπερδεύουμε με το (ΕΑΤ-ΕΣΑ). Θα είναι κάτι σαν την Επιθεώρηση Εργασίας; 4 υπάλληλοι για ολόκληρη την περιφέρεια Θεσσαλίας;
Αυτή η κυβέρνηση έχει δείξει την αγάπη της για τη Δημόσια Παιδεία, όπως και κάθε τι Δημόσιο, οπότε να μην ανησυχούμε. Όλα γίνονται με διάλογο, δεν υπάρχει τίποτα προαποφασισμένο, πάντα για το καλό μας.
Το εξεταστικό σύστημα τους φταίει. Οι ίδιοι που το δημιουργούν, χωρίς να ρωτάνε κανέναν, οι ίδιοι το βρίσκουν προβληματικό μετά από λίγα χρόνια! Βάζουν και τους φίλους τους στα ΜΕΣΑ ΜΑΖΙΚΗΣ ΕΞΗΜΕΡΩΣΗΣ να πιπιλίσουν πόσο λάθος είναι το εξεταστικό, αυτό φταίει για όλα και πρέπει να αλλάξει για μια ακόμα φορά. “Ορκιζόμαστε θα είναι η τελευταία”.
Τι τραγελαφικοί τύποι! Βάζουν επικεφαλίδα:
“το Λύκειο έχει σταδιακά χάσει την παιδαγωγική του αυτονομία και λειτουργεί κυρίως ως μηχανισμός εξεταστικής προετοιμασίας”.
και ετοιμάζουν ένα σύστημα με εξετάσεις και στις τρεις τάξεις.
Με Τράπεζα Θεμάτων! Ώστε να ακυρώσουν πλήρως την παρουσία του καθηγητή μέσα στην τάξη. Ας βάλουν και ένα ρομποτ να λύνει ασκήσεις μόνο από την τράπεζά τους. Θα δουλεύει άνετα 13ωρο. -
Ανδρέα προς στιγμήν μου φάνηκε πως καλαμπούριζες με το “ΕΣΑ”.
Έτσι προσέφυγα στην ΤΝ και έλαβα:Τα αρχικά για το Εθνικό Σώμα Αξιολογητών είναι ΕΣΑ.
Πρόκειται για έναν θεσμό που ανακοινώθηκε πρόσφατα (Ιανουάριος/Φεβρουάριος 2026) από το Υπουργείο Παιδείας, Θρησκευμάτων και Αθλητισμού, στο πλαίσιο των αλλαγών για το Εθνικό Απολυτήριο και την εισαγωγή στην τριτοβάθμια εκπαίδευση.
Σύμφωνα με τις τρέχουσες μεταρρυθμίσεις:- Το ΕΣΑ θα αποτελείται από εκπαιδευτικούς αυξημένων προσόντων οι οποίοι θα επιλέγονται με αυστηρά κριτήρια.
- Αποστολή του θα είναι η βαθμολόγηση των γραπτών στις εξετάσεις που θα διεξάγονται σε εθνικό επίπεδο (όπως αυτές της Β’ και Γ’ Λυκείου για το Εθνικό Απολυτήριο).
- Σκοπός της δημιουργίας του είναι η διασφάλιση της αντικειμενικότητας, της εγκυρότητας και του αδιάβλητου της βαθμολόγησης των μαθητών σε όλη τη χώρα.
Η σύσταση του Σώματος συνδέεται άμεσα με τη λειτουργία της Εθνικής Αρχής Εξετάσεων και την αναμόρφωση της Τράπεζας Θεμάτων.
-
Αμέσως μετά σκέφτηκα ότι τα θέλει ο οργανισμός τους.
Θα ονόμαζες εσύ κάτι με όνομα βεβαρυμμένο;
Θα ονόμαζες ‘Γκεστάπο” τη βάρκα σου αντί “Μαργιωρή”;
Θα ήθελες ο εγγονός να ονομαστεί ‘Εφιάλτης” αντί “Ανδρέας” ή έστω “Φοίβος”;Δεν υπάρχει συναίσθηση;
-
Επιτέλους. 40 τοσα χρόνια περίμενα το Λύκειο να αποβάλει τον εξετασιοκεντρικό χαρακτήρα του.
όλα τα ελληνόπουλλα να συναγωνίζονται με ίσους όρους και να αξιολογούνται μαθητές , καθηγητές , σχολεία , από την ΕΣΑ.
Ήρθε ο Αρσένης να βάλει τέλος στην ανισότητα και να εξασφαλίσει ίσες ευκαιρίες για όλα τα παιδιά από Γαύδο ως Διδυμότειχο. Όμως δεν πρόλαβε. Δεν ξαναβγήκε βουλευτής.
Το ίδιο συνέβη με Αρβανιτόπουλο,Διαμαντοπούλου,Γιαννάκου,
Γαβρογλου.
Έκανα λοιπόν την εξής ερώτηση σε φίλη μου
1)Είναι καιρός πλέον το λύκειο να αποβάλλει τον εξετασιοκεντρικό χαρακτήρα του.
2)Όλοι οι μαθητές να συναγωνίζονται με ίσους όρους.
3)Κοινά θέματα από Γαύδο ως Διδυμότειχο. Τέρμα οι ανισοτητες. Αξιολόγηση συνεχής.
Το εθνικό απολυτήριο θα καταφέρει να θεραπεύσει ή έστω να αμβλύνει όλα τα παραπάνω???
Επισυνάπτω την απάντηση αν και δεν κρύβω ότι τρόμαξα. -
Καμία εκπαιδευτική μεταρρύθμιση δεν είναι ταξικά ουδέτερη. Το σχολείο στον καπιταλισμό:
δεν λειτουργεί μόνο ως χώρος γνώσης,
αλλά ως μηχανισμός αναπαραγωγής της εργατικής δύναμης (Althusser) και ταξικής ιεραρχίας.
Το εθνικό απολυτήριο, με κεντρικές και συνεχείς εξετάσεις, εμφανίζεται ως:«αξιοκρατία», «αντικειμενικότητα», «ίσο μέτρο για όλους»
Στην πράξη όμως λειτουργεί ως φίλτρο ταξικής επιλογής.- Παιδί εργατικής οικογένειας:
- γονείς σε εξαντλητικά 13ωράρια
- λιγότερος χρόνος υποστήριξης
- άγχος, επισφάλεια, εργασία από νωρίς
- Παιδί μικροαστικής/αστικής οικογένειας:
- φροντιστήρια
- ιδιαίτερα
Οι συνεχείς εξετάσεις δεν μετρούν μόνο γνώση, αλλά:
αντοχή στο άγχος
εξοικείωση με τον εξεταστικό μηχανισμό- πρόσβαση σε εξωσχολική υποστήριξη
Δηλαδή μετρούν ταξικό υπόβαθρο.
Το εθνικό απολυτήριο:
απαλλάσσει το κράτος από την ευθύνη για:- ισότιμη δημόσια εκπαίδευση
- καθολική στήριξη των μαθητών
- μετατρέπει την αποτυχία σε ατομικό φταίξιμο
Ο μαθητής που «δεν τα καταφέρνει»:δεν είναι θύμα κοινωνικών ανισοτήτων είναι ανεπαρκής, δεν προσπαθει,δεν είναι άξιος
το μέτρο:
πειθαρχεί τη νεολαία
μαθαίνει την υποταγή στην αξιολόγηση
προετοιμάζει για:
επισφαλή εργασία
συνεχή έλεγχο- «δια βίου αξιολόγηση»
Το σχολείο γίνεται προθάλαμος αγοράς εργασίας, όχι χώρος χειραφέτησης.
Τελικά ποιοι θα τα καταφέρνουν?
όχι οι πιο ικανοί
αλλά όσοι έχουν ταξικά εφόδια
Το μέτρο:
θα αυξήσει τη σχολική διαρροή
θα σπρώξει παιδιά της εργατικής τάξης:
σε πρόωρη εργασία
σε χαμηλής ειδίκευσης διαδρομές
θα νομιμοποιήσει τις ανισότητες με το μανδύα της δικαιοσύνης.
Το «εθνικό απολυτήριο» δεν έρχεται να καταργήσει τις ανισότητες, αλλά:
να τις κατανείμει νωρίτερα
Έτσι θα υπάρξει μεγάλη σχολική διαρροή και επομένως πιο γρήγορα φθηνή εργασία.
Το κράτος- Μειώνει κόστος
Μεταφέρει την ευθύνη
«δεν φταίει το σχολείο, φταίει ο μαθητής»
Το μέτρο δεν είναι αυταρχικό κατά λάθος.
Είναι δομικά αυταρχικό.
Οι συνεχείς εξετάσεις:
σκοτώνουν τη συλλογική μάθηση
μετατρέπουν τη γνώση σε:- βαθμό
- μόρια
- πιστοποίηση
Το παιδί μαθαίνει:
όχι να κατανοεί τον κόσμο
αλλά να επιβιώνει σε μηχανισμούς αξιολόγησης
Για τα παιδιά της εργατικής τάξης:
το σχολείο γίνεται χώρος φόβου
η αποτυχία γίνεται εσωτερικευμένη ντροπή
«δεν είμαι ικανός» αντί «το σύστημα είναι άδικο»
Αυτό είναι ιδεολογική βία, όχι παιδαγωγική. -
Το «Εθνικό Απολυτήριο» στην πράξη συνεπάγεται πολλαπλασιασμό εξετάσεων και αξιολογικών φραγμών. Στην ουσία σε κάθε τάξη του Λυκείου οι εξετάσεις θα έχουν τον χαρακτήρα πανελλαδικών εξετάσεων με τους εφήβους να ζουν διαρκώς σε συνθήκες με το Λύκειο να μετατρέπεται σε εξεταστικό κάτεργο
Όσο αυξάνονται οι εξεταστικοί φραγμοί, τόσο οικογένειες με οικονομική δυνατότητα θα μπορούν να προσφέρουν στα παιδιά τους περισσότερη υποστήριξη, ενώ οι εργατικές και λαϊκές οικογένειες θα οδηγούνται σε νέα αδιέξοδα.
Είναι φανερό ότι η κυβέρνηση και το υπουργείο παιδείας – αντιμετωπίζοντας και την εκπαίδευση ως ένα ακόμη επιχειρηματικό πεδίο κι όχι ως κοινωνικό αγαθό – επιλέγουν την εισαγωγή επιχειρηματικών πρακτικών και τη διόγκωση των ταξικών ανισοτήτων
«Άλογα κούρσας» και «ουραγοί», ταξικά οριοθετημένοι, στο νέο αριστοκρατικό Λύκειο που ετοιμάζεται.
Με το νέο σύστημα, το σχολείο θα μεταλλαχθεί απόλυτα σε μηχανισμό διαρκούς αξιολόγησης, όπου οι μαθητές και οι μαθήτριες θα ζουν υπό το άγχος τριετών εξετάσεων, με αποτέλεσμα να εξουδετερώνονται η έννοια της γενικής παιδείας, η όποια κριτική σκέψη, να εξαϋλώνεται ο ρόλος των εκπαιδευτικών του σχολείου αφού μετατρέπονται σε προγυμναστές των θεμάτων της περίφημης Τράπεζας ενώ ταυτόχρονα διευρύνονται οι κοινωνικές και ταξικές ανισότητες.
Εξαφανίζεται ο ρόλος των εκπαιδευτικών ενός σχολείου στις ενδοσχολικές εξετάσεις και αντικαθίστανται από μια απρόσωπη τράπεζα θεμάτων που δεν γνωρίζει στο ελάχιστο τις δυσκολίες, τα προβλήματα, την κοινωνικοοικονομική κατάσταση μαθητών και περιοχής φοίτησής τους.
Η θέσπιση εθνικού απολυτήριου αποτελεί διακαή πόθο του αστισμού ήδη από τα μέσα της δεκαετίας του 1990. Όλες οι οδηγίες των υπερεθνικών οργανισμών (Ε.Ε, ΟΟΣΑ) η έκθεση Πισσαρίδη, ΣΕΒ απαιτούν την εφαρμογή του Εθνικού Απολυτήριου ως ένα από τα βασικά εργαλεία των αντιδραστικών αναδιαρθρώσεων μετάλλαξης της δημόσιας εκπαίδευσης με στόχο την βίαιη εκδίωξη των εφήβων από το δημόσιο Λύκειο και την τριτοβάθμια εκπαίδευση προς την φθηνή, ευέλικτη επαγγελματική κατάρτιση και μαθητεία.
Άθελα ή ηθελημένα μας λέει ότι στο νέο εξεταστικό σύστημα δεν χωράει η κριτική σκέψη, δεν χωράνε οι υπαρκτές κοινωνικές, πολιτισμικές διαφορές αλλά ο εξισωτισμός με βάση την αντικειμενοποίηση που επιβάλλει η εξουσία.
Δεν θα πρέπει να διαφεύγει στην οπτική μας ότι το Εθνικό Απολυτήριο συνδέεται άμεσα με την προσπάθεια επιβολής του πολλαπλού βιβλίου που έχει καταντήσει σαν το γεφύρι της Άρτας αφού η παράδοση τους πάει για το Σεπτέμβρη του 2027, αλλά και τα νέα αναλυτικά προγράμματα.
Υπάρχει άλλος δρόμος. Ο δρόμος της απελευθερωτικής παιδείας
Για ένα σχολείο που θα μορφώνει και δεν θα εξοντώνει. -
Γιάννη, η ερώτησή σου για το όνομα της βάρκας, μου θύμισε την πολύ καλή Γερμανική ταινία Der Vorname (How About Adolf). Σε ένα οικογενειακό δείπνο, ο πατέρας ανακοινώνει ότι σκοπεύει να ονομάσει το αγέννητο παιδί του Αδόλφο, κάτι που προκαλεί χάος, καβγάδες και ξεσπάσματα μεταξύ συγγενών και φίλων.
Γιώργο, τα είπες όλα.
Το παιδί μαθαίνει:
όχι να κατανοεί τον κόσμο
αλλά να επιβιώνει σε μηχανισμούς αξιολόγησης
Για τα παιδιά της εργατικής τάξης:
το σχολείο γίνεται χώρος φόβου
η αποτυχία γίνεται εσωτερικευμένη ντροπή
«δεν είμαι ικανός» αντί «το σύστημα είναι άδικο»
Αυτό είναι ιδεολογική βία, όχι παιδαγωγική.Ελπίζουμε ότι δε θα προλάβουν να τα εφαρμόσουν. Ας κυκλοφορούμε τη μπάλα στην άμυνα μέχρι να τελειώσει ο αγώνας.
-
-
H/o Παύλος Αλεξόπουλος έγραψε ένα νέο άρθρο πριν από 2 μήνες, 2 εβδομάδες
Κίνηση αγωγού εντός Ο.Μ.Π.
 Δύο κατακόρυφοι μεταλλικοί αγωγοί Αx και Γy, μεγάλου μήκους, απέχουν μεταξύ τους απόσταση ℓ = 1 m και έχουν αμελητέα ωμική αντίσταση. Τ […]
Δύο κατακόρυφοι μεταλλικοί αγωγοί Αx και Γy, μεγάλου μήκους, απέχουν μεταξύ τους απόσταση ℓ = 1 m και έχουν αμελητέα ωμική αντίσταση. Τ […]-
Γεια σου Παύλο. Ουσιώδης (ειδικά το γ) και κομψή. Κατάλληλη για μαθητές. Να είσαι καλά.
-
Σε ευχαριστώ Δημήτρη για το σχόλιο και χαίρομαι που σου αρέσει.
-
Γεια σου Πάυλο.
Ωραία άσκηση με το τρίτο ερώτημα πιο όμορφο που μάλλον θα ήταν και η αφορμή για την κατασκευή της άσκησης. -
Γεια σου Χρήστο, σε ευχαριστώ για το σχόλιο. Έχεις δίκιο ακριβώς έτσι κινήθηκα.
-
Καλημέρα Παύλο, υπέροχη άσκηση με διδακτικό ενδιαφέρον! Ως φοιτητής πλέον σποραδικά ρίχνω μια ματιά στη σχολική πραγματικότητα. Θυμάμαι πέρυσι ότι η τελευταία άσκηση που έκανα με τον καθηγητή μου (Θέμα Δ) τελείωνε ακριβώς έτσι. Ο αγωγός μέσω μεταβλητής δύναμης ανέρχεται με σταθερή ταχύτητα 4m/s και με την κατάργηση της F επιβραδύβεται μέχρι να σταματήσει και τέλος κατέρχεται αποκτώντας uοριακή=2m/s. Ζητούμενο ήταν ο ρυθμός μεταβολής της κινητικής ενέργειας του αγωγού τη στιγμή που ο ρυθμός με τον οποίο εκλύονταν θερμότητα στον αντιστάτη είναι το 1/4 της μέγιστης τιμής του (δηλαδή τη στιγμή που η ταχύτητα είναι η μισή της μέγιστης). Δεν προλάβαμε όμως ποτέ να το δούμε ούτε είδα τη λύση (η άσκηση δεν ήταν πρωτότυπη αλλά παρμένη από βοήθημα). Έπρεπε να σκεφτούμε ότι η μέγιστη ταχύτητα σε όλη τη διάρκεια του φαινομένου είναι 4m/s (και όχι 2) άρα για την ταχύτητα τη συγκεκριμένη χρονική στιγμή ισχύει u=2m/s και συνεπώς να πάρουμε περιπτώσεις; Στην άνοδο θα έβγαινε μία αρνητική τιμή και στην κάθοδο 0J/s.
-
Γεια σου Απόστολε. Σε ευχαριστώ για το σχόλιο και χαίρομαι που σου αρέσει η άσκηση. Καλές σπουδές εύχομαι!
-
- Φόρτωσε Περισσότερα
Καλησπέρα Παναγιώτη
Φονικά όπλα με βάση τα δηλητήρια από βάτραχους όχι στον Αρκτικό αλλά στην Αμαζονία.
Βέλη με αιχμές που τρίφτηκαν στο δέρμα δηλητηριωδών βατράχων της ζούγκλας, όταν το δηλητήριο είναι πολύ ισχυρό.
Αλλιώς, το δηλητήριο συλλέγεται ψήνοντας τους βατράχους στη φωτιά.
Χρήση: στις εμπλοκές με μέλη άλλων φυλών και στο κυνήγι.
Το δηλητήριο κυκλοφορούσε στο αίμα των θυμάτων – όχι στο μυϊκό σύστημα, οπότε μετά το μαγείρεμα τα θηράματα ήταν ακίνδυνα για βρώση.
Ένα εντυπωσιακό χαρακτηριστικό των βατράχων με δηλητήριο που σχετίζεται με την Δαρβίνεια Προσαρμογή.
Ο βαθμός τοξικότητας των βατράχων συνδυάζεται με όσο πιο έντονα χρώματα στο δέρμα τους ενώ παράλληλα αυτά τα αμφίβια εξελίχθηκαν αποκλειστικά σε ημερήσιους θηρευτές.
Αυτά τα χρώματα σχετίζονται με τη διατροφή που έχεις ήδη αναφέρει Παναγιώτη. Μυρμήγκια, σαρανταποδαρούσες, ακάρεα.
Αυτά τα χαρακτηριστικά τους λειτουργούν ως χρωματική προειδοποίηση για τους ανταγωνιστές τους και χάρις στην ανάρτησή σου έμαθα ότι ονομάζονται αποσηματισμός.
Καλημέρα Γιώργο και σ’ ευχαριστω για τον χρονο σου και την απαντηση – σκεφτομουν την δομή και το περιεχομενο των αναρτησεων σου, οταν με το ΑΙ εφτιαχνα αυτη την αναρτηση. Εντυπωσιακη η Δαρβίνεια Προσαρμογή οπως και ο αποσηματισμος που δεν γνωριζα, οποτε σ’ ευχαριστουμε (και) γι’ ‘αυτό!
Πώς ανιχνεύθηκε η ουσία; Δείτε με κλικ ΕΔΩ.